Úvod
Lamotrigin představuje platnou možnost v léčbě bipolární poruchy.1 Pacienti s bipolární poruchou tráví téměř 40% svého života v depresivní fázi a nejdůležitější účinky lamotriginu spočívají v prevenci bipolární deprese.2 Mezi další výhody lamotriginu patří jeho dobrá snášenlivost, příznivý kognitivní profil a adherence k pacientům.3 Tento profil je zvláště užitečný pro bipolárních pacientů vzhledem k jejich nízké míře adherence k léčbě.4 Jeho použití však bylo omezeno kvůli riziku potenciálně závažných dermatologických reakcí, zejména Stevens-Johnsonova syndromu a toxické epidermální nekrolýzy.5 Známé rizikové faktory pro tento typ reakcí patří rychlé zvýšení dávky, současné užívání kyseliny valproové, předchozí vyrážka spojená s antikonvulzivy v anamnéze, ženy a mladší než 13 let.6,7 Při zavedení se standardním postupným zvyšováním i V dávkování se míra závažných kožních reakcí s lamotriginem snižuje z 1% na 0,1–0,01% .8 Míra benigních kožních reakcí se však nezměnila, zůstává mezi 8% a 11% .9 Vzhled benigních vyrážka je problémem pro lékaře, kteří mají k dispozici několik terapeutických alternativ, které jsou účinné při bipolární depresi. Aby se zabránilo této nežádoucí reakci, byla pro pacienty, kteří zahajují léčbu lamotriginem, stanovena řada preventivních opatření10, aniž by bylo možné snížit míru výskytu, jak ukazuje nedávná randomizovaná studie.11 Obnovení léčby lamotriginem s pomalejší titrací dávky je strategie obvykle používaná, když se objeví vyrážka. To obvykle začíná dávkou 5 mg / den, pokud je jeho použití klinicky oprávněné. Neexistují však žádné rozsáhlé studie, které by identifikovaly konkrétní a spolehlivé ukazatele, které by umožnily předem předpovědět selhání nebo úspěch této strategie. V této studii byly podrobně popsány některé markery, které předpovídají nežádoucí účinky při obnovení léčby lamotriginem po výskytu vyrážky. Toho bylo dosaženo studií otevřených případů a přehledem existující literatury.
Série MethodCase
Po vymývacím období 5 poločasů jakoukoli předchozí psychotropní medikací užívanou účastníkem byla zahájena léčba lamotriginem jeho účinnost a snášenlivost při léčbě bipolární poruchy typu I a II. Účastníci byli ve věku od 18 do 57 let a splňovali kritéria DSM-IV pro bipolární poruchu typu I a II. Navíc byli v depresivní nebo smíšené fázi poruchy. Porucha byla potvrzena pomocí klinického rozhovoru DSM-IV. Pacienti měli hodnotu ≥20 na Hamiltonově škále pro hodnocení deprese (17 položek) 12 a hodnotu ≤12 na Young Mania Rating Scale.13 Kritéria pro vyloučení zahrnovala diagnózu další osy I, přítomnost velké depresivní epizody trvající 12 měsíců, porucha užívání návykových látek nebo závislost (DSM-IV) (kromě nikotinu) nebo jiné klinicky významné zdravotní onemocnění. Studie byla schválena místní etickou komisí a byla provedena v souladu se standardy správné klinické praxe. Před každým zařazením do studie byl od každého subjektu získán informovaný souhlas.
Během vymývacího období nebylo povoleno požití benzodiazepinů. Pacienti s bipolární poruchou, u které se během 4 měsíců po zahájení léčby lamotriginem objevila vyrážka, byli v průběhu roku 2010 prospektivně identifikováni na ambulantním psychiatrickém oddělení. Pro posouzení intenzity vyrážky byla použita pětibodová stupnice na základě intenzity a lokalizace ohniska (tabulka 1) .14
Klasifikace lézí vyrážky.
| Třída | Klinické charakteristiky vyrážka / propuknutí |
| stupeň 1 | Makulární nebo papulární ohnisko nebo erytém bez souvisejících příznaků |
| Stupeň 2 | Makulární nebo papulární ohnisko nebo erytém se svěděním nebo jinými souvisejícími příznaky. Lokalizovaný peeling nebo jiné léze, které pokrývají |
| stupeň 3 | generalizovaná erytrodermie nebo makulární, papulární nebo vezikulární ohnisko. Peeling pokrývá ≥ 50% BSA |
| stupeň 4 | generalizovaná exfoliativní, ulcerózní nebo bulózní dermatitida |
| Stupeň 5 | Těžký, život ohrožující Stevens-Johnsonův syndrom |
Na obr. 1 je několik příkladů vyrážkových lézí podle jejich závažnost.V obou případech byla závažnost ohniska kontrastována s potenciálním přínosem lamotriginu. Informovaný souhlas byl získán od každého z pacientů považovaných za vhodné pro obnovení lamotriginu. Případy lézí stupně 3–5 byly vyloučeny z důvodu možnosti rozvoje Stevens-Johnsonova syndromu nebo epidermální nekrolýzy. V případě benigních lézí (stupeň 1) byl učiněn pokus o zlepšení vyrážky snížením dávky lamotriginu. Pokud nedošlo k žádnému zlepšení, léčba byla přerušena a byla navržena možnost později obnovit léčbu. Než bylo možné znovu zahájit léčbu, musely uplynout alespoň 2 týdny. V tomto okamžiku léčba začala dávkou lamotriginu 5 mg denně nebo 5 mg každý druhý den u pacientů současně léčených kyselinou valproovou. Denní dávka byla zvyšována o 5 mg každé 2 týdny, dokud nebylo dosaženo dávky 25 mg / den, kdy by titrace pokračovala podle pokynů výrobce.15 Jeden pacient nedodržoval správně plán obnovy léčby (titroval rychleji, než bylo doporučeno) ; nicméně tento pacient byl do analýzy zahrnut. K analýze zlepšení pomocí lamotriginu byla použita stupnice CGI-I (Clinical Global Impression-Improvement) .16

Příklady vyrážkových lézí / ohnisek.
Recenze literatury týkající se Studie nebo studie lamotriginu s opakovaným podáváním
Hledání Medline bylo provedeno pomocí klíčových slov „lamotrigin“ a „vyrážka“ (n = 240). Abstrakty byly zkontrolovány, aby byly identifikovány ty studie, kde byl lamotrigin obnoven poté, co se objevila vyrážka, s použitím pomalejšího titrace dávky než v počáteční plán (n = 8). Kromě toho byly přezkoumány odkazy v uvedených studiích (n = 4). Data extrahovaná ze zmíněných publikací byla hodnocena a ohniska byla klasifikována podle stupnice v tabulce 1. Data získaná z tohoto přehledu literatury byla zkombinována s aktuální řadou případů za účelem vytvoření metaanalýzy. Byla provedena post hoc analýza s cílem posoudit, zda riziko vyrážky při obnovení léčby lamotriginem po propuknutí choroby je spojeno se závažností vypuknutí choroby nebo s intervalem mezi počátečním vypuknutím choroby a opětovnou výzvou.
Řada ResultsCase
Z 80 pacientů léčených lamotriginem pro bipolární poruchu typu I nebo II se u 15 (18,75%) objevila kožní vyrážka během 2 měsíců po léčbě; 10 z těchto pacientů podstoupilo opětovné podávání lamotriginu. Opakovaná výzva představovala nepříznivé výsledky u 2 pacientů: u 1 se vyvinula závažná vyrážka 4. stupně a u druhé se objevila vyrážka 3. stupně. U žádného pacienta se během počáteční léčby nebo opakované léčby lamotriginem nevyvinul Stevens-Johnsonův syndrom nebo epidermální nekrolýza (tabulka 2).
Charakteristika pacientů, kteří podstoupili opětovné podávání lamotriginu.
| Předmět | Diagnostika | Věk | Sex | Vyrážka (týdny) | Závažnost | Interval mezi ukončením a opětovnou výzvou | Výsledek | CGI-I |
| 1 | BP I | 28 | F | 2 | 1 | 14 | + | 2 |
| 2 | deprese BP II | 45 | F | 2 | 2 | 19 | + | 1 |
| 3 | deprese BP II | 37 | F | 3 | 2 | 16 | + | 1 |
| 4 | BP I deprese | 49 | M | 1 | 2 | 17 | + | 2 |
| 5 | BP není zadán | 51 | M | 3 | 2 | 21 | + | 1 |
| 6 | deprese BP II | 56 | M | 2 | 2 | 16 | + | 2 |
| 7 | BP I | 29 | M | 3 | 1 | 23 | + | 1 |
| 8 | BP II | 37 | M | 2 | 2 | 29 | + | 1 |
| 9 | BP II deprese | 41 | F | 1 | 3 | 28 | – | 5 |
| 10 | deprese BP II | 53 | F | 1 | 3 | 34 | – | 6 |
5 pacientů, kteří nepodstoupili opětovné podávání lamotriginu, se spontánně zotavilo z vyrážky po snížení dávky (n = 1), poté, co byli převedeni na jiný lék (n = 2) nebo poté, co odmítli pokračovat léčba (n = 1). Závažnost vyrážky u pacientů, kteří podstoupili opakovanou léčbu, oscilovala mezi 1. a 2. stupněm (průměr = 1,75). U 2 pacientů, kteří podstoupili rechallenge s nepříznivými výsledky, se vyskytla vyrážka stupně 3. Kromě toho po opětovném podání se znovu objevily potenciálně závažné puchýřovité kožní vyrážky na zádech a obličeji, kromě horečky, eozinofilie a slizničních puchýřů v ústní dutině, které po léčbě kortikosteroidy a vysazení lamotriginu ustoupily. Z pacientů, kteří podstoupili rechallenge, 37,5% uvedlo zlepšení později. Tito pacienti také v metaanalýze získali výsledky 1 a 2 (zlepšení a výrazné zlepšení) ve srovnání s výchozí hodnotou po opětovném podání lamotriginu.
Obnovili jsme 69 případů extrahovaných z 12 publikací, ve kterých byl znovu zahájen lamotrigin bylo provedeno po vyrážce (tabulka 3). 17–22
V 18% případů se po obnovení léčby objevila kožní reakce. Přerušení léčby tyto reakce vyřešilo, ale nebyly hlášeny žádné závažné reakce stupně 4 nebo 5 naznačující Stevens-Johnsonův syndrom nebo toxickou epidermální nekrolýzu. Většinou šlo o retrospektivní nebo prospektivní případy, zatímco 4 z nich byly jednorázové studie. 19,21,23,24 Ve 30% případů byl lamotrigin znovu podáván v dávce vyšší než 5 mg / den, kvůli původně vysokým hodnotám počáteční dávky vyšší než 200 mg / den v prvním týdnu. Míra pozitivních výsledků se v těchto případech nelišila od míry zjištěné při opětovném podávání dávky 5 mg / den (83% oproti 89%). Vztah mezi rizikem vyrážky během opětovného podávání a intervalem čekání, jakož i vztah mezi rizikem a počáteční závažností vyrážky, byl studován post hoc analýzou. To zahrnovalo dříve publikované případy, které byly vhodné pro analýzu, získané z přehledu literatury (n = 26 pro závažnost, n = 48 pro interval). Míra pozitivních výsledků při opětovném podání po benigní vyrážce (stupeň 1) byla 100%. U vyrážek 2. a 3. stupně byla míra relapsu navzájem podobná (31,25%, respektive 33,3%). Počáteční vyrážka stupně 3 měla 66,7% míru relapsu (tabulka 4).
2 současné případy, které podstoupily opakovanou léčbu po vyrážce stupně 3, nevykazovaly příznivý vývoj. Místo toho se objevila závažnější vyrážka s puchýři na zádech, tváři a v ústní dutině, které ustoupily poté, co 2 pacienti přerušili léčbu.
Pokud jde o souvislost mezi relapsem vyrážky během opakované léčby a intervalem mezi ukončením léčby a obnovení léčby lamotriginem výsledky ukázaly, že čím kratší je interval, tím vyšší je riziko relapsu (obr. 2).Tento účinek se stal zvláště významným, když byl lamotrigin obnoven za méně než 2 týdny, ve srovnání s obnovením po 4 týdnech (46% oproti 2%, P = 0,001) (tabulka 5).
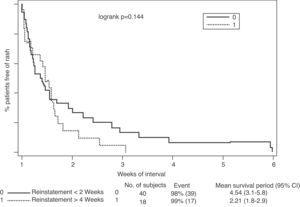
Míra vyrážky podle intervalu opakované výzvy lamotriginu.
Diskuze
Výsledky této studie podpořily myšlenku titrace lamotriginové rechallenge po vyrážce pomocí nižších dávek. V případě kožních reakcí 1. stupně lze poslední dávku snížit o 25–50 mg s monitorováním, dokud vyrážka neustoupí. Poté mohla titrace pokračovat se zvyšujícími se dávkami, dokud nebylo dosaženo klinické stabilizace. Pokud vyrážka neustupuje, můžete přerušit podávání lamotriginu a retitrovat dávku pomalejším tempem po 4–6 týdnech bez výskytu kožních vyrážek. V případě kožních vyrážek stupně 2 můžete postupovat podle předchozího plánu s větší opatrností ohledně přetrvávání kožní reakce. U závažnějších vyrážek (jako je stupeň 3 nebo 4) se opětovné podávání nedoporučuje, jak bylo prokázáno v případech 2 pacientů v této studii se špatným vývojem. Post hoc analýzy naznačují, že čekání 4–6 týdnů po zlepšení vyrážky před obnovením léčby lamotriginem je alternativou, která nabízí větší bezpečnost ve srovnání s méně konzervativními zprávami.10 Pokud je nutné pokračovat v léčbě lamotriginem navzdory přetrvávání vyrážky, může zvolit kombinaci lamotriginu s riluzolem23 nebo s valproátem. 19,25 Riluzol a lamotrigin inhibují glutamát blokováním sodíkových kanálů. První byl studován u rezistentní deprese a jako náhrada lamotriginu po silné vyrážce. Kombinace lamotriginu a inhibitoru enzymu umožňuje snížit hladinu lamotriginu při zachování jeho terapeutické účinnosti. Další alternativou, kterou lze použít před vysazením lamotriginu v případě vyrážky, je konzultace s dermatologem, který má zkušenosti s tímto typem ohniska, v rozumném intervalu 48–72 hodin. Pokud je však konzultace ještě zpožděna, riskuje pacient zhoršení vyrážkových lézí. V tomto okamžiku se doporučuje, aby se pacient uchýlil k dalším alternativám, jako je obnovení léčby nižší dávkou nebo přerušení léčby a obnovení léčby o 2–4 týdny později. Pokud jde o léčbu vyrážek kortikosteroidy, mohou zhoršit depresivní nebo smíšený stav bipolární poruchy, a proto je vhodné se jim co nejvíce vyhnout.26
Etické zveřejnění
Ochrana lidí a zvířat. Autoři prohlašují, že dodržované postupy odpovídají etickým standardům odpovědné komise pro experimentování s lidmi a jsou v souladu se Světovou lékařskou asociací a Helsinskou deklarací. Důvěrnost údajů. Autoři prohlašují, že dodržovali protokoly svého pracovního centra týkající se zveřejňování údajů o pacientech a že všichni pacienti zahrnutí do studie obdrželi dostatečné informace a písemně vyjádřili souhlas k účasti na uvedené studii. Právo na soukromí a informovaný souhlas. Autoři prohlašují, že v tomto článku nejsou uvedena žádná data pacientů.
Střet zájmů
Autoři nemají žádný střet zájmů, který by mohli deklarovat.