Klinický případ
Prezentována 45letá žena s 20letou anamnézou Crohnovy choroby s horečkou, zimnicí a únavou po dobu 10 dnů. Krátce před nástupem příznaků podstoupila pacientka nekomplikovanou kolonoskopii, při které jí byla provedena 17 biopsií pro sledování nebo polypektomii. Během kolonoskopie byla její Crohnova choroba v remisi a nebyl zaznamenán žádný zánět sliznice.
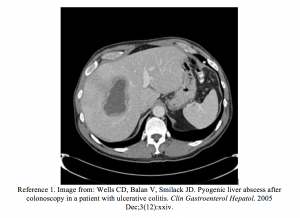
V ED byly vitální funkce pacienta HR 110, BP 120/80, RR 18, T 102,5. Měla mírnou citlivost pravé horní části břicha. Laboratorní studie odhalily zvýšený počet bílých krvinek (15 000) a zvýšené AST a ALT (120/137 U / L) s mírně zvýšenou alkalickou fosfatázou 200 IU / L. Počítačová tomografie (CT) skenování břicha odhalilo několik oblastí s nízkým útlumem v pravém jaterním laloku v souladu s jaterními abscesy. Byla vypěstována drenáž abscesů a rostl Streptococcus anginosus. K vymizení všech lézí došlo poté, co byly odstraněny intervenční radiologií, a pacient dostal 6týdenní léčbu intravenózními antibiotiky.
Úvod
Kolonoskopie je běžně prováděný postup při diagnostice a léčbě široké škály stavů, včetně rakoviny, zánětlivých onemocnění střev, polypů, krvácení a striktur. Podle Americké rakovinové společnosti se screeningová kolonoskopie doporučuje každých 10 let počínaje věkem 50 let. U vysoce rizikových pacientů, jako jsou pacienti se zánětlivým onemocněním střev, se kolonoskopie provádí častěji. Tento postup je stále nejúčinnějším způsobem, jak najít a odstranit malé předrakovinné polypy, a tím snížit riziko úmrtí na rakovinu tlustého střeva a konečníku.
Obecně je kolonoskopie velmi bezpečná. Systematický přehled 12 studií z roku 2008 s celkovým počtem 57 742 kolonoskopií provedených pro screening průměrného rizika ukázal celkovou míru závažných nežádoucích účinků pouze 2,8 na 1000 postupů a úmrtnost 0,007% .2 Riziko kolonoskopie však není napříč skupinami konstantní a některé komplikace jsou častější než ostatní. Starší dospělí mají ve srovnání s mladšími pacienty zvýšené riziko závažných komplikací. Ve studii s 53 220 kolonoskopiemi měli pacienti ve věku 80 až 84 let významně vyšší výskyt závažných komplikací ve srovnání s pacienty ve věku 66 až 69 let. Riziko závažných komplikací bylo také zvýšeno u pacientů s komorbidními stavy, jako je anamnéza cévní mozkové příhody, CHOPN, fibrilace síní a srdeční selhání.
Pyogenní jaterní absces (PLA) je vzácná, ale závažná komplikace kolonoskopie . Většina komplikací kolonoskopie se projeví do 7 dnů, ale PLA se může objevit o několik dní nebo dokonce týdnů později a historie nedávné kolonoskopie nemusí být ani vyvolána, pokud si klinický lékař není vědom této entity.4-6 Kvůli opožděné povaze PLA, je pravděpodobné, že tito pacienti budou diagnostikováni na pohotovostním oddělení.
Další pozdní komplikace, jako je postpolypektomický elektrokoagulační syndrom, a častější problémy se zpožděným krvácením, nespecifickými bolestmi břicha, reakcemi na sedativní látky a perforaci lze pozorovat také v ED. Naproti tomu v ED bude zřídka vidět exploze plynu nebo okamžité krvácení, protože tyto problémy se obvykle rychle vyskytují v sadě endoskopie, kde jsou řešeny naléhavě. Lékaři ED si musí být vědomi všech možných komplikací a jejich časového průběhu a mít nástroje pro správnou diagnostiku a léčbu nešťastného pacienta po kolonoskopii, který trpí vážnou komplikací.
Komplikace
Pyogenní Absces jater
PLA je nebezpečné onemocnění s vysokou morbiditou a mortalitou, které se vyskytuje u 10 až 20 případů na 100 000 hospitalizací.4-6 S pokrokem v diagnostických technikách a intervencích se úmrtnost zlepšuje.7 Pacienti jsou však stále ve vážném nebezpečí, zejména pokud je diagnóza opožděna, jak to často bývá, protože pacienti se mohou projevovat nespecificky. Retrospektivní studie 63 pacientů s PLA ukázala, že horečka byla častá (59%), ale další příznaky a příznaky, jako je bolest v pravém horním kvadrantu, a peritoneální příznaky, byly přítomny pouze u 39%, respektive 14%. 8 Diagnóza v této studii byla často zpožděno v průměru o jeden týden od nástupu příznaků.
Kolonoskopie je vzácné, ale také pravděpodobně nedostatečně uznávané srážedlo PLA. Předpokládá se, že tiché mikroperforace během procedury vedou k infekci, která může naočkovat játra portálním oběhem. Podobně mohou jiné intraabdominální infekce, jako je divertikulitida, potenciálně způsobit PLA, pokud je infikovaná oblast vyčerpána portální žílou.9 Jaterní clearance bakterií prostřednictvím portálové sítě je u zdravých pacientů běžným jevem, ale obstrukce žlučových cest, špatná perfúze a vysoká bakteriální zátěž (jako v případě infekce nebo více biopsií během kolonoskopie naočkování krevního řečiště) mohou předisponovat k proliferaci a abscesu formace. Literatura popisuje přibližně 34% případů PLA jako kryptogenní, ale část z nich mohou dobře tvořit pacienti s nedávnou kolonoskopií, která nebyla uznána jako rizikový faktor pro chorobný proces.8
Většina izolátů PLA je polymikrobiálních a skládá se z normální střevní flóry. Krevní kultury jsou pozitivní v 33–65% případů, ale kultury abscesů jsou téměř všechny pozitivní.10 Nejčastěji izolovanými mikroorganismy jsou druhy Streptococcus (37%), Eserichia Coli (33%), druhy Bacteroides (24%), Klebsiella pneumoniae (18%) a mikroaerofilní streptokoky (12%). 10-11 Strep anginosus, nalezený v případě tohoto pacienta, je fakultativně anaerobním grampozitivním kokem a jedním z běžnějších organismů nalezených v PLA.
Okamžitá diagnóza PLA je kritická, protože i když se diagnostika a léčba zlepšuje, úmrtnost zůstává na 10%. 5,7 Infekční komplikace kolonoskopie jsou obecně vzácné, ale opět je pravděpodobně nedostatečně uznán kauzální vztah. Kolonoskopie se podílí alespoň na několika případech PLA. 12–14 Zdá se však, že přechodná systémová bakteremie, pozorovaná u 4% kolonoskopií, sama o sobě nezvyšuje riziko infekce.15 Spíše se předpokládá, že se infekce v PLA šíří prostřednictvím skutečných mikroperforací.
I když je známo, že upřímné perforace jsou relativně vzácné (méně než 0,1% kolonoskopií), výskyt a patofyziologie mikroperforací není zcela znám.16-17 Vyzbrojeni znalostmi této klinické klinický pracovník, který má dobrou historii a má vysoký index podezření, může rychleji diagnostikovat PLA u pacienta s nedávnou kolonoskopií.
Infekce
Je všeobecně přijímáno, že přechodná bakteremie po kolonoskopii dochází přibližně u 4% výkonů, i když rozsah je uváděn jako 0-25% a rizikové faktory pro bakteremii nejsou definovány.18 Vyšší výskyt bakteriémie se vyskytuje při běžných každodenních činnostech, jako je čištění zubů a žvýkání jídla. Ačkoli příznaky nebo příznaky systémové infekce u pacientů s přechodnou bakteremií jsou vzácné, pacienti mohou pociťovat horečku, zimnici a potíže připomínající vše od infekcí horních cest dýchacích po břišní infekce.18
Ačkoli přechodná bakteriémie je přijatelným rizikem kolonoskopie , neexistuje prokázaný přínos pro rutinní profylaxi antibiotiky a většina pacientů nebude užívat antibiotika podle postupu.18 Současné pokyny Americké společnosti pro gastroenterologii (ASGE) souhlasí s American Heart Association (AHA) a doporučují proti antibiotické profylaxi pro pacienti podstupující rutinní kolonoskopii.19
Může být obtížné odlišit příznaky přechodné bakterémie od skutečné infekce.18 Obecně platí, že pacienti s infekčními příznaky ve dnech následujících po kolonoskopii vyžadují laboratorní studie zahrnující krevní kultury a v závislosti na index podezření na perforaci, zobrazení břicha. 20-21 Pokud je podezření na perforaci nízké nebo jsou diagnostikovány s je vyloučeno, může být podána IV hydratace a antibiotika, pokud to vyžaduje klinický stav pacienta.
Krvácení
Krvácení po polypektomii může být buď okamžité, nebo opožděné. Okamžité krvácení je spojeno s technikami polypektomie, při nichž se nepoužívá kauterizace nebo pokud se pro zákrok používá smíšený proud. Zpožděné krvácení je častěji pozorováno u ED, protože okamžité krvácení je často detekováno v době zákroku a řešeno endoskopistou. Zpožděné krvácení lze pozorovat až 7 dní po zákroku. Předpokládá se, že k tomu dochází v důsledku odlupování eschary, která zakrývala cévu, nebo v důsledku rozšíření zóny tepelné nekrózy na neporaněnou tkáň, což by mohlo vést ke krvácení, pokud by šlo o cévu.19,22
Několik velkých studií uvádí krvácení u 1 až 6 na 1 000 kolonoskopií (0,1% – 0,6%). 22 Studie analyzující více než 50 000 kolonoskopií však zjistila, že míra GI krvácení se významně liší v závislosti na tom, zda byla provedena polypektomie. Po polypektomii dochází ke krvácení u 1–2%, přičemž vyšší míry jsou pozorovány při odstraňování větších polypů. Riziko post-polypektomického krvácení může být zvýšeno u pacientů s trombocytopenií nebo koagulopatiemi.23
Známé rizikové faktory pro krvácení po kolonoskopii zahrnují velikost polypu, počet odstraněných polypů, historii nedávného užívání antikoagulancií nebo polyp histologie.22 Kupodivu velké a velké studie nezjistily užívání aspirinu spojeného s post-polypektomickým krvácením.24-26
Pacienti se zpožděným krvácením mohou mít jakékoli známky krvácení nebo anémie, včetně únavy, slabosti , bledost, silné krvácení nebo sraženiny po otření, tachykardie, bolest na hrudi a dušnost.Pacienti mohou popsat hematochezii nebo melenu v závislosti na místě krvácení.
Počáteční léčba pacienta s podezřením na krvácení zahrnuje řešení základních dýchacích cest, dýchání a oběhu pomocí 2 intravenózních roztoků s velkým objemem, krystaloidních tekutin a srdeční monitorování. Pacienti s hrubým nižším GI krvácením mohou rychle dekompenzovat a měli by mít aktivní typ a screening v případě, že je nutná transfuze.
Zobrazování není vždy nutné a pokud je to možné, rozhodnutí o zobrazování by mělo být provedeno společně s GI poraďte se, nejlépe s lékařem, který provedl kolonoskopii. Opakovaná kolonoskopie je často diagnostickým a terapeutickým postupem volby. Americká vysoká škola radiologie dává kolonoskopii nejvyšší hodnocení vhodnosti, ale zahrnuje také CTA břicha / pánve a Tc-99m RBC skenování břicha / pánve jako možné vhodné diagnostické kroky.27
Pokud pacient je nestabilní a provádějící endoskopista není k dispozici, lékař ED by měl konzultovat obecnou intervenční radiologii (IR), GI a chirurgii.
Perforace
Kolonoskopická perforace (CP) je jednou z nejzávažnější a nejobávanější komplikace kolonoskopie. Ačkoli je CP vzácný, vede k vysoké morbiditě a mortalitě.28-32 Perforace může být výsledkem mechanických sil proti stěně střeva, barotraumatu nebo elektrokauterizaci a může vést k tvorbě abscesů, tvorbě píštělí, nitrobřišní sepse, prodlouženému pobytu v nemocnici a dokonce smrt.
CP se vyskytuje u přibližně 0,016% diagnostických kolonoskopií, ale lze jej pozorovat až u 5% terapeutických kolonoskopií.33-35 V závislosti na tom, co se skutečně dělo během kolonoskopie, může být riziko perforace vyšší nebo nižší než průměr, takže získání operativní zprávy nebo historie od endoskopisty může být užitečné při určování rizika.
Riziko CP pro různé kolonoskopické výkony: 1,36-37
– Screeningová kolonoskopie: 0,01-0,1%
-Anastomotická dilatace striktury: 0-6%
-Crohnova choroba dilatace striktury: 0-18%
-Stent umístění: 4%
-Colonicní dekompresní trubice umístění: 2%
-Colonicální endoskopická resekce sliznice 0-5%
Kromě událostí během postup, specifické rizikové faktory pro CP zahrnují pokročilý věk, mnohočetné komorbidity, divertikulózu, obstrukci, resekci polypů, polypy o velikosti větší než 1 cm nebo ty, které se nacházejí v pravém tlustém střevě, snížená pohyblivost tlustého střeva, existující slabost stěny tlustého střeva , předchozí neúplný pokus o kolonoskopii nebo endoskopická nezkušenost.20
U pacientů s CP se může projevit náhlá zhoršující se bolest břicha, po které následuje falešně uklidňující úplné rozptýlení bolesti, protože perforace dekomprimuje zanícený orgán. Jak se obsah GI nadále rozlévá do pobřišnice, objevují se zhoršující se bolesti a peritoneální příznaky. Příznaky se však budou lišit v závislosti na umístění a velikosti perforace, stupni prosakování fekálií do pobřišnice a věku a komorbiditách pacienta.
Je pozoruhodné, že perforace mohou být také retro-peritoneální, což odpovídá umístění vzestupného a sestupného tlustého střeva a jaterních a slezinových ohybů. Ačkoli nejčastějším příznakem perforace tlustého střeva je bolest břicha, mohou mít starší pacienti otupělou odpověď. Mezi další příznaky patří horečka, nevolnost, zvracení, dušnost, bolest na hrudi, bolest lopatky a bolest krku. Zejména retroperitoneální perforace mohou mít minimální nebo atypické příznaky a vitální funkce mohou vykazovat tachykardii a horečku, ale mohou být také normální.20
Počáteční léčba podezření na perforaci zahrnuje pozornost dýchacích cest, dýchání, cirkulace 2 velkoobjemové infuzní roztoky, krystaloidní tekutiny a srdeční monitor. Měly by být získány laboratoře včetně CBC, CMP, lipázy a získání typu a screeningu. Pacient by měl být přísně NPO s empirickými IV antibiotiky. Statické zobrazování s CT břicha / pánve nebo rentgenem břicha, pokud je nestabilní, by mělo být objednáno spolu s chirurgickým zákrokem na stat. 21
Post-polypektomický syndrom
Post-polypektomický syndrom, také známý jako postpolypektomický elektrokoagulační syndrom nebo syndrom transmurálního popálení, je výsledkem elektrokoagulačního poranění stěny střeva, což vede k transmurálnímu popálení a fokální peritonitidě bez upřímné perforace. ). Syndrom po polypektomii byl hlášen u 6 pacientů ze 16 318 kolonoskopií provedených v letech 1994 až 2002 ve velkém integrovaném zdravotním systému.39 Rizikové faktory pro tuto neobvyklou komplikaci nejsou známy.
Pacienti s post-polypektomickým syndromem jsou obvykle přítomni do 12 hodin po kolonoskopii s horečkou, tachykardií a bolestmi břicha. Avšak nástup příznaků může být opožděn až o 5–7 dní po výkonu.40 Pacienti mají často leukocytózu a mohou vykazovat rigiditu a tachykardii, což vše napodobuje perforaci tlustého střeva.41
Avšak na rozdíl od perforace, která může vyžadovat urgentní chirurgický zákrok, jsou pacienti s post-polypektomickým syndromem obvykle konzervativně léčeni intravenózními tekutinami, kontrolou bolesti a postupným zlepšováním stravy, s nebo bez antibiotik zaměřených na gram negativní a anaerobní patogeny.42 Méně závažné případy lze zvládnout i ambulantně perorálními antibiotiky a čirými tekutinami po dobu 1–2 dnů.42-43
Protože tito pacienti mohou být k nerozeznání od pacientů s perforací, jakýkoli pacient podezřelý z post-polypektomického syndromu zaručuje laboratoře a zobrazování. U syndromu po polypektomii bude CT obvykle vykazovat fokální zesílení stěny tlustého střeva s okolním uvíznutím tuku bez jakéhokoli extramurálního vzduchu, i když v mírných případech může být CT negativní.42 Bez ohledu na výsledek zobrazování, jako u perforace, pokud je syndrom po polypektomii pokud existuje podezření, měl by se pacient poradit s chirurgem.
Perly
- Kolonoskopie je široce používaný screeningový test u pacientů nad 50 let. Komplikace mohou být časné nebo opožděné. Lékaři EM by si měli být vědomi možných komplikací a jejich očekávané časové osy, aby mohli přesně diagnostikovat a zvládat všechny možné komplikace.
- Mezi komplikace patří krvácení, perforace, syndrom po polypektomii, infekce, výbuch plynu a pyogenní jaterní absces.
- Historie diagnostiky a léčby ED může vést o faktorech pacienta a samotném postupu (základní stavy, léky, odstranění polypů, použití kauterizace, okamžité krvácení).
- Pyogenní jaterní absces se může objevit 1–2 týdny po kolonoskopii s bolestí a horečkou v pravém horním kvadrantu.
- Velká část tlustého střeva je retroperitoneální. Retroperitoneální perforace mohou způsobovat vágní a atypické příznaky, index podezření proto musí být vysoký.
- Post-polypektomický syndrom může napodobovat perforaci a lze jej obvykle odlišit zobrazením.
Odkazy / Další čtení:
- Wells CD, Balan V, Smilack JD. Pyogenní jaterní absces po kolonoskopii u pacienta s ulcerózní kolitidou. Clin Gastroenterol Hepatol. Prosinec 2005; 3 (12): xxiv.
- Whitlock, E.P., Lin, J.S., Liles, E. a kol. Screening na kolorektální karcinom: cílený, aktualizovaný systematický přehled pro americkou pracovní skupinu preventivních služeb. Ann Intern Med. 2008; 149: 638–658.
- Warren JL, Klabunde CN, Mariotto AB, Meekins A, Topor M, Brown ML, Ransohoff. Nežádoucí účinky po ambulantní kolonoskopii v populaci Medicare. Ann Intern Med. 2009; 150 (12): 849.
- Johannsen EC, Sifri CD, Madoff LC. Pyogenní jaterní abscesy. Infekční Dis Clin North Am. 2000; 14: 547–63.
- Meddings L, Myers RP, Hubbard J a kol. Populační studie pyogenních jaterních abscesů ve Spojených státech: Incidence, úmrtnost a časové trendy. Jsem J. Gastroenterol. 2010; 105: 117–24.
- Kaplan GG, Gregson DB, Laupland KB. Populační studie epidemiologie a rizikových faktorů pro pyogenní jaterní absces. Clin Gastroenterol Hepatol. 2004; 2: 1032-8.
- Petri A, Höhn J, Hódi Z, Wolfárd A, Balogh A. Pyogenic absces jater – 20 let zkušeností. Srovnání výsledků léčby ve dvou obdobích. Langenbecks Arch Surg. 2002; 387: 27–31.
- Pang TC, Fung T, Samra J, Hugh TJ, Smith RC. Pyogenní jaterní absces: audit s desetiletou zkušeností. Svět J Gastroenterol. 2011; 17: 1622–30.
- Murarka S, Pranav F, Dandavate V. DisseminatedStreptococcus anginosus ze sigmoidní divertikulitidy. J Glob Infect Dis. 2011; 3: 79–81.
- Branum GD, Tyson GS, Branum MA, Meyers WC. Jaterní absces. Změny v etiologii, diagnostice a řízení. Ann Surg. 1990 Dec. 212 (6): 655-62.
- Gyorffy EJ, Frey CF, Silva J Jr, McGahan J. Pyogenní jaterní absces. Diagnostické a terapeutické strategie. Ann Surg. 1987 Dec. 206 (6): 699-705.
- Bonenfant F, Rousseau É, Farand P. Streptococcus anginosuspyogenic jaterní absces po screeningové kolonoskopii. Canadian Journal of Infectious Diseases & lékařská mikrobiologie. 2013; 24 (2): e45-e46.
- Ian G. Harnik. Pyogenní jaterní absces po maligní polypektomii. Digital Dis Sci. 2007; 52: 3524–5.
- Paraskeva KD, Bury RW, Isaacs P. Abscesy jater Streptococcus milleri: Neobvyklá komplikace po kolonoskopickém odstranění postižené rybí kosti. Gastrointest Endosc. 2000; 51: 357–8.
- Low DE, Shoenut JP, Kennedy JK a kol. Perspektivní hodnocení rizika bakteremie pomocí kolonoskopie a polypektomie. Dig Dis Sci. 1987; 32: 1239–43.
- Becker F, Nusko G, Welke J, Hahn EG, Mansmann U. Sledování po kolorektální polypektomii: Analýza přínosů a rizik německých doporučení pro dohled. Int J Colorectal Dis. 2007; 22: 929–39.
- Macrae FA, Tan KG, Williams CB. Směrem k bezpečnější kolonoskopii: Zpráva o komplikacích 5 000 diagnostických nebo terapeutických kolonoskopií. Střevo. 1983; 24: 376–83.
- Nelson, D.B.Infekční komplikace GI endoskopie: část II, exogenní infekce. Gastrointest Endosc. 2003; 57: 695–711.
- Khashab, M.A., Chithadi, K.V., Acosta, R.D. a kol. Antibiotická profylaxe pro GI endoskopii. Výbor pro standardy praxe ASGE. Gastrointest Endosc. 2015; 81: 81-89.
- Lohsiriwat V. Kolonoskopická perforace: Incidence, rizikové faktory, management a výsledek. World Journal of Gastroenterology: WJG. 2010; 16 (4): 425-430.
- American College of Radiology ACR Vhodnost Kritéria: Akutní (nelokalizované)
- Ko, C.W. a Dominitz, J.A. Komplikace kolonoskopie: velikost a řízení. Gastrointest Endosc Clin N Am. 2010; 20: 659–671.
- Warren JL, Klabunde CN, Mariotto AB, et al. Nežádoucí účinky po ambulantní kolonoskopii v populaci Medicare. Ann Intern Med 2009; 150: 849-57.
- Hui, A.J., Wong, R.M., Ching, J.Y. et al. Riziko krvácení z kolonoskopické polypektomie s antikoagulancii a antiagregačními látkami: analýza 1657 případů. Gastrointest Endosc. 2004; 59: 44–48.
- Sawhney, M.S., Salfiti, N., Nelson, D.B. et al. Rizikové faktory pro závažné opožděné postpolypektomické krvácení. Endoskopie. 2008; 40: 115–119
- Yousfi, M., Gostout, C.J., Baron, T.H. et al. Postpolypektomie krvácení do dolního gastrointestinálního traktu: potenciální role aspirinu. Jsem J. Gastroenterol. 2004; 99: 1785–1789.
- American College of Radiology ACR Vhodnost Kritéria: Radiologická léčba krvácení do dolního gastrointestinálního traktu. https://acsearch.acr.org/docs/69457/Narrative/ (Přístup k 16. červenci 2017).
- Lohsiriwat V, Sujarittanakarn S, Akaraviputh T, Lertakyamanee N, Lohsiriwat D, Kachinthorn U. Kolonoskopická perforace: zpráva ze školícího střediska endoskopie Světové gastroenterologické organizace v Thajsku. Svět J Gastroenterol. 2008; 14: 6722–6725.
- Iqbal CW, Cullinane DC, Schiller HJ, Sawyer MD, Zietlow SP, Farley DR. Chirurgická léčba a výsledky 165 kolonoskopických perforací z jedné instituce. Arch Surg. 2008; 143: 701–706; diskuse 706-707.
- Teoh AY, Poon CM, Lee JF, Leong HT, Ng SS, Sung JJ, Lau JY. Výsledky a prediktory úmrtnosti a tvorby stomie při chirurgickém řešení kolonoskopických perforací: multicentrický přehled. Arch Surg. 2009; 144: 9–13.
- Lüning TH, Keemers-Gels ME, Barendregt WB, Tan AC, Rosman C. Kolonoskopické perforace: přehled 30 366 pacientů. Surg Endosc. 2007; 21: 994–997.
- Mai CM, Wen CC, Wen SH, Hsu KF, Wu CC, Jao SW, Hsiao CW. Iatrogenní perforace tlustého střeva kolonoskopií: fatální komplikace u pacientů s vysokým anestetickým rizikem. Int J Colorectal Dis. Duben 2010; 25 (4): 449-54.
- Rathgaber SW, Wick TM. Míra dokončení a komplikace kolonoskopie v komunitní gastroenterologické praxi. Gastrointest Endosc. 2006; 64: 556–562.
- Damore LJ, Rantis PC, Vernava AM, Longo WE. Kolonoskopické perforace. Etiologie, diagnostika a léčba. Dis Colon Rectum. 1996; 39: 1308–1314.
- Repici A, Pellicano R, Strangio G, Danese S, Fagoonee S, Malesci A. Endoskopická mukosální resekce pro časnou kolorektální neoplázii: patologické základy, postupy a výsledky. Dis Colon Rectum. 2009; 52: 1502–1515.
- Chukmaitov A, Bradley CJ, Dahman B a kol. Sdružení technik polypektomie, objemu endoskopistů a typu zařízení s komplikacemi kolonoskopie. Gastrointest Endosc. 2013; 77: 436.
- Fisher DA, Maple DT a kol. Komplikace kolonoskopie. Výbor pro standardy praxe ASGE Gastrointest Endosc. 2011; 74: 745. Bolest břicha a horečka nebo podezření na absces břicha; Varianta 1: Pooperační pacient s horečkou. https://acsearch.acr.org/docs/69356/Narrative/ (Přístup k červenci 17,2017).
- Hirasawa K, Sato C, Makazu M a kol. Koagulační syndrom: Zpožděná perforace po kolorektální endoskopické léčbě. World Journal of Gastrointestinal Endoscopy. 2015; 7 (12): 1055-1061.
- Levin TR, Zhao W, Conell C, Seeff LC, Manninen DL, Shapiro JA, Schulman J. Komplikace kolonoskopie v integrovaném systému poskytování zdravotní péče. Ann Intern Med. 2006; 145 (12): 880.
- Kim HW. Co se liší mezi postpolypektomickou horečkou a postpolypektomickým koagulačním syndromem? Clin Endosc. 2014; 47 (3): 205–6.
- Stock C, Ihle P, Sieg A, Schubert I, Hoffmeister M, Brenner H Nežádoucí účinky vyžadující hospitalizaci do 30 dnů po ambulantním screeningu a nevyšetření kolonoskopií. Gastrointest Endosc. 2013 Mar; 77 (3): 419-29.
- Sethi A, Song LMWK. Nežádoucí účinky související s endoskopickou resekcí sliznice tlustého střeva a polypektomií. Gastrointest Endosc Clin N Am. 2015; 25 (1): 55–69.
- Benson BC, Myers JJ, Laczek JT. Syndrom elektrokoagulace popolypektomii: napodobovač perforace tlustého střeva. Case Rep Emerg Med. 2013; 2013 687931.