pahanlaatuinen suonensisäinen tulehdus
Sepsiksellä on viitattu pahanlaatuiseen suonensisäiseen tulehdukseen . Normaalisti voimakas, monimutkainen, immunologinen kaskadi varmistaa nopean suojavasteen mikro-organismien hyökkäykselle ihmisissä. Puutteellinen immunologinen puolustus voi antaa infektion vakiintua; liiallinen tai huonosti säännelty vaste voi kuitenkin vahingoittaa isäntää alkuperäiskehittyneiden tulehdusyhdisteiden sopeutumattomalla vapautumisella (katso alla oleva kuva).
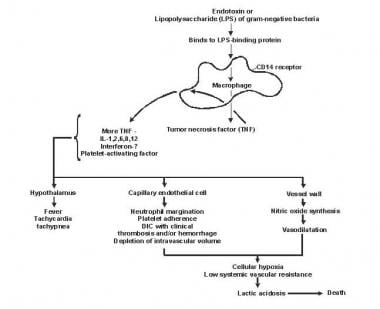 Sepsiksen ja moniorganistisen vajaatoiminnan patogeneesi.
Sepsiksen ja moniorganistisen vajaatoiminnan patogeneesi. Lipidi A ja muut bakteerituotteet vapauttavat sytokiinit ja muut immuunimodulaattorit, jotka välittävät sepsiksen kliinisiä ilmenemismuotoja. Interleukiinit, tuumorinekroositekijä (TNF) -α, gammainterferoni (IFN-y) ja muut pesäkkeitä stimuloivat tekijät tuotetaan nopeasti muutamassa minuutissa tai tunnissa monosyyttien ja makrofagien vuorovaikutuksesta lipidi A: n kanssa.
Tulehduksellisesta välittäjäaineen vapautumisesta tulee itsestimuloiva prosessi, ja muiden vastaavien välittäjien vapautuminen, mukaan lukien interleukiini (IL) -1, verihiutaleiden aktivoiva tekijä, IL-2, IL-6, IL-8, IL-10 ja typpioksidi (NO) lisäävät edelleen sytokiinitasoja. Tämä johtaa polymorfonukleaaristen leukosyyttien (PMN), makrofagien ja lymfosyyttien jatkuvaan aktivoitumiseen; tulehdukselliset välittäjät rekrytoivat enemmän näistä soluista. Kaikki nämä prosessit luovat destruktiivisen immunologisen dissonanssin tilan.
Sepsistä kuvataan autodestruktiivisena prosessina, joka sallii infektion normaalin patofysiologisen vasteen laajentamisen muutoin normaalien kudosten ja tulosten saamiseksi. MODS-tilassa. Elinten toimintahäiriöt tai elinten vajaatoiminta voivat olla sepsiksen ensimmäinen kliininen merkki, eikä mikään elinjärjestelmä ole immuuni sepsiksen tulehduksellisten liiallisten vaikutusten johdosta. Kuolleisuus lisääntyy elinten vajaatoiminnan lisääntyessä.
Vaikka hallitsematon, kun MODS kehittää järjestelmällisiä todisteita sekä tulehdusta ehkäisevistä että tulehduksia ehkäisevistä ylössäätelyistä, viittaa siihen, että isännän puolustuksen homeostaasin epäonnistuminen on viimeinen reitti sepsiksestä MODS: ään pikemminkin kuin yksinkertainen hypotension aiheuttama loppuelimen vaurio, kuten voi esiintyä verenvuotoshokin yhteydessä. MODS-oireyhtymän selviytyminen vaikeasta sepsiksestä liittyy yleensä tulehdusta ja tulehdusta estävän vasteen yleiseen vähenemiseen.
Äskettäin on ilmaantunut uusi hypoteesi, että vaikeasta sepsiksestä selviytyminen vaatii kehon immuunivasteen, energisten toimintojen ja niihin liittyvän elimen suorituskyvyn yleinen alaspäin säätäminen. Täten MODS voi isännän mukautuvalla reaktiolla ylivoimaiseen tulehdukseen, jolloin tulehdus voi selvitä aiheuttamatta pysyviä loppuelinten haittoja. Kuten jäljempänä keskustellaan, kaikki elimet paljastavat yleistyneen hyporesponsiivisuuden, joka on selvästi poikkeavaa terveydentilassa, mutta voi merkitä selviytymisstrategiaa vaikeassa sepsiksessä.
Elinjärjestelmien toimintahäiriöt
Verenkierron häiriö
Merkittävä häiriö verenkierron autoregulaatiossa on tyypillistä sepsikselle. Vasoaktiiviset välittäjät aiheuttavat vasodilataatiota ja lisäävät mikrovaskulaarista läpäisevyyttä infektiokohdassa. NO: lla on keskeinen rooli septisen sokin vasodilataatiossa. Myös vasopressiinin erityksen heikkenemistä voi esiintyä, mikä saattaa sallia vasodilataation jatkumisen.
Sekä systolissa että systolisessa ja diastolisessa kammion suorituskyvyssä tapahtuu muutoksia. Frank-Starling-mekanismin avulla sydämen teho kasvaa usein verenpaineen ylläpitämiseksi systeemisen vasodilataation läsnä ollessa. Potilaat, joilla on ennestään sydänsairaus, eivät pysty lisäämään sydämen tuotosta asianmukaisesti.
Alueellisesti sepsis häiritsee systeemisen verenkierron normaalia jakautumista elinjärjestelmiin. Tästä syystä ydinelimet eivät välttämättä saa asianmukaista happea, ja tuloksena on alueellinen hypoperfuusio.
Mikroverenkierto on sepsiksen vamman keskeinen kohde-elin, koska verisuonten endoteeli on kiertävät tulehdusvälittäjät vaikuttavat yleisesti. Vaikka on epäselvää, johtavatko mikroverenkierron poikkeavuudet loppuelimen vaurioille vai syyttömille sivullisille, selviä mikrovaskulaarisia toimintahäiriöitä esiintyy. Perfusoitujen kapillaarien lukumäärä vähenee, vaikka vasodilataattorihoitoja käytettäessä tapahtuu täysi mikrovaskulaarinen rekrytointi. Mitokondrioiden toimintahäiriöitä esiintyy myös, ja niihin liittyy usein vähentyneitä mitokondrioiden transmembraanipotentiaaligradientteja, jotka ovat välttämättömiä oksidatiivisen fosforylaation ajamiseksi. Lopputulos on loppuelinten ilmeinen kyvyttömyys uuttaa maksimaalisesti happea.
Jatketaan keskustelua siitä, onko tämä energia-aineenvaihdunnan epäonnistuminen sopeutumismekanismi, joka muistuttaa lepotilaa, vai heijastavatko se primaarista mitokondrioiden patologiaa. Nämä ovat aktiivisen tutkimuksen alueita, mutta eivät tällä hetkellä tarkoita selkeitä kliinisen käytännön ohjeita. Lisääntynyt kapillaarien endoteelin läpäisevyys johtaa laajaan proteiinipitoiseen kudosödeemaan. Septiselle sokille ja SIRS: lle on tunnusomaista palautuva sydänlihaksen masennus, joka voi osoittautua vastustuskykyiseksi katekoliamiinin ja nesteen antamiselle. Kiertävä ”sydänlihaksen lamaava tekijä” – joka edustaa todennäköisesti TNF-a: n, IL-1β: n, muiden sytokiinien ja NO: n synergistisiä vaikutuksia – liittyy patogeneesiin. Tämän akuutin stressi-sydänlihaksen masennuksen kaksi ominaisuutta ovat heikentynyt adrenerginen reaktiivisuus ja diastolinen toimintahäiriö, joka johtaa suhteellinen katekoliamiiniresistenssi ja pienet kuin laajentuneet sydämet. Makrovaskulaarinen sydänlihasiskemia ja hypoperfuusio ovat epätodennäköisiä tekijöitä.
Vaikeassa sepsiksessä ja septisessä sokissa mikroverenkierron toimintahäiriöt ja mitokondrioiden masennus aiheuttavat alueellista kudosvaivaa, ja alueellinen dysoksia jatkuu tämän vuoksi. Tätä tilaa kutsutaan mikroverenkierto- ja mitokondrioiden distress-oireyhtymäksi (MMDS). Sepsiksen aiheuttama tulehduksellinen autoregulaation toimintahäiriö jatkuu, eikä hapen tarve täsmää toimituksen kanssa, mikä johtaa MODS: ään.
Suonensisäisen nestemäärän uudelleenjakautuminen johtuu pienentyneestä valtimoiden verisuonten sävystä, vähentyneestä laskimoiden paluusta laskimoiden di sydänlihakseen lamaavien aineiden vapautuminen aiheuttaa hypotensiota.
Keuhkojen toimintahäiriö
Keuhkoverisuonten endoteelivaurio johtaa häiriöihin kapillaariverenkierto ja parantunut mikrovaskulaarinen läpäisevyys, mikä johtaa interstitiaaliseen ja alveolaariseen turvotukseen. Neutrofiilien tarttuminen keuhkojen mikroverenkiertoon aloittaa ja vahvistaa alveolaaristen kapillaarikalvojen vaurioita. Akuutti keuhkovaurio ja akuutti hengitysvaikeusoireyhtymä (ARDS) ovat usein näiden vaikutusten ilmenemismuotoja. Sepsis ja keuhkokuume ovat todellakin yleisimmät ARDS-syyt.
Ruoansulatuskanavan toimintahäiriöt
Ruoansulatuskanava (GI) voi auttaa levittämään sepsiksen vahinkoa. Bakteerien liikakasvu ylemmässä ruoansulatuskanavassa voi imeytyä keuhkoihin aiheuttaen sairaalahoitoa tai aspiraatiokeuhkokuumetta. Suolen normaali estotoiminto voi vaikuttaa, jolloin bakteerit, endotoksiinit ja normaalit ruoansulatuskanavan proteaasit siirtyvät systeemiseen verenkiertoon ja pidentävät septistä vastetta.
Septinen sokki voi aiheuttaa paralyyttinen ileus, joka voi johtaa viivästymiseen enteraalisessa ruokinnassa. Ylimääräisen NO-tuotannon uskotaan olevan sepsiksen aiheuttaman ileuksen aiheuttaja. Ravitsemuksellisen saannin optimaalinen taso häiriintyy korkeiden proteiini- ja kalorivaatimusten vuoksi. Huumeet ja lihasrelaksantit voivat edelleen heikentää ruoansulatuskanavan motiliteettia.
Maksan toimintahäiriö
Maksan roolin seurauksena isännän puolustuksessa maksan toimintahäiriön aiheuttamat epänormaalit synteettiset toiminnot voivat vaikuttaa sekä sepsiksen alkamiseen että etenemiseen. Maksan retikuloendoteliaalijärjestelmä toimii ensimmäisenä puolustuslinjana puhdistettaessa bakteereja ja niiden tuotteita; maksan toimintahäiriö johtaa näiden tuotteiden leviämiseen systeemiseen verenkiertoon.
Maksan vajaatoiminta (”järkyttynyt maksa”) voi ilmetä maksaentsyymien ja bilirubiinin nousuna, hyytymisvirheinä ja epäonnistuminen toksiinien, kuten ammoniakin, erittämisessä, mikä johtaa enkefalopatian pahenemiseen.
Munuaisten toimintahäiriö
Akuutti munuaisvaurio (AKI) usein seuraa sepsistä. AKI: n eri etiologioita on raportoitu, ja syyn uskotaan tyypillisesti olevan monitekijäinen. AKI: n mekanismi on monimutkainen, mutta todennäköisesti siihen liittyy tehokkaan suonensisäisen tilavuuden lasku, joka johtuu systeemisestä hypotensiosta, suorasta munuaisten vasokonstriktiosta, sytokiinien vapautumisesta, ja neutrofiilien aktivaatio endotoksiineilla ja muilla peptideillä, jotka edistävät munuaisvaurioita.Vielä useimmat eläintutkimukset osoittavat, että munuaisten verenkierto lisääntyy, ei laske sepsiksessä, vaikka siihen liittyy heikentynyt tubulaarinen toiminta ja merkittävän histologisen todistuksen puute tu bulaarivamma.
Keskushermoston toimintahäiriö
Keskushermoston (CNS) osallistuminen sepsisiin tuottaa enkefalopatiaa ja perifeeristä neuropatia. Patogeneesi on määritelty huonosti, mutta se liittyy todennäköisesti systeemiseen hypotensioon, joka voi johtaa aivojen hypoperfuusioon.
Koagulopatia
Subkliininen koagulopatia, josta viittaa lievä trombiiniajan (TT) tai aktivoidun osittaisen tromboplastiiniajan (aPTT) nousu tai kohtalaisen lyheneminen verihiutaleiden määrä on erittäin yleinen; Kuitenkin myös ilmeinen disseminoitunut suonensisäinen hyytyminen (DIC) voi kehittyä. Proteaasiaktivoidut reseptorit (PAR), erityisesti PAR 1, muodostavat molekyylisen yhteyden hyytymisen ja tulehduksen välille; PAR1: llä on sytoprotektiivisia vaikutuksia, kun sitä stimuloi aktivoitu proteiini C tai pieniannoksinen trombiini, mutta sillä on häiritseviä vaikutuksia endoteelisolujen estofunktioon, kun se aktivoidaan suuriannoksisella trombiinilla.
Elinten toimintahäiriöiden ja loukkaantumismekanismit
Soluvamman ja siitä johtuvan sepsiksen elinten toimintahäiriön tarkkoja mekanismeja ei tunneta täysin. MODS liittyy laajalle levinneisiin endoteelisolujen ja parenkymaalisolujen vaurioihin, joista osa voidaan selittää seuraavilla 4 ehdotetulla mekanismilla.
Hypoksinen hypoksia
Septinen verenkierron vaurio häiritsee kudosten hapettumista, muuttaa kudosten hapensiirron metabolista säätelyä ja edistää elinten toimintahäiriöitä. Mikrovaskulaariset ja endoteelipoikkeavuudet vaikuttavat sepsiksen septiseen mikroverenkiertoon. Reaktiiviset happilajit, lyyttiset entsyymit ja vasoaktiiviset aineet (esim. NO ja endoteelin kasvutekijät) johtavat mikroverenkiertoon johtaviin vaurioihin, joihin liittyy punasolujen kyvyttömyys navigoida septisessä mikroverenkierrossa.
Suora sytotoksisuus
Endotoksiini, TNF-α ja NO voivat vahingoittaa mitokondrioiden elektronikuljetuksia, mikä johtaa häiriintyneeseen energia-aineenvaihduntaan. Tätä kutsutaan sytopaattiseksi tai histotoksiseksi hapettomuudeksi, kyvyttömäksi käyttää happea silloinkin, kun sitä on läsnä.
Apoptoosi
Apoptoosi ( ohjelmoitu solukuolema) on pääasiallinen mekanismi, jolla toimintahäiriösolut eliminoidaan normaalisti. Proinflammatoriset sytokiinit voivat viivästyttää apoptoosia aktivoiduissa makrofageissa ja neutrofiileissä, mutta muut kudokset (esim. Suolen epiteeli) voivat käydä kiihtyneessä apoptoosissa. Siksi apoptoosin häiriöllä on kriittinen rooli sepsiksen kudosvaurioissa.
Immunosuppressio
Tulehduksellisten ja tulehdusta ehkäisevät välittäjät voivat johtaa niiden väliseen epätasapainoon. Tulehdusreaktio tai immuunipuutos voi olla hallitseva tai molemmat voivat olla läsnä.
Isäntävaste ja muut tulokseen vaikuttavat tekijät
Kliiniset ominaisuudet, jotka liittyvät vakavuuteen sepsiksen piiriin kuuluvat isännän vastaus infektioon, infektiokohta ja -tyyppi, mikrobilääkehoidon ajoitus ja tyyppi, rikkoneen organismi, sokin kehittyminen, perussairaus, potilaan pitkäaikainen terveydentila ja epäonnistuneiden määrä elimet. Sepsisiin ja septiseen sokkiin johtavat tekijät eivät välttämättä ole välttämättömiä lopullisen tuloksen määrittämisessä.
Isäntävasteelle sepsikselle on tunnusomaista sekä tulehdusta edeltävät että tulehdusta estävät immunosuppressiiviset vasteet. Näiden reaktioiden suunnan, laajuuden ja keston määräävät sekä isäntätekijät (esim. Geneettiset ominaisuudet, ikä, samanaikaiset sairaudet, lääkkeet) että patogeenitekijät (esim. Mikrobikuormitus, virulenssi).
lektiinireseptorit), endosomissa (TLR) tai sytoplasmassa (retinoiinihapon indusoimat geenin 1 kaltaiset reseptorit ja nukleotidia sitovat oligomerointidomeenin kaltaiset reseptorit).
Liioitellun tulehduksen seurauksena on sivukudosvaurio ja nekroottinen solukuolema, joka johtaa vaurioihin liittyvien molekyylimallien, ns. vaaramolekyylien vapautumiseen, jotka jatkavat ainakin tulehdusta osittain toimimalla samoilla patogeenien laukaisemilla kuvion tunnistamisreseptoreilla.