USPharm。 2018; 43(7):22-26。
要約:スタチンは、心血管イベントの一次および二次予防に広く使用されている薬剤のクラスです。一般的に利用可能な6つのスタチンを使用して、適切な薬剤の選択は、投薬の考慮事項、薬物相互作用、および有害事象を含む薬物固有の要因に基づいて決定することができます。個別の患者ケア計画は、重要な臨床研究からのデータ、ガイドラインの違い、およびスタチンの使用に関連する2つの主要な有害事象に関する現在の管理上の推奨事項に基づいて作成できます。
脂質異常症治療の基礎には、 3-ヒドロキシ-3-メチルグルタリル-コエンザイムAレダクターゼ阻害剤、より一般的にはスタチンとして知られています。市場に出回っているさまざまなジェネリック医薬品とその使用を裏付ける強力な証拠により、スタチンは世界で最も広く処方されている医薬品の一部です1。しかし、これらの薬剤を頻繁に使用することで、安全性が継続的に精査され、その使用について継続的な議論が行われています。治療における役割。ジェネリックスタチンに焦点を当てたこの記事では、治療におけるスタチンの役割についての議論に焦点を当て、適切な使用について議論し、2つの主要な有害事象を取り巻く証拠を探ります。
市場に出回っている7つの異なるスタチンのうち、6つ2-7 3つの利用可能なブランド製剤は、ピタバスタチン(Livalo)、シンバスタチン経口懸濁液(FloLipid)、およびロバスタチン徐放性(Altoprev)です。8-10治療におけるブランド薬剤の役割は限られています。ジェネリックオプションが広く利用可能です。
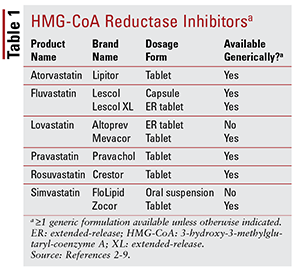
アトルバスタチンとシンバスタチンはいくつかの組み合わせ製品。これらには、高血圧の適応となるカルシウムチャネル遮断薬(CCB)であるアトルバスタチンとアムロジピンの組み合わせ、および高コレステロール血症でも適応となる腸のコレステロール吸収阻害剤であるシンバスタチンとエゼチミベの組み合わせが含まれます11,12。共製剤化されたスタチンおよびナイアシン製品(ナイアシン/ロバスタチンおよびナイアシン/シンバスタチン)は、スタチン治療を受けた患者にナイアシンを追加すると、スタチン単独で見られるよりも心血管(CV)の結果がさらに低下するという証拠がないため、2016年に市場から削除されました。13
治療の推奨事項
スタチンは、HDLコレステロール(HDL-C)のレベルを上げながら、LDLコレステロール(LDL-C)とトリグリセリドのレベルを下げるのに効果的であることが繰り返し証明されています14。一次予防と二次予防の両方における主要なCVイベント(CVE)などの患者志向の結果。15-19
いくつかの激しく議論されている治療ガイドラインは、hyの治療におけるスタチンの役割について論じています。過脂血症。これらには、2013 American College of Cardiology / American Heart Association(ACC / AHA)ガイドラインと2017 American Academy of Clinical Endocrinology(AACE)ガイドラインが含まれます14,20。どちらのガイドラインも、禁煙を含むライフスタイルの変更を実施した後、運動療法、および心臓の健康的な食事療法の後、スタチンはCV疾患(CVD)の一次および二次予防の両方の第一選択療法です14,20。ただし、ガイドラインは、どのスタチンがどのスタチンに適切であるかを決定する方法が異なります。
2013年のACC / AHAガイドラインでは、スタチン療法の対象となる4つの治療グループが導入されました。
1。以前のイベント(すなわち、急性冠症候群、心筋梗塞の病歴、安定狭心症または不安定狭心症、冠状動脈または他の動脈血行再建術、脳卒中、一過性脳虚血発作、または推定される末梢動脈疾患)の患者を含む、以前のアテローム性動脈硬化症CVD(ASCVD)の患者アテローム性動脈硬化症の起源)。
2。 ASCVDイベントの病歴がなく、LDL-Cレベルが190mg / dL以上の患者。年齢はこの基準から除外する根拠ではありません。
3。糖尿病を患っているがASCVDイベントの病歴がなく、LDL-Cレベルが70〜189mg / dLの40〜75歳の患者。
4。 ASCVDイベントの病歴がなく、LDL-Cレベルが70〜189 mg / dLである糖尿病のない40〜75歳の患者。20
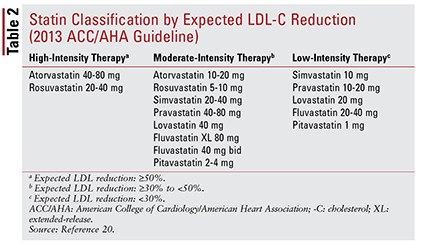
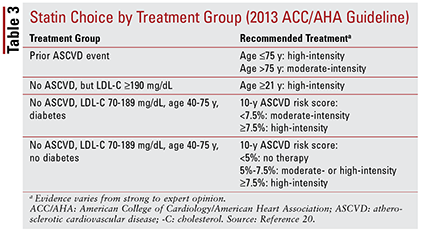
ACC / AHAガイドラインでは、スタチンをグループ化するというアイデアも導入されました。強度別(すなわち、期待されるLDL-C低下能力)(表2)。20治療群(上記で定義)に基づいて、ガイドラインは特定の臨床状況に特定のスタチン強度を推奨しています(表3)。20いくつかの治療群ASCVDリスク推定器を使用してASCVDリスクスコアを計算する必要があります。このオンラインツールは、患者の年齢、性別、人種、収縮期血圧、総コレステロール、HDL-C、および高血圧治療、糖尿病、または喫煙に重要な過去の病歴を考慮に入れます21。すべての入力が入力されると、患者の10 -ASCVDイベントを経験する年のリスクが計算されます。
これらの推奨事項は、特定のサブグループの患者には自動的には適用されません。たとえば、高齢者でのスタチンの使用には注意が必要です。高齢患者の二次予防のためのスタチンの使用は大きな利益をもたらしますが、一次予防のためのその使用は不明です。22-24さらに、心不全の患者は心不全のない患者と同じスタチン療法の利益を経験することが見出されていません。これらの所見について、推奨される治療法には、高強度スタチンの開始を75歳未満の患者に限定し、心不全患者のスタチンを回避することが含まれます20。全体として、これらのグループでスタチンを使用する決定は明確ではなく、治療の潜在的なリスクと利点についてプロバイダーと患者の間で進行中の会話。20
治療グループの分類に従って治療を開始するという2013年のACC / AHA勧告とは異なり、2017年のAACEガイドラインでは個々の患者が検査結果に基づいて治療されます14。このガイドラインによると、患者のリスクは、さまざまな主要な、追加の、 nd非伝統的な危険因子。次に、個人は5つのリスクグループの1つに分類され、それぞれに対応するLDL-Cおよび非HDL-Cの目標があります(表4)。現在のレベルと個別の目標に基づいて、スタチン単独または他の薬剤との組み合わせは、予想されるLDL-Cまたは非HDL-C低下能力に基づいて開始する必要があります。14

進行中のスタチン療法に2番目の薬剤を追加することを含む併用療法は、やや物議を醸すトピックのままです。以前の試験とガイドラインでは、バックグラウンドスタチン療法への他の薬剤の追加が最小限に抑えられていましたが、最近の研究とコンセンサスステートメント(ACC / AHAからのものを含む)は、エゼチミブ、エボロクマブ、またはアリロクマブの使用をサポートしています。これらの最後の2つはプロタンパク質転換酵素サブチリシンです。 /ケキシン9型阻害剤、二次予防の追加療法として。20,26-31とはいえ、スタチンは一次予防と二次予防の両方で普遍的な一次治療のままです。他の特定の薬剤の決定的な役割は不明なままです。
スタチンの選択
スタチン療法の選択は、それがACC / AHAのスタチン治療法であるかどうかにかかわらず、臨床医が好む治療アプローチから始まります。グループまたはLDL-Cまたは非HDL-C目標のAACEメソッド。そこから、個々の患者に最適なオプションを決定するために、各スタチンの特性を考慮に入れる必要があります。すべてのスタチンが等しいわけではなく、投薬の考慮事項、薬物相互作用、有害事象(AE)など、患者の選択に影響を与える可能性のあるいくつかの重要な違いが存在します。
投薬
ただし、ほとんどのスタチンは食事に関係なく服用する場合、生物学的利用能が高まるため、即時放出(IR)ロバスタチンは夕食と一緒に服用する必要があります4。 .8さらに、すべてのスタチンは1日1回投与できますが、IRフルバスタチンとロバスタチンは1日2回の投与が必要な場合があります3,4。最後に、アトルバスタチン、プラバスタチン、ロスバスタチンはいつでも投与できますが、フルバスタチン、ロバスタチン、シンバスタチンは夕方に服用する必要があります。3,4,7特に、シンバスタチンは、朝とは対照的に夕方に服用した場合に有意に異なる効果があることが示されました。32
薬物相互作用
スタチンはそれぞれ異なりますそれぞれが代謝される特定の経路のため、薬物-薬物および薬物-食品の相互作用に関する懸念(表5)。それぞれを詳細に議論するには、薬物相互作用が多すぎます。したがって、以下では選択したいくつかのみを説明します。
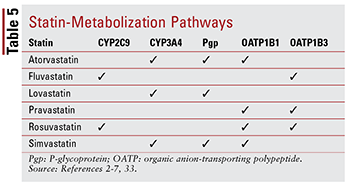
フィブラート:組み合わせはフィブラートとスタチンの併用が臨床転帰を有意義に変化させることは示されていませんが、患者は依然として、重度に制御されていない高トリグリセリド血症を標的とするために、スタチンと一緒にゲムフィブロジル、フェノフィブラート、またはフェノフィブラートを処方される可能性があります14,20,26,33。併用療法は、筋肉関連の毒性に関連しているため、併用療法は、いずれかの療法単独と比較して、このリスクを大幅に増加させます33。この相加毒性は、他のフィブラートよりもゲムフィブロジルでより頻繁に見られます33。したがって、ゲムフィブロジルの使用は、シンバスタチンと禁じられており、他のスタチン7,20スタチンとフィブラートを併用する場合は、フェノフィブラートまたはフェノフィブラートが好ましい20,33。ただし、ゲムフィブロジルを使用する必要がある場合は、フルバスタチン、または注意深く監視しながら、アトルバスタチンまたはロスバスタチン(1日最大10 mg )—最適なエージェントです。33
アミオダロン:脳室線維化の適応となるこの抗不整脈薬は、P-糖タンパク質(Pgp)およびCYP450酵素系、特にCYP3A4、および程度は低いがCYP2C9.33,34の既知の阻害剤です。その結果、アミオダロンと併用した場合、ロバスタチン(1日最大40 mg)とシンバスタチン(1日最大20 mg)の最大推奨投与量が存在します。4,7,33アトルバスタチンはCYP3A4を介して代謝されますが、投与量の調整は必要ありません(他のスタチンと同様)。アトルバスタチンとアミオダロンを併用した場合、データは深刻なAEを示唆していないためです。2,33
CCB:ジヒドロピリジン(アムロジピン)と非ジヒドロピリジンCCB(ジルチアゼム、ベラパミル)の両方がスタチンと有意義な薬物相互作用を示すことが示されています。アミオダロンと同様に、アムロジピン、ジルチアゼム、およびベラパミルはCYP3A4.33,35-37を阻害します。アムロジピンもPgpに対して阻害効果があります。33,35文献で報告されているAEに基づくと、ロバスタチンの最大1日投与量は20mgが推奨されます。アムロジピン、ジルチアゼム、またはベラパミルと併用4,33アムロジピンと併用する場合は、シンバスタチンが20 mgを超えないようにすることも推奨されますが、ジルチアゼムとベラパミルと併用する場合は、10mgの低用量を投与する必要があります7,33。アトルバスタチンには推奨事項がありますが、非ジヒドロピリジンCCBのいずれかと一緒に投与する場合は注意が必要です。2,33
薬物の有害反応
スタチンは一般的に忍容性が良好です。しかし、中止率は依然として高い38。スタチン療法の中止および有害な薬物反応の発生後のスタチン療法の再開の失敗は、CVEの増加率と関連している39。2つの主要なスタチン関連AEに照らしたスタチンの安全性に関する患者の懸念—筋毒性と新たに発症した糖尿病—スタチンの中止につながる可能性があります。
筋毒性:スタチンは、筋痛(クレアチンキナーゼの上昇を伴わない筋肉痛)、ミオパチー(筋肉の総称)など、筋肉関連の毒性と長い間関連してきました。疾患)、および筋炎(筋肉の炎症)、これらの最後の2つは有意なCKの上昇を伴います40,41。すべてのスタチンは、横紋筋肉溶解のまれではあるが深刻な副作用に対する警告を共有しています。2-7しかし、多くの場合、スタチンに起因する筋毒性はノセボ効果による;つまり、人は薬が害を引き起こし、その後薬が予想される害を引き起こすと信じています42,43。したがって、最良の結果を確実にするために、薬剤師はこの一般的に報告される副作用とその適切な管理に精通している必要があります。
筋肉症状のすべての報告がノセボ効果によるものであると仮定するのは誤りです。患者の過去の病歴(PMH)の適切な検査、痛みの説明、およびスタチン療法との関連が不可欠です44。まず、PMHのCK上昇およびその他の筋肉の痛みまたは衰弱の潜在的な原因を調べることにより、臨床医は代替治療を行うことができます。スタチン代謝を変える可能性のある根本的な病態生理学または正しい要因。一般的な原因には、老齢、薬物相互作用、腎機能または肝機能の障害、身体活動の増加、ビタミンD欠乏症などがあります。20,41
次に、臨床医は患者の症状を一般的に見られるスタチン誘発症状と比較する必要があります。 。スタチン誘発性の筋肉毒性は、通常、痛み、圧痛、けいれん、脱力感として現れ、通常は脚の筋肉に見られます20,41。これらの症状は通常、運動後に悪化し、問題のある薬剤を中止しないと解消されません。41
最後のステップは、症状とスタチン使用の間に因果関係が存在するかどうかを判断することです。軽度から中等度の症状の原因としてスタチンが疑われる場合は、一時的な離脱が推奨されます。約2週間経っても症状が改善しない場合は、スタチンが原因ではない可能性が高いため、元の用量で再開する必要があります。ただし、症状が解消した場合は、同じまたはより低い用量で同じスタチンの再試行を行う必要があります。その後、同様の症状が見られた場合は、スタチンが原因と推定され、中止されるべきです。症状が解消したら、低用量の代替スタチンを開始し、最大耐量まで滴定する必要があります20,41。ノセボ効果によりさらに知覚される反応が生じる可能性があるため、患者の受け入れとこのプロセスの理解が重要です。
これらの症状を管理および予防するための戦略は他にもいくつかあります。第一に、症状の可能性が高いため、臨床医は最も親油性のスタチン(ロバスタチンとシンバスタチン)を避け、より親水性のスタチン(フルバスタチン、プラバスタチン、ロスバスタチン)を優先することを選択する可能性があります44。シンバスタチン80mgを新品として開始しないでくださいスタチン関連の筋肉症状の頻度が異常に高いため、どの患者でも治療が可能です。7,45コエンザイムQ10などの代替治療は一貫した効果を示していませんが、心理的に誘発された症状を経験している患者では検討される可能性があります。41,44,46最後に、スタチン薬を1日1回ではなく、週に数回投与することを含む、延長間隔投与を検討することができます。このアプローチは、以前にスタチン不耐性のある患者のアドヒアランスと脂質プロファイルを改善します。47-49
新規発症糖尿病:スタチン使用に関連する重要なAEは新規発症糖尿病です。スタチンは糖尿病発症のリスクを高めることが示されていますが、いくつかの重要な警告が存在します50。まず、これはクラス効果のようなものと見なすことができますが、特定の各スタチンの真のリスクはまだ不明です51,52。 -これまでの分析では、プラバスタチンが最もリスクが低く、シンバスタチンとアトルバスタチンが中程度のリスクであり、ロスバスタチンが新たに発症する糖尿病を引き起こすリスクが最も高かった53。しかし、これらの所見はいずれも統計的に有意ではなかった53。スタチンの投与量が増加するにつれてリスクが増加します54
スタチン誘発性糖尿病は、すでに糖尿病を発症するリスクが高い人に最も多く見られます50,54。これには、高齢の患者や前糖尿病または代謝性の患者が含まれますシンドローム50,55一貫した発見の1つは、スタチンによって引き起こされた糖尿病の新しい症例ごとに、リスクの高い患者でいくつかのCVEを予防できるということです50。したがって、薬剤師は糖尿病を発症するリスクがCVリスク低減の利点によって相殺される以上のCV合併症のリスクが中程度または高いスタチン使用者。ただし、CVEのリスクが非常に低い患者では、リスクとベネフィットの比率は不明です。50
結論
スタチン療法にはリスクがないわけではありませんが、CVの結果を減らすことでのベネフィットはそれをCVE予防の基礎にしました。利用可能なガイドラインは大きく異なりますが、1つの定数は、スタチンがほぼすべての患者の一次および二次予防のための第一選択療法であるべきであるということです。スタチンの広範なジェネリック医薬品の入手可能性により、これらの薬剤はますます入手しやすくなっています。すべてのスタチンが同じであるとは限らないことを理解することにより、薬剤師は各患者に可能な限り最良の結果を保証するのに役立ちます。
1。ヘルスケア情報学のためのIMS研究所。米国での医薬品の使用と支出:2015年のレビューと2020年までの見通し。https://morningconsult.com/wp-content/uploads/2016/04/IMS-Institute-US-Drug-Spending-2015.pdf。 2018年3月18日にアクセス。
2。リピトール(アトルバスタチン)の添付文書。ニューヨーク州ニューヨーク:ファイザー社; 2017年6月。
3。 Lescol / Lescol XL(フルバスタチン)の添付文書。ニュージャージー州イーストハノーバー:Novartis Pharmaceuticals Corp; 2017年8月。
4。 Mevacor(ロバスタチン)添付文書。ニュージャージー州ホワイトハウスステーション:Merck & Co、Inc; 2014年2月。
5。プラバコール(プラバスタチン)添付文書。ニュージャージー州プリンストン:ブリストルマイヤーズスクイブカンパニー; 2016年7月。
6。クレストール(ロスバスタチン)の添付文書。デラウェア州ウィルミントン:AstraZeneca Pharmaceuticals LP; 2017年8月。
7。 Zocor(シンバスタチン)の添付文書。ニュージャージー州ホワイトハウスステーション:Merck & Co、Inc; 2015年2月。
8。アルトプレフ(ロバスタチン)添付文書。スイス、ツーク:Covis Pharma; 2017年4月。
9。 FloLipid(シンバスタチン)の添付文書。フロリダ州ブルックスビル:Salerno Pharmaceuticals LP; 2017年7月。
10。リバロ(ピタバスタチン)の添付文書。アラバマ州モンゴメリー:Kowa Pharmaceuticals America、Inc; 2016年11月。
11。 Caduet(アムロジピン/アトルバスタチン)の添付文書。ニューヨーク州ニューヨーク:ファイザー社; 2017年10月。
12。 Vytorin(ezetimibe / simvastatin)の添付文書。ニュージャージー州ホワイトハウスステーション:Merck & Co、Inc; 2018年2月。
13。 AbbVie Inc。; AdvicorおよびSimcorの新薬承認申請の承認の撤回。 www.federalregister.gov/documents/2016/04/18/2016-08894/abbvie-inc-withdrawal-of-approval-of-new-drug-applications-for-advicor-and-simcor。 2018年3月18日にアクセス。
14。ジェリンジャーPS、ハンデルスマンY、ローゼンブリットPD、他。脂質異常症の管理と心血管疾患の予防のための米国臨床内分泌学者協会と米国内分泌学大学のガイドライン。内分泌学。 2017; 23(suppl 2):1-87。
15。 LaRosa JC、Grundy SM、WatersDDなど。安定した冠状動脈疾患の患者におけるアトルバスタチンによる集中的な脂質低下。 N Engl JMed。 2005; 352:1425-1435。
16。 Ridker PM、Danielson E、Fonseca FA、他。 C反応性タンパク質が上昇している男性と女性の血管イベントを予防するロスバスタチン。 N Engl JMed。 2008; 359:2195-2207。
17。ミハイロバB、エンバーソンJ、ブラックウェルL、他血管疾患のリスクが低い人々におけるスタチン療法によるLDLコレステロール低下の効果:27件のランダム化試験からの個々のデータのメタアナリシス。ランセット。 2012; 380:581-590。
18。 Baigent C、Landray MJ、Reith C、他慢性腎臓病患者におけるシンバスタチンとエゼチミブによるLDLコレステロール低下の効果(心臓および腎保護の研究):無作為化プラセボ対照試験。ランセット。 2011; 377:2181-2192。
19。キャノンCP、ブラウンヴァルトE、マッケイブCH、他急性冠症候群後のスタチンによる集中的対中等度の脂質低下。 N Engl JMed。 2004; 350:1495-1504。
20。 Stone NJ、Robinson JG、Lichtenstein AH、他成人のアテローム性動脈硬化性心血管リスクを低減するための血中コレステロールの治療に関する2013年ACC / AHAガイドライン:米国心臓病学会/米国心臓協会の診療ガイドラインに関するタスクフォースの報告。サーキュレーション。 2014; 129(25 suppl 2):S1-S45。
21。アメリカ心臓病学会。 ASCVDリスクエスティメータプラス。 http://tools.acc.org/ASCVD-Risk-Estimator。 2018年3月18日にアクセス。
22。ウェンガーNK、ルイスSJ、ヘリントンDM、他。安定した冠状動脈性心臓病の65歳以上の患者に高用量または低用量のアトルバスタチンを使用した結果。アンインターンメッド。 2007; 147:1-9。
23。 Shepherd J、Blauw GJ、Murphy MB、他血管疾患のリスクがある高齢者におけるプラバスタチン(PROSPER):ランダム化比較試験。ランセット。 2002; 360:1623-1630。
24。 Teng M、Lin L、Zhao YJ、他高齢患者の心血管疾患の一次予防のためのスタチン:系統的レビューとメタアナリシス。ドラッグエイジング。 2015; 32:649-661。
25。 Kjekshus J、Apetrei E、Barrios V、他収縮期心不全の高齢患者におけるロスバスタチン。 N Engl JMed。 2007; 357:2248-2261。
26。 Ginsberg HN、Elam MB、LovatoLCなど。 2型糖尿病における脂質併用療法の効果。 N Engl JMed。 2010; 362:1563-1574。
27。 Kastelein JJ、Akdim F、StroesESなど。家族性高コレステロール血症におけるエゼチミブの有無にかかわらずシンバスタチン。 N Engl JMed。 2008; 358:1431-1443。
28。キャノンCP、ブレイジングMA、ジュリアーノRP、他エゼチミブは、急性冠症候群後のスタチン療法に追加されました。 N Engl JMed。 2015; 372:2387-2397。
29。 Sabatine MS、Giugliano RP、KeechACなど。心血管疾患患者におけるエボロクマブと臨床転帰。 N Engl JMed。 2017; 376:1713-1722。
30。ロイドジョーンズDM、モリスPB、バランタインCMなど。アテローム性動脈硬化性心血管疾患リスクの管理におけるLDLコレステロール低下のための非スタチン療法の役割に関する2016ACCエキスパートコンセンサス決定パスウェイの2017年の焦点を絞った更新:エキスパートコンセンサス決定パスウェイに関する米国心臓病学会タスクフォースの報告。 J Am CollCardiol。 2017; 70:1785-1822。
31。 ODYSSEYの結果:結果は、PCSK9阻害剤の使用がACS患者のCVイベント、LDL-Cを減少させることを示唆しています。アメリカ心臓病学会。 www.acc.org/latest-in-cardiology/articles/2018/03/05/15/53/sat-9am-odyssey-outcomes-cv-outcomes-with-alirocumab-after-acs-acc-2018。 2018年6月20日にアクセス。
32。ウォレスA、チンD、ルービンG.夕方と比較して朝にシンバスタチンを服用:ランダム化比較試験。 BMJ。 2003; 327:788。
33。 Wiggins BS、Saseen JJ、Page RL、他。心血管疾患の患者に使用されるスタチンおよび選択された薬剤との臨床的に重要な薬物間相互作用の管理に関する推奨事項:米国心臓協会からの科学的声明。サーキュレーション。 2016; 134:e468-e495。
34。パセロン(アミオダロン)の添付文書。ミネソタ州メープルグローブ:Upsher-Smith Laboratories LLC; 2017年7月。
35。 Norvasc(アムロジピン)の添付文書。ニューヨーク州ニューヨーク:ファイザー社; 2017年10月。
36。 Cardizem(ジルチアゼム)の添付文書。ニュージャージー州ブリッジウォーター:Valeant Pharmaceuticals; 2016年11月。
37。カラン(ベラパミル)の添付文書。ニューヨーク州ニューヨーク:ファイザー社; 2017年9月。
38。 Riaz H、Khan AR、Khan MS、他スタチン不耐性の有病率に関するプラセボ対照ランダム化比較試験のメタアナリシス。 Jカルディオールです。 2017; 120:774-781。
39。 Zhang H、Plutzky J、Shubina M、Turchin A.副作用と患者の転帰後の継続的なスタチン処方:コホート研究。アンインターンメッド。 2017; 167:221-227。
40。 Tomaszewski M、Stepien KM、Tomaszewska J、Czuczwar SJスタチン誘発性ミオパチー。 Pharmacol Rep.2011; 63:859-866。
41。 Stroes ES、Thompson PD、Corsini A、他。スタチン関連の筋肉症状:スタチン療法への影響—評価、病因および管理に関する欧州アテローム性動脈硬化症学会コンセンサスパネル声明。 Eur Heart J. 2015; 36:1012-1022。
42。グプタA、トンプソンD、ホワイトハウスA、他アングロスカンジナビア心臓転帰試験-脂質低下薬(ASCOT-LLA)における非盲検であるが盲検ではないスタチン療法に関連する有害事象:ランダム化二重盲検プラセボ対照試験とその非ランダム化非盲検延長段階。ランセット。 2017; 389:2473-2481。
43。 Pedro-Botet J、Rubiés-PratJ。スタチン関連の筋肉症状:ノセボ効果に注意してください。ランセット。 2017; 389:2445-2446。
44。 Laufs U、Filipiak KJ、Gouni-Berthold I、他スタチン関連筋肉症状(SAMS)の管理における実際的な側面。 AtherosclerSuppl。 2017; 26:45-55。
45。 FDA医薬品安全性コミュニケーション:筋肉損傷のリスクを低減するためのZocor(シンバスタチン)の新しい制限、禁忌、および用量制限。 www.fda.gov/Drugs/DrugSafety/ucm256581.htm。 2018年3月18日にアクセス。
46。Banach M、Serban C、Sahebkar A、他スタチン誘発性ミオパチーに対するコエンザイムQ10の効果:ランダム化比較試験のメタアナリシス。メイヨークリニックProc。 2015; 90:24-34。
47。 Goldberg AS、DeGorter MK、Ban MR、他ロスバスタチンの非毎日投与による有効性と血漿中薬物濃度。 Jカルディオールできます。 2013; 29:915-919。
48。 Matalka MS、Ravnan MC、DeedwaniaPC。アトルバスタチンの交互の1日量は高脂血症の患者を治療するのに効果的ですか?アトルバスタチン研究(ADDAS)の隔日投与と毎日投与。 Am Heart J. 2002; 144:674-677。
49。 Copher HR、Stewart RD高コレステロール血症患者におけるシンバスタチンの毎日の投与と隔日投与。薬物療法。 2002; 22:1110-1116。
50。 Rochlani Y、Kattoor AJ、Pothineni NV、他一次予防とスタチン誘発性糖尿病予防のバランスをとる。 Jカルディオールです。 2017; 120:1122-1128。
51。コラオG、イブラヒムB、ニコトラF、他スタチンと糖尿病のリスク:大規模な人口ベースのコホート研究からの証拠。糖尿病治療。 2014; 37:2225-2232。
52。 Lim S、Oh PC、Sakuma I、KohKK。心血管代謝の利点とスタチンのリスクのバランスをとる方法。アテローム性動脈硬化症。 2014; 235:644-648。
53。 Navarese EP、Buffon A、Andreotti F、他新たに発症した2型糖尿病に対するスタチンのさまざまな種類と用量の影響のメタアナリシス。 Jカルディオールです。 2013; 111:1123-1130。
54。 Crandall JP、Mather K、Rajpathak SN、他スタチンの使用と糖尿病を発症するリスク:糖尿病予防プログラムの結果。 BMJオープン糖尿病レスケア。 2017; 5:e000438。
55。ガンダOP。スタチン誘発性糖尿病:発生率、メカニズム、および影響。 F1000Res。 2016; 5。