이 과정은 2016 년 3 월호에 게시되었으며 2019 년 3 월 31 일에 만료됩니다. 저자는 공개 할 상업적 이해 상충이 없습니다. 이 2 학점 자습 활동은 전자적으로 중재됩니다.
목표
이 과정을 읽은 후 참가자는 다음을 수행 할 수 있어야합니다.
- 치은 비대를 유발할 수있는 약물입니다.
- 치은 비대의 임상 적 특징을 식별합니다.
- 약물로 인한 치은 비대의 원인과 위험 요소를 설명합니다.
- 이 상태를 치료할 수있는 옵션을 나열하십시오.
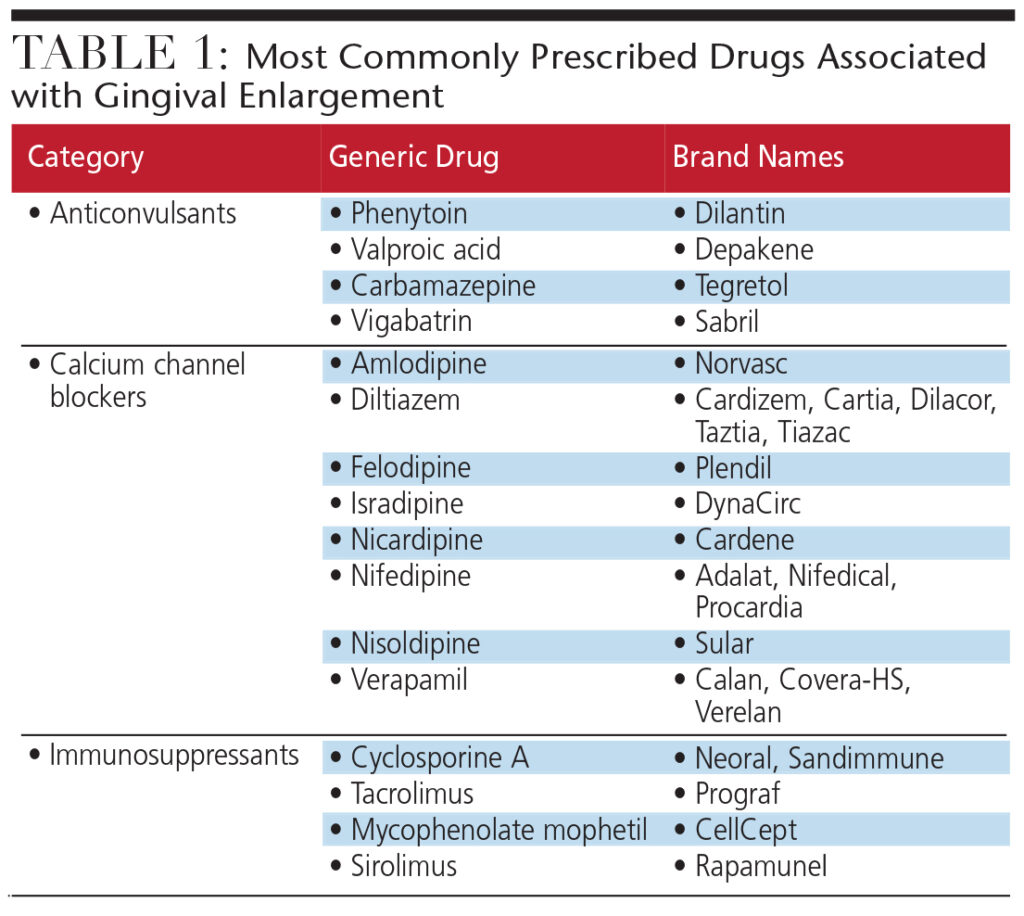
박테리아, 바이러스, 신 생물 및 특정 약물은 치은 건강에 부정적인 영향을 미칠 수 있습니다. 치은 비대는 감염, 충치 및 치주 질환의 위험을 높이고 미소 미학에 부정적인 영향을 미칩니다. 전신 및 염증 요인에 의해 시작되는 치은 비대는 흔히 일반적인 처방약에 의해 발생합니다. 이러한 약물 (항 경련제, 칼슘 채널 차단제 (CCB) 및 면역 억제제)은 섬유 아세포 기능의 변화를 촉진하여 치은 결합 조직의 세포 외 기질을 증가시킵니다 (표 1). 정상적인 섬유 아세포 기능과 치은 건강을 회복하기 위해 문제가되는 약물을 다른 약물로 대체해야 할 수 있습니다. 대체가 불가능한 경우, 치은 조직의 외과 적 절제가 약물로 인한 치은 비대에 영향을받은 환자에게 일시적인 완화를 제공 할 수 있습니다.
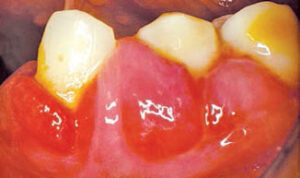
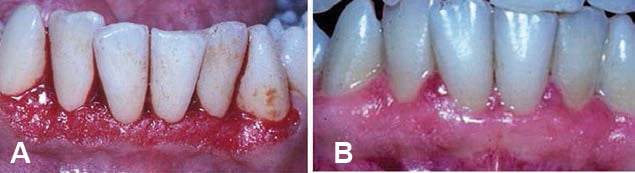
1938 년 Merritt와 Putnam이 페니토인을 발견하여 간질 환자 .1 그러나 도입 직후 페니토인과 치은과 성장을 연결하는보고가 표면화되기 시작했습니다 .2 양성 확대의 유병률이 인구 하위 집합에 따라 다르기 때문에이 약물에 대한 감수성은 보편적이지 않습니다. 항 경련제에 의한 치은 비대는 소아와 입원 환자에서 현저히 높습니다. 기관에 입원하지 않은 환자의 경우 페니토인으로 인한 치은 과성 장의 유병률은 약 50 %이며이 상태는 상악 전치에 가장 자주 영향을 미칩니다 (그림 1) .3 치은 비대는 일반적으로 페니토인의 첫 번째 투여 후 2 개월 ~ 3 개월 후에 나타납니다. , 약 12 개월에서 18 개월 후에 최대 심각도에 도달합니다.
1938 년 이후 페니토인의 부작용을 극복하기 위해 발 프로 산, 카르 바 마제 핀, 페노바르비탈 및 비가 바 트린을 포함한 여러 항 경련제가 도입되었습니다. . 이 약제에서도 치은 비대 사례가 지적되었지만 그러한보고는 드물고 제대로 문서화되지 않았습니다.
경련성 발작 장애를 제어하는 효과와 저렴한 비용과 폭 넓은 가용성으로 인해 페니토인 특히 대말, 측두엽 및 정신 운동 발작의 경우 간질 치료에 여전히 선택되는 약물입니다. 많은 환자들이 새로운 종류의 항 경련제로 대체하기를 꺼리기 때문에 구강 건강 전문가는 증가 된 위험을 인식하고 이러한 환자 집단에서 페니토인 유발 치은 비대를 해결할 준비가되어 있어야합니다.
CALCIUM CHANNEL BLOCKERS
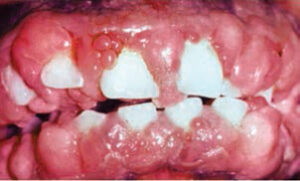
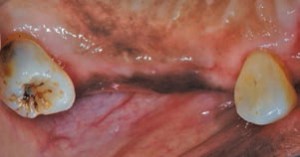
이 종류의 약물은 고혈압, 협심증 및 심 실상 심장 부정맥 관리에 널리 사용됩니다. 이들 약물은 세포막을 통한 칼슘 이온 유입을 방지하여 주요 치료 효과를 도출합니다. 그러나 모든 CCB가 동일한 방식으로 치은에 영향을 미치는 것은 아닙니다. 니페디핀은 약물로 인한 치은 과잉 성장에서 가장 빈번하게 연루된 CCB입니다 (그림 2 ~ 그림 4) .4 Lederman 등은 1984 년에 처음으로 부정적인 구강 영향을보고했으며 후속 연구에 따르면 부작용의 유병률이 14 %에서 83 % .5–7
음성 치은 효과의 유병률은 베라파밀과 암로디핀 (각각 4.2 % 및 3.3 %)에서 상당히 낮습니다.8,9 또한 felodipine, nicardipine, manidipine 및 diltiazem과 같은 새로운 세대의 CCB와 잇몸 비대와 관련된 수많은보고가 있습니다.
면역 억제제
면역 억제제는 주요 장기 (예 : 간, 췌장, 심장 또는 폐) 이식 후 동종 이식 거부 반응의 발생률과 중증도를 줄이고 류마티스 관절염과 같은자가 면역 상태를 관리합니다. .
1977 년 Borel 등이 발견 한 이래, 사이클로스포린 A는 장기 거부를 예방하기 위해 가장 일반적으로 처방되는 약물이되었습니다 .10 불행히도 신 독성, 당뇨병 상태 유도 등 심각한 부작용을 일으킬 수 있습니다. , 만성 두통 및 치은 비대 손상 (그림 5). 치은과 성장에 대한 최초의 발표는 초기 투여 후 4 주에서 6 주 사이에 신장 이식 환자에서보고되었습니다 .11 비대는 치은의 음순 측면에서 더 두드러졌으며 상당한 출혈과 관련이있었습니다. 그러나 수술로 치아를 뽑았을 때 비대는 영구적으로 제거되었습니다. 사이클로스포린 A 관련 치은 비대의 유병률은 8 %에서 81 %이며, 어린이와 청소년이 가장 위험합니다 .12,13
타크로리무스, 마이코 페놀 레이트 모 페틸 및시 롤리 무스와 같은 새로운 면역 억제제가 제공되었습니다. 치은 과잉 성장의 위험없이 장기 이식 환자를 관리하기위한 대체 옵션 .14
임상 특징
각 유형의 약물 유발 치은 비대의 구강 증상은 유사하며 진단 요인은 아닙니다. 상세한 환자 병력을 유지하면 치과 전문가가 정확한 진단을 내리는 데 도움이됩니다. 초기 단계에서 병변은 치간 유두의 확고한 결절 확장으로 나타날 수 있으며 구강 전체에 나타날 수 있습니다. 치은의 과성 장은 구개 / 설측 표면보다 안면 / 구강 표면에서 더 큰 두드러짐과 함께 앞쪽 영역에 더 일반적으로 영향을 미칩니다 .15 비대는 치간 치은 유두의 경미한 증가에서 변연 및 유두 조직의 심한 비대까지 다양합니다. 심한 경우에는 전체 유두와 주변 조직이 확대되어 치은 조직이 엽상 모양으로 보입니다 (그림 6).
확대는 관상으로 확장되어 저작 및 언어를 방해 할 수 있습니다. 또한 전치와 관련된 경우 심미적 문제로 이어질 수 있습니다. 자란 조직은 칫솔이나 치실이 닿지 않는 곳에 병원성 미생물을 저장할 수있는 주머니를 만듭니다.
이러한 약물은 기저 치조골에 직접적인 영향을주지 않지만 기존 치주염 환자에게 치은 비대가 중첩 될 수 있습니다. 또는 환자가 동시에 획득 할 수 있습니다. 치은 비대는 비염증성, 단단하고 섬유 성 치은에서부터 부종, 홍반 및 출혈이 지배적 인 치은 조직에 이르기까지 다양한 형태로 나타날 수 있습니다.
차등 진단
약물로 인한 치은 과성 장은 부족합니다. 구강 건강 전문가가 정확한 진단에 도달하도록 돕는 독특한 임상 마커. 이러한 병변은 유사하게 나타나는 여러 병리학 적 상태를 모방합니다. 확대는 국소화되거나 일반화 될 수 있습니다. 국소 치은 과성 장은 치주 농양, 섬유종 또는 화농성 육아종 (자극, 외상 또는 임신 중 경험하는 것과 같은 호르몬 변동으로 인한 조직 과다 성장)으로 인해 발생할 수 있습니다. 이러한 병변의 국부적 특성은 임상 징후 및 증상, 환자의 의료 및 치과 기록과 함께 약물 사용으로 인한 치은 비대와 구별하는 데 도움이됩니다.
일반화 된 치은 확대 일부 환자에서 어려운 진단 문제를 제기합니다. 대부분의 치은 비대에 관여하는 가장 일반적인 요인은 구강 생물막이며, 이는 우수한자가 관리와 함께 스케일링 및 뿌리 계획을 통해 플라크 유발 치은과 성장으로 처리되어야합니다. 병변이 치료 후 3 주에서 4 주까지 지속되는 경우, 환자는 원인 인자로 전신 질환을 배제하기 위해 의료 제공자에게 의뢰되어야합니다. 진단되지 않거나 제대로 조절되지 않는 당뇨병이 주요 원인으로, 전신 염증성 치은 비대 및 심각한 치주 파괴를 유발합니다.
치은 비대를 유발할 수있는 기타 전신 질환으로는 급성 백혈병, 베게너 육아 종증 및 괴혈병이 있습니다. 출혈을 수반하는 급속한 치은 과성 장은 급성 근모 구성 백혈병, 만성 골수성 백혈병, 급성 림프 구성 백혈병 또는 만성 림프 구성 백혈병의 존재를 나타낼 수 있습니다. 급성 골수 아 구성 백혈병으로 진단받은 환자 중 5 %는 첫 번째 합병증으로 치은 비대를 경험합니다 .16,17 백혈병은 악성 질환이며 성공적인 해결은 조기 진단과 치료에 달려 있습니다. 구강 건강 전문가는 과성 장의 급속한 진행이 확인되면 환자를 의료 전문가에게 의뢰해야합니다 .16,17
베게너 육아 종증에서 치은은 부풀어 오르고 밝은 빨간색으로 나타나며 입상은 “딸기 잇몸”으로 설명됩니다. ” 이러한 특징적인 임상 증상을 통해 감별 진단이 의심 되나 생검으로 확인해야합니다. 비타민 C 결핍으로 인한 괴혈병은 매우 드물지만이 질환에 걸린 환자는 심한 치은 부종과 출혈을 경험할 수 있으며 이동성 치아를 동반 할 수 있습니다. 임상의는이 환자 그룹의 치은 비대를 해결하기 위해 고용량의 비타민 C와 비수술 적 치주 요법에 의존 할 수 있습니다.
또한, 일반화 된 과성 장은 유전성 치은 섬유종증이라는 희귀 한 유전 적 상태 때문일 수 있습니다. 치은의 점진적인 비대를 특징으로합니다. 이러한 경우에는 과도한 섬유 성 치은 조직을 제거하기 위해 일반적으로 외과 적 개입이 필요하지만 병변 재발은 예측할 수 없습니다. 이러한 병변의 섬유 성 특성은 환자의 병력 및 가족력과 함께 약물과 구별 될 수 있습니다. -유도 된 치은과 성장.
병인 및 위험 요인
약물 유도의 병인 ed 치은 확대는 완전히 이해되지 않았습니다. 이는 콜라게나 아제에 의한 콜라겐 분해 감소 또는 세포 외 기저 물질의 과잉 생산 결과 때문일 수 있습니다 .18,19 다른 가능한 경로는 이러한 약물에 유 전적으로 감수성 인 치은 섬유 아세포의 하위 집합의 존재입니다 .20 Johnson 등은보고했습니다. 인간 치은 섬유 아세포에 의한 콜라겐 합성 향상에있어 전 염증성 사이토 카인 (IL-1b 및 IL-6)의 시너지 효과는이 비대와 관련된 또 다른 가능한 요인입니다 .21
바이오 필름은 모든 형태의 일반적인 위험 요소입니다. 염증성 치주 질환의 원인이되며 약물로 인한 치은 비대를 악화시킵니다. 다른 위험 요인에는 성별이 포함될 수 있습니다. 남성은 여성보다 치은 과잉 성장이 발생할 가능성이 3 배 더 높기 때문입니다 .22 연령은 페니토인 및 사이클로스포린 A로 인한 치은 비대와 역 상관 관계가 있습니다. 어린이와 청소년이 성인보다 이러한 병변의 유병률이 더 높기 때문입니다. .23 복용량과 관련하여, 비대 정도와 이러한 약물 종류의 일일 섭취량 사이의 연관성에 대한 상충되는보고가 있습니다. 대부분의보고는 약물 투여 량과 치은 비대의 중증도 사이에 중요한 관계를 발견하지 못했습니다 .18
치료
약물로 인한 치은 비대에 대한 가장 효과적인 치료법은 불쾌한 약물. 의료 서비스 제공자는 CCB를 베타 차단제, 이뇨제 또는 안지오텐신 전환 효소 억제제로 대체 할 수 있습니다. 예를 들어 구강 조직에는 영향을 미치지 않습니다. Phenytoin은 carbamazepine, ethosuximide 또는 sodium valproate로 대체 될 수 있습니다 .24 Cyclosporine A는 tacrolimus로 대체 될 수 있습니다. 이러한 옵션에도 불구하고 의사와 환자는 특히 질병이 잘 통제되거나 다른 옵션이 이미 탐색 된 경우 다른 요법으로 전환하기를 꺼립니다. 약물 교체가 옵션이 아닌 경우 일부 병변은 비수술 적으로 관리 될 수 있습니다. CCB로 유발 된 치은 비대의 경미한 병변은 스케일링과 치근 계획 및 항균 구강 세정제에 호의적으로 반응합니다.
좋은 구강 위생은 추가 염증을 예방하고 정기적 인 비수술 적 치주 요법을 포함하여 전문적인 치료를 통해 긍정적 인 결과를 유지하는 데 중요합니다.페니토인에 의한 확대의 경우, 병변의 콜라겐 함량이 높기 때문에 스케일링 및 뿌리 편평에 대한 치은 반응이 좋지 않아 상당한 조직 수축을 방지합니다.
확장 된 조직의 수술 적 절제 치은 절제술은 의사 주머니를 제거하여 조직 구조, 외관 및 기능을 복원 할 수 있습니다. 이 절차는 블레이드, 수술 용 칼, 전기 수술 장치 또는 레이저로 수행됩니다 (그림 7). 약물로 인한 치은 비대의 재발은 외과 적 또는 비수술 적 방법으로 치료 한 경우에보고되었습니다. 특히 문제가되는 약물의 중단이 일시적이거나 애초에 선택 사항이 아닌 경우에 더욱 그렇습니다. 재발은 중재 후 3 ~ 6 개월 이내에 발생할 수 있으며 환자의 최대 40 %에 영향을 미칩니다 .25 구강 위생이 좋지 않거나 전문적인 치료를받을 수없는 사람들에게 재발이 더 흔합니다 (그림 8).
약물로 인한 치은 비대는 다양한 약물로 인해 발생할 수있는 일반적인 상태입니다. 이러한 병변은 플라크 관련 병변과 구별 할 수있는 임상 마커가 없으며 진단하기 어려울 수 있습니다. 상세한 병력은 약물로 인한 치은 비대를 보이는 환자의 병인, 진단 및 치료 옵션에 관한 임상의를 안내하는 데 도움이됩니다.
- Merritt HH, Putnam TJ. 획기적인 기사 1938 년 9 월 17 일 : 경련성 질환 치료에 사용되는 나트륨 디 페닐 히단 토이 네이트. JAMA. 1984; 251 : 1062–1067.
- Kimball OP. diphenylhydantoinate 나트륨으로 간질 치료. JAMA. 1939; 112 : 1244–1245.
- Casetta I, Granieri E, Desidera M, et al. 페니토인 유도 치은과 성장 : 이탈리아 페라라의 지역 사회 기반 횡단면 연구. 신경 역학. 1997; 16 : 296–303.
- Butler RT, Kalkwarf KL, Kaldahl WB. 약물 유발 치은 증식 : 페니토인, 사이클로스포린 및 니페디핀. J Am Dent Assoc. 1987; 114 : 56–60.
- Lederman D, Lumerman H, Reuben S, Freedman PD. 니페디핀 요법과 관련된 치은 증식. 사건보고. Oral Surg Oral Med Oral Pathol. 1984; 57 : 620–622.
- Barak S, Engelberg IS, Hiss J. 니페디핀으로 인한 치은 증식. 조직 병리학 적 소견. J Periodontol. 1987; 58 : 639–642.
- Fattore L, Stablein M, Bredfeldt G, Semla T, Moran M, Doherty-Greenberg JM. 치은 증식 : 니페디핀과 딜 티아 젬의 부작용. Spec Care Dentist. 1991; 11 : 107–109.
- 밀러 CS, Damm DD. 치과 인구에서 베라파밀 유발 치은 증식의 발생률. J Periodontol. 1992; 63 : 453–456.
- Jorgensen MG. 암로디핀 관련 치은 증식의 유병률. J Periodontol. 1997; 68 : 676–678.
- Borel JF, Feurer C, Magnée C, Stähelin H. 동물에서 새로운 항 림프구 펩티드 사이클로스포린 A의 효과. 면역학. 1977; 32 : 1017–1025.
- Rateitschak-Plüss EM, Hefti A, Lörtscher R, Thiel G. 사이클로스포린 -A가 사람의 치은 비대를 유도한다는 초기 관찰. J Clin Periodontol. 1983; 10 : 237–246.
- Friskopp J, Klintmalm G. 치은 확대. 시클로 스포린과 아자 티오 프린 치료를받은 신장 동종 이식 수혜자 간의 비교. Swed Dent J. 1986; 10 : 85–96.
- Pernu HE, Pernu LM, Huttunen KR, Nieminen PA, Knuuttila ML. 면역 억제제와 가능한 국소 적 배경 요인과 관련된 신장 이식 수혜자의 치은 과잉 성장. J Periodontol. 1992; 63 : 548–553.
- Keown PA. 새로운 면역 억제 전략. Curr Opin Nephrol Hypertens. 1998; 7 : 659–663.
- Marshall RI, Bartold PM. 약물 유발 치은과 성장에 대한 임상 검토. Aust Dent J. 1999; 44 : 219–232.
- Demirer S, Ozdemir H, Sencan M, Marakoglu I. 급성 단핵구 백혈병의 조기 진단 구강 증상으로서의 치은 증식 : 증례보고. Eur J Dent. 2007; 1 : 111–114.
- Wu J, Fantasia JE, Kaplan R. 급성 골수 단핵구 성 백혈병의 경구 발현 : 백혈병 분류에 대한 사례 보고서 및 검토. J Periodontol. 2002; 73 : 664–668.
- Barclay S, Thomason JM, Idle JR, Seymour RA. 니페디핀 유발 치은 과성 장의 발생률과 심각도. J Clin Periodontol. 1992; 19 : 311–314.
- Lucas RM, Howell LP, Wall BA. 니페디핀 유발 치은 증식. 조직 화학 및 초 구조 연구. J Periodontol. 1985; 56 : 211–215.
- Pernu HE, Knuuttila MLE, Huttenen KRH, Tiilikainen ASK. 약물 유발 치은과 성장 및 클래스 I1 주요 조직 적합성 항원. 이식. 1994; 57 : 1811–1813.
- Johnson RB, Zebrowski EJ, Dai X. 체외에서 니페디핀과 인터루킨 -1- 베타에 노출 된 인간 치은 섬유 아세포에 의한 콜라겐 성 단백질 합성의 시너지 향상. J Oral Pathol Med. 2000; 29 : 8–12.
- Ellis JS, Seymour RA, Steele JG, Robertson P, Butler TJ, Thomason JM. 칼슘 채널 차단제에 의한 치은 과성 장의 유병률 : 커뮤니티 기반 연구. J Periodontol. 1999; 70 : 63–67.
- Daley TD, Wysocki GP, Day C.사이클로스포린 유발 치은 증식의 임상 적 및 약리학 적 상관 관계. Oral Surg Oral Med Oral Pathol. 1986; 62 : 417–421.
- Seymour RA, Smith DG, Turnbull DN. 성인 간질 환자의 치주 건강에 대한 페니토인과 발 프로 산 나트륨의 효과. J Clin Periodontol. 1985; 12 : 413–419.
- Ilgenli T, Atilla G, Baylas H. 약물 유발 치은 과다 성장 환자에서 치주 요법의 효과. 장기적인 결과. J Periodontol. 1999; 70 : 967–972.