Dette kurset ble publisert i mars 2016-utgaven og utløper 31.3.19. Forfatterne har ingen kommersielle interessekonflikter å avsløre. Denne 2 studiepoeng selvstudiet er elektronisk formidlet.
MÅL
Etter å ha lest dette kurset, skal deltakeren være i stand til å:
- Diskuter de forskjellige typene medisiner som kan forårsake tannkjøttforstørrelse.
- Identifiser de kliniske egenskapene til tannkjøttforstørrelse.
- Forklar etiologien og risikofaktorene for medisinindusert tannkjøttutvidelse.
- Liste over tilgjengelige alternativer for behandling av denne tilstanden.
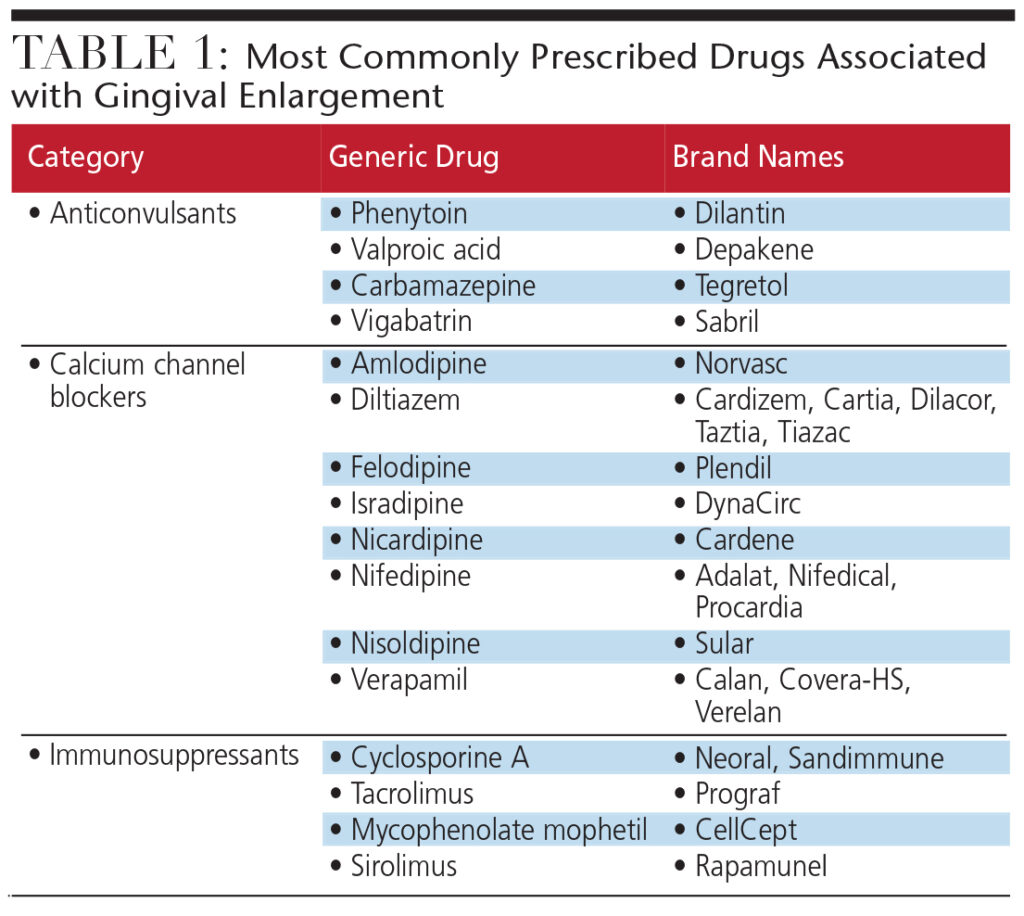
Bakterier, virus, svulster og visse medisiner kan påvirke tannkjøttets helse negativt. Gingivalforstørrelse øker risikoen for infeksjon, karies og periodontal sykdom, og påvirker smilestetikk negativt. Initiert av både systemiske og inflammatoriske faktorer, er tannkjøttforstørrelse ofte forårsaket av vanlige reseptbelagte medisiner. Disse stoffene – antikonvulsiva, kalsiumkanalblokkere (CCB) og immunsuppressiva – fremmer endringer i fibroblastfunksjonen, noe som fører til en økning i den ekstracellulære matrisen til bindevevet i tannkjøttet (tabell 1). For å gjenopprette normal fibroblastfunksjon og tannkjøtthelse, kan det hende at et annet medikament må erstattes med den krenkende medisinen. Når erstatning ikke er mulig, kan kirurgisk eksisjon av tannkjøttvev gi midlertidig lindring til pasienter som er rammet av medikamentindusert tannkjøttforstørrelse.
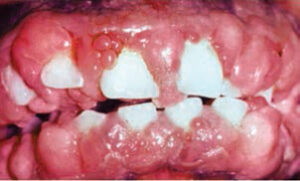
Oppdagelsen av fenytoin i 1938 av Merritt og Putnam ga et stort gjennombrudd i behandlingen av pasienter med epilepsi.1 Kort tid etter introduksjonen begynte det imidlertid å dukke opp rapporter som knytter fenytoin til tannkjøttovervekst.2 Følsomhet overfor dette legemidlet er ikke universell, da forekomsten av godartet utvidelse varierer mellom befolkningens undergrupper. Forstørrelse av tannkjøtt indusert av antikonvulsiva er betydelig høyere blant barn og institusjonaliserte pasienter. For ikke-institusjonaliserte pasienter er forekomsten av tannkjøttovervekst forårsaket av fenytoin omtrent 50%, og tilstanden påvirker oftest de fremre tennene i kjevehulen (figur 1) .3 Tandkjøttforstørrelse vises vanligvis to måneder til tre måneder etter at den første dosen av fenytoin er tatt og nådde maksimal alvorlighetsgrad ca. 12 måneder til 18 måneder senere.
Siden 1938 har flere antikonvulsive midler blitt introdusert – inkludert valproinsyre, karbamazepin, fenobarbital og vigabatrin – i et forsøk på å overvinne de negative effektene av fenytoin. . Det er også observert tilfeller av tannkjøttforstørrelse med disse midlene, men slike rapporter er sjeldne og dårlig dokumentert.
På grunn av dens effektivitet i å kontrollere krampeanfall, så vel som den lave kostnad og bred tilgjengelighet, fenytoin er fremdeles det valgte medikamentet for behandling av epilepsi – spesielt for grand mal, temporal lobe og psykomotoriske anfall. Mange pasienter er motvillige til å erstatte den med en ny klasse antikonvulsiva, noe som gjør det viktig at oral helsepersonell anerkjenner den økte risikoen og er forberedt på å adressere fenytoin-indusert tannkjøttforstørrelse i disse pasientpopulasjonene.
KALSIKKANALBLOCKERINGER
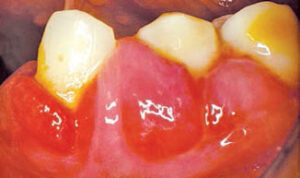
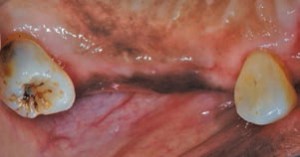
Denne medisinen er mye brukt for å håndtere hypertensjon, angina og supraventrikulær hjerterytmeforstyrrelse. Disse stoffene får sine viktigste terapeutiske effekter ved å forhindre kalsiumiontilstrømning gjennom cellemembraner. Ikke alle sentralbanker påvirker gingiva på samme måte. Nifedipin er den hyppigst impliserte CCB i medikamentindusert gingival gjengroing (figur 2 til og med figur 4). 4 Lederman et al rapporterte først sine negative orale effekter i 1984, og påfølgende studier viste at forekomsten av bivirkninger varierte fra 14% til 83% .5–7
Forekomsten av negative gingivaleffekter er betydelig lavere med verapamil og amlodipin (henholdsvis 4,2% og 3,3%).8,9 Tallrike rapporter har også assosiert med utvidelse av tannkjøttet med den nye generasjonen av CCB, slik som felodipin, nikardipin, manidipin og diltiazem.
IMMUNOSUPPRESSANTER
Immunosuppressiva reduserer forekomsten og alvorlighetsgraden av avvisning av allograft etter transplantasjoner av store organer (f.eks. lever, bukspyttkjertel, hjerte eller lunge), samt for å håndtere autoimmune tilstander, som revmatoid artritt .
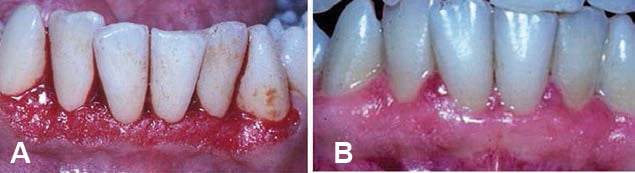
Siden oppdagelsen av Borel et al i 1977, har syklosporin A blitt det mest foreskrevne legemidlet for å forhindre organavstøtning.10 Det kan dessverre utøve alvorlige bivirkninger, inkludert nefrotoksisitet, induksjon av en diabetisk tilstand. , kronisk hodepine og skjemmende gingivalforstørrelse (figur 5). Den første publiseringen av tannkjøttovervekst ble rapportert hos nyretransplanterte pasienter fire uker til seks uker etter startdosen.11 Forstørrelsen var mer uttalt på det labiale aspektet av tannkjøttet, og var assosiert med betydelig blødning. Når tennene ble trukket ut kirurgisk, ble forstørrelsen imidlertid permanent eliminert. Forekomsten av cyklosporin A-assosiert tannkjøttforstørrelse varierer fra 8% til 81%, med barn og ungdommer med størst risiko. 12,13
Nye immunsuppressive medikamenter, som takrolimus, mykofenolatmophetil og sirolimus, har gitt alternative muligheter for å håndtere organtransplantasjonspasienter uten risiko for tannkjøttovervekst.14
KLINISKE FUNKSJONER
Mens den orale manifestasjonen av hver type medikamentindusert tannkjøttforstørrelse er lik, det er ikke en diagnostisk faktor. Å ha en detaljert pasientmedisinsk historie vil hjelpe tannleger å oppnå en nøyaktig diagnose. I sine innledende stadier kan lesjoner fremstå som en fast nodulær forstørrelse av de interdentale papiller, og kan forekomme i munnhulen. Gingival gjengroing påvirker oftere den fremre regionen, med større uttalelse på ansikts / bukkale overflater enn palatal / lingual overflater.15 Forstørrelsen kan variere fra en mild økning av interproximal gingival papiller til alvorlig utvidelse av både marginale og papillære vev. I alvorlige tilfeller forstørres hele papiller og omkringliggende vev, noe som gir tannkjøttvevet et lobulert utseende (figur 6).
Forstørrelsen kan strekke seg koronalt og forstyrre mastiksjon og tale; I tillegg kan det føre til estetiske problemer i tilfeller med fremre tenner. Overgrodd vev skaper lommer som kan huse patogene mikrober utenfor rekkevidden til en tannbørste eller tanntråd.
Selv om disse stoffene ikke direkte påvirker det underliggende alveolære beinet, kan tannkjøttforstørrelsen bli overlappet blant pasienter med allerede eksisterende periodontitt, eller pasienter kan få det samtidig. Gingivalforstørrelse kan presentere seg med forskjellige former, alt fra ikke-betent, fast og fibrøs gingiva til tannkjøttvev dominert av ødem, erytem og blødning.
DIFFERENTIELL DIAGNOS
Legemiddelindusert gingivalovervekst mangler særegen klinisk markør for å hjelpe oral helsepersonell i å nå en nøyaktig diagnose. Disse lesjonene etterligner flere patologiske tilstander som manifesterer seg på samme måte. Utvidelsen kan være lokalisert eller generalisert. En lokal gingival gjengroing kan være forårsaket av en periodontal abscess, fibroma eller et pyogent granulom (vevs gjengroing forårsaket av irritasjon, traumer eller hormonelle svingninger, slik som opplevd under graviditet). Den lokale naturen til disse lesjonene – sammen med de kliniske tegnene og symptomene og pasientens medisinske og tannhistorie – bidrar til å skille dem fra tannkjøttforstørrelse forårsaket av medisinering.
Generalisert gingivalforstørrelse utgjør en vanskelig diagnostisk utfordring hos noen pasienter. Den vanligste faktoren involvert i flertallet av tannkjøttforstørrelsen er oral biofilm, som skal behandles som plakkindusert tannkjøttvekst med skalering og rotplaning, kombinert med god egenomsorg. Hvis lesjonene vedvarer tre uker til fire uker etter behandlingen, bør pasienten henvises til en medisinsk leverandør for å utelukke systemisk sykdom som en årsaksfaktor. Utiagnostisert eller dårlig kontrollert diabetes er en viktig skyldige som forårsaker generalisert inflammatorisk utvidelse av tannkjøttet og betydelig periodontal ødeleggelse.
Andre systemiske sykdommer som kan forårsake tannkjøttforstørrelse inkluderer akutt leukemi, Wegeners granulomatose og skjørbuk. Rask gingival gjengroing ledsaget av blødning kan indikere tilstedeværelsen av akutt myeoblastisk leukemi, kronisk myeloid leukemi, akutt lymfocytisk leukemi eller kronisk lymfocytisk leukemi. Blant pasienter diagnostisert med akutt myeloblastisk leukemi, opplever 5% tannkjøttforstørrelse som den første komplikasjonen. 16,17 Leukemi er en ondartet sykdom, og den vellykkede oppløsningen avhenger av tidlig diagnose og behandling. Oral helsepersonell bør henvise pasienter til en medisinsk fagperson når rask fremvekst av gjengroing er notert. 16,17
I Wegeners granulomatose virker tannkjøttet hovent og knallrødt, med en granulær overflate beskrevet som «jordbærgummi. ” Differensialdiagnose mistenkes gjennom denne karakteristiske kliniske manifestasjonen, men den må bekreftes ved biopsi. Skjørbuk, resultatet av vitamin C-mangel, er ganske sjelden, men pasienter som er rammet av denne tilstanden kan oppleve alvorlig gingival hevelse og blødning, ledsaget av mobile tenner. Klinikere kan stole på en høy dose av vitamin C og ikke-kirurgisk periodontal behandling for å løse tannkjøttforstørrelse i denne pasientgruppen.
I tillegg kan generalisert gjengroing skyldes en sjelden genetisk tilstand som kalles arvelig gingival fibromatose, som er preget av en progressiv forstørrelse av tannkjøttet. Disse tilfellene krever vanligvis kirurgisk inngrep for å fjerne overflødig fibrotisk tannkjøttvev, men gjentakelse av lesjon er uforutsigbar. Den fibrotiske naturen til disse lesjonene, sammen med pasientens medisinske historie og familiehistorie, kan skille dem fra legemiddel -indusert gingival gjengroing.
ETIOLOGI OG RISIKOFAKTORER
Patogenesen av medikamentindusert ed gingival utvidelse er ikke helt forstått. Det kan være på grunn av en reduksjon av kollagennedbrytning ved kollagenase, eller resultatet av overproduksjon av ekstracellulært grunnstoff.18,19 Andre mulige veier er tilstedeværelsen av en undergruppe av gingival fibroblaster som er genetisk utsatt for disse medisinene.20 Johnson et al. Har rapportert den synergistiske effekten av proinflammatoriske cytokiner (IL-1b og IL-6) i forbedring av kollagensyntese av humane gingivalfibroblaster som en annen mulig faktor involvert i denne utvidelsen.21
Biofilm er en vanlig risikofaktor for alle former av inflammatorisk periodontal sykdom, og dens tilstedeværelse forverrer medikamentindusert tannkjøttforstørrelse. Andre risikofaktorer kan inkludere kjønn, ettersom menn har tre ganger større sannsynlighet for å utvikle tannkjøttovervekst enn kvinner. 22 Alder er omvendt korrelert med fenytoin- og cyklosporin A-indusert tannkjøttforstørrelse, ettersom barn og tenåringer har en høyere forekomst av disse lesjonene enn voksne .23 Når det gjelder dosering, er det motstridende rapporter om en sammenheng mellom alvorlighetsgraden av utvidelsen og det daglige inntaket av noen av disse legemiddelklassene. Flertallet av rapportene har ikke oppdaget en signifikant sammenheng mellom medikamentdosering og alvorlighetsgraden av tannkjøttforstørrelse.18
BEHANDLING
Den mest effektive behandlingen for medisinindusert tannkjøttforstørrelse er å trekke tilbake fornærmende narkotika. Medisinske leverandører kan for eksempel erstatte CCB med betablokkere, diuretika eller angiotensinkonverterende enzymhemmere – ingen av dem påvirker det orale vevet. Fenytoin kan erstattes av karbamazepin, etosuksimid eller natriumvalproat. 24 Syklosporin A kan erstattes med takrolimus. Til tross for disse alternativene er leger og pasienter ofte motvillige til å bytte til et annet regime, spesielt når sykdommen er godt kontrollert eller andre alternativer allerede er utforsket. Hvis det ikke er mulig å bytte medisiner, kan noen lesjoner håndteres ikke-kirurgisk. Mild lesjoner av CCB-indusert tannkjøttforstørrelse reagerer gunstig på skalering og rotplaning og antimikrobiell munnskylle.
God munnhygiene er avgjørende for å forhindre ytterligere betennelse og opprettholde positive resultater oppnådd med profesjonell pleie, inkludert periodisk ikke-kirurgisk periodontal behandling.Når det gjelder fenytoin-indusert utvidelse, er ikke tannkjøttresponsen på skalering og rotplaning ikke så gunstig på grunn av det høye innholdet av kollagen i lesjonene, noe som forhindrer betydelig vevskrymping.
Kirurgiske eksisjoner av det forstørrede vevet ved gingivektomi kan eliminere pseudolommene, og gjenopprette vevsarkitektur, utseende og funksjon. Denne prosedyren utføres med kniver, kirurgiske kniver, elektrokirurgiske enheter eller lasere (figur 7). Gjentakelse av medikamentindusert tannkjøttforstørrelse har blitt rapportert i tilfeller behandlet med kirurgiske eller ikke-kirurgiske metoder – spesielt hvis opphør av det krenkende legemidlet bare var midlertidig eller ikke et alternativ i utgangspunktet. Gjentakelse kan forekomme så tidlig som tre til seks måneder etter intervensjonen, og rammer så mange som 40% av pasientene.25 Gjentakelse er mer vanlig blant de med dårlig munnhygiene eller som mangler tilgang til profesjonell pleie (Figur 8).
Legemiddelindusert utvidelse av tannkjøttet er en vanlig tilstand som kan være forårsaket av en rekke medisiner. Disse lesjonene mangler kliniske markører som skiller seg fra plakkassosierte lesjoner, og kan være vanskelig å diagnostisere. En detaljert medisinsk historie vil hjelpe klinikere med hensyn til etiologi, diagnose og behandlingsalternativer for pasienter som presenterer medikamentindusert tannkjøttforstørrelse.
- Merritt HH, Putnam TJ. Landemerkeartikkel 17. september 1938: Sodium difenylhydantoinate i behandlingen av krampeforstyrrelser. JAMA. 1984; 251: 1062–1067.
- Kimball OP. Behandling av epilepsi med natriumdifenylhydantoinat. JAMA. 1939; 112: 1244-1245.
- Casetta I, Granieri E, Desidera M, et al. Fenytoin-indusert gingival gjengroing: En samfunnsbasert tverrsnittsstudie i Ferrara, Italia. Nevroidemiologi. 1997; 16: 296–303.
- Butler RT, Kalkwarf KL, Kaldahl WB. Legemiddelindusert gingival hyperplasi: fenytoin, cyklosporin og nifedipin. J Am Dent Assoc. 1987; 114: 56–60.
- Lederman D, Lumerman H, Reuben S, Freedman PD. Gingival hyperplasi assosiert med nifedipinbehandling. Rapport om en sak. Oral Surg Oral Med Oral Pathol. 1984; 57: 620–622.
- Barak S, Engelberg IS, Hiss J. Gingival hyperplasi forårsaket av nifedipin. Histopatologiske funn. J Periodontol. 1987; 58: 639–642.
- Fattore L, Stablein M, Bredfeldt G, Semla T, Moran M, Doherty-Greenberg JM. Gingival hyperplasi: en bivirkning av nifedipin og diltiazem. Spec Care Tannlege. 1991; 11: 107–109.
- Miller CS, Damm DD. Forekomst av verapamil-indusert gingival hyperplasi i en tannpopulasjon. J Periodontol. 1992; 63: 453–456.
- Jorgensen MG. Utbredelse av amlodipin-relatert gingival hyperplasi. J Periodontol. 1997; 68: 676–678.
- Borel JF, Feurer C, Magnée C, Stähelin H. Effekter av det nye anti-lymfocytiske peptidet cyclosporin A hos dyr. Immunologi. 1977; 32: 1017–1025.
- Rateitschak-Plüss EM, Hefti A, Lörtscher R, Thiel G. Innledende observasjon om at cyclosporin-A induserer tannkjøttforstørrelse hos mennesker. J Clin periodontol. 1983; 10: 237-246.
- Friskopp J, Klintmalm G. Gingival utvidelse. En sammenligning mellom syklosporin- og azathioprin-behandlede nyreproduktmottakere. Swed Dent J. 1986; 10: 85–96.
- Pernu HE, Pernu LM, Huttunen KR, Nieminen PA, Knuuttila ML. Gingival gjengroing blant nyretransplantasjonsmottakere relatert til immunsuppressiv medisinering og mulige lokale bakgrunnsfaktorer. J Periodontol. 1992; 63: 548–553.
- Keown PA. Nye immunsuppressive strategier. Curr Opin Nephrol Hypertens. 1998; 7: 659–663.
- Marshall RI, Bartold PM. En klinisk gjennomgang av medisinindusert gingival gjengroing. Aust Dent J. 1999; 44: 219–232.
- Demirer S, Ozdemir H, Sencan M, Marakoglu I. Gingival hyperplasi som en tidlig diagnostisk oral manifestasjon ved akutt monocytisk leukemi: en saksrapport. Eur J Dent. 2007; 1: 111–114.
- Wu J, Fantasia JE, Kaplan R. Orale manifestasjoner av akutt myelomonocytisk leukemi: en saksrapport og gjennomgang av klassifiseringen av leukemier. J Periodontol. 2002; 73: 664–668.
- Barclay S, Thomason JM, Idle JR, Seymour RA. Forekomsten og alvorlighetsgraden av nifedipin-indusert tannkjøtt gjengroing. J Clin periodontol. 1992; 19: 311–314.
- Lucas RM, Howell LP, Wall BA. Nifedipin-indusert gingival hyperplasi. En histokjemisk og ultrastrukturell studie. J Periodontol. 1985; 56: 211–215.
- Pernu HE, Knuuttila MLE, Huttenen KRH, Tiilikainen ASK. Legemiddelindusert gingival gjengroing og klasse I1 store histokompatibilitetsantigener. Transplantasjon. 1994; 57: 1811–1813.
- Johnson RB, Zebrowski EJ, Dai X. Synergistisk forbedring av kollagen protein-syntese av humane gingivalfibroblaster eksponert for nifedipin og interleukin-1-beta in vitro. J Oral Pathol Med. 2000; 29: 8–12.
- Ellis JS, Seymour RA, Steele JG, Robertson P, Butler TJ, Thomason JM. Utbredelse av tannkjøttovervekst indusert av kalsiumkanalblokkere: en samfunnsbasert studie. J Periodontol. 1999; 70: 63–67.
- Daley TD, Wysocki GP, dag C.Kliniske og farmakologiske sammenhenger i cyklosporin-indusert gingival hyperplasi. Oral Surg Oral Med Oral Pathol. 1986; 62: 417–421.
- Seymour RA, Smith DG, Turnbull DN. Effekten av fenytoin og natriumvalproat på periodontal helse hos voksne epileptiske pasienter. J Clin periodontol. 1985; 12: 413–419.
- Ilgenli T, Atilla G, Baylas H. Effektivitet av periodontal behandling hos pasienter med medisinindusert tannkjøttovervekst. Langsiktige resultater. J Periodontol. 1999; 70: 967–972.