Inhalasjonsmidler brukes som misbruk av et stort antall mennesker globalt. Disse stoffene finnes i en rekke billige og lovlig tilgjengelige kommersielle produkter (tynner, bensin og lim osv.), Som er allment tilgjengelige i supermarkeder, arbeidsplasser og online (Ridenour et al., 2007). I USA rapporterte omtrent 5,2% av tenåringer inhalasjonsbruk minst en gang i løpet av livet (Johnston et al., 2014). De flyktige forbindelsene kan inhaleres ved forskjellige metoder, som er referert til som «sniffing», «snorting», «huffing» og «bagging.» Vanligvis er varigheten av inhalasjonen noen få minutter (10–15 min). I løpet av denne perioden kan imidlertid en høy konsentrasjon av løsemidler (over 6000 ppm) inhaleres, og denne rutinen kan utføres flere ganger om dagen (Bowen et al., 2006).
Innånding av løsningsmidler har skadelige effekter på hjernen, gir alvorlige systemiske svekkelser, og øker risikoen for selvmord og død (Ridenour et al., 2007). Misbruk av løsemidler kan resultere i nevrologiske lidelser, inkludert psykiatriske sykdommer som depresjon, angst, bipolar stemningsforstyrrelse og avhengighet (Ridenour et al., 2007). Langvarig eksponering for organiske løsningsmidler kan også gi kronisk encefalopati, som er preget av abnormiteter i hjernestrukturer og kognitiv dysfunksjon (Ramcharan et al., 2014).
Vanligvis resulterer kommersielt misbruk av løsemidler i eksponering for flere flyktige stoffer, som toluen, n-heksan, xylen og benzen. Dette gjør det vanskelig å studere de nevrotoksiske effektene av de enkelte bestanddelene (Ramcharan et al., 2014). Derfor må forskere studere effekten av hvert løsemiddel for å avklare deres rolle i hjernedegenerasjon og nevrologisk svekkelse.
Sykloheksan er et flyktig stoff som har vært involvert i kognitiv forverring (Bespalov et al., 2003; Lammers et al., 2009). Opprinnelig ble cykloheksan ansett som en trygg erstatning for benzen og toluen på grunn av mangel på kreftfremkallende effekter og lav toksisitet (Sikkema et al., 1995; Yuasa et al., 1996). Imidlertid er cykloheksan et sterkt lipofilt molekyl som lett kan diffundere gjennom nevrale vev og målrette mot mange hjerneområder (figur 1). Effekten av cykloheksaninnånding på nervesystemet ble først evaluert hos skoarbeidere. Etter en 6 timers eksponering for lave nivåer av dette løsningsmidlet utvikler forsøkspersoner dempet syn (Yasugi et al., 1994), søvnighet, svimmelhet, svakhet i lemmer, sensoriske forstyrrelser (hypestesi og parestesi) og motorisk dysfunksjon i median, ulnar og peroneale nerver (Mutti et al., 1982; Yuasa et al., 1996). Frivillige utsatt for en moderat konsentrasjon av cykloheksan (250 ppm) rapporterte en høyere forekomst av hodepine, tørr hals og verbal hukommelsessvikt enn personer utsatt for svært lave konsentrasjoner av forbindelsen (25 ppm; Lammers et al., 2009). I denne studien av Lammers et al. (2009) tilsvarte sykloheksankonsentrasjonen typiske yrkeseksponeringsnivåer. Imidlertid er effekten av rekreasjonsdoser av cykloheksan (ofte over 6000 ppm) fortsatt ukjent. Å identifisere minimumskonsentrasjonen av cykloheksan som produserer nevral degenerasjon, vil hjelpe regulatorer til å sette grenser for konsentrasjonen av dette løsningsmidlet i kommersielt tilgjengelige produkter.
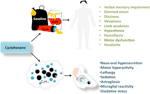
Figur 1. Atferdsmessige og histologiske endringer observert etter cykloheksaninnånding hos mennesker og gnagere.
De kliniske egenskapene til løsemiddelmisbrukere inkluderer nedsatt motor, eufori, spenning, ataksi og depresjon. Løsningsmidler som toluen og trikloretylen (TCE) viser bifasisk dose-responskurver, preget av motorisk eksitasjon ved lave eksponeringsnivåer, og motorisk svekkelse, sedering og anestesi ved høye eksponeringsnivåer (Bowen et al., 2006). Interessant, en lignende bifasisk dose-responseffekt er blitt beskrevet hos mus eksponert for cykloheksan, og er assosiert med nevrohistologiske endringer (Campos-Ordonez et al., 2015). Videre produserer disse flyktige løsningsmidlene dramatiske strukturelle endringer i hjernen, inkludert atrofi av hjernebarken, hvit substans, corpus callosum, hippocampus, hjernestamme, lillehjernen, basalganglier, røde kjerner og substantia nigra (Fan et al., 2014; Ramcharan et al., 2014). Eksperimentelle modeller av toluen, 1-brompropan, TCE og diklormetaneksponering har avslørt tilstedeværelsen av astrocyttereaktivitet og en mikroglialrespons i hippocampus, lillehjernen og hjernebarken. Den astrogliale responsen på hjernens fornærmelser er preget av økt celleproliferasjon, hypertrofi og økt ekspresjon av glialfibrillært surt protein (GFAP; Gonzalez-Perez et al., 2015).Til sammenligning er mikroglialresponsen preget av dramatiske morfologiske endringer som inkluderer en overgang til en amoeboid morfologi og en reduksjon i cellulære prosesser (Gonzalez-Perez et al., 2012).
Sykloheksan i konsentrasjoner som er typiske for de brukt av narkotikabrukere (9000 ppm) induserer også en gliacellerespons i hippocampus (Campos-Ordonez et al., 2015). Astrocyts- og mikroglialresponsene kan ha to og motsatte effekter på CNS. Disse cellene kan være nevrobeskyttende fordi de skiller ut flere nevrotrofiske faktorer og fjerner giftstoffer (Gonzalez-Perez et al., 2015). Imidlertid kan disse cellene også utøve en nevrotoksisk effekt fordi de utskiller inflammatoriske cytokiner og produserer nitrogenoksid og andre reaktive oksygenarter (ROS) som fører til nerveskader og celledød (Gonzalez-Perez et al., 2012).
De molekylære mekanismene som ligger til grunn for de cytoarchitectural endringene i hjernen til løsningsmiddelbrukere er uklare. Imidlertid fant en nylig studie at cykloheksan fremmer overekspresjon av AP-endonuklease 1 (APE1) i hippocampus. Dette proteinet aktiverer den cellulære responsen på oksidativt stress og regulerer transkripsjonen av gener involvert i neuronal overlevelse og DNA-reparasjon (Campos-Ordonez et al., 2015). Dette antyder at cykloheksan forstyrrer redoksbalansen i celler og påvirker vevets evne til å avgifte ROS. Akkumuleringen av ROS forårsaker cellulær dysfunksjon ved å skade membraner, lipider, proteiner, mitokondrier og DNA. Imidlertid er det behov for ytterligere studier for å avklare ROSs rolle i cykloheksanindusert nevrodegenerasjon.
Den økende bruken av cykloheksan som en relativt sikker erstatning for benzen eller toluen i et mylder av kommersielle produkter, inkludert elektroniske sigaretter, nødvendiggjør en bedre forståelse av de biologiske effektene av dette løsningsmidlet. Innsikt i de cellulære og molekylære mekanismene for nevral degenerasjon indusert av cykloheksan vil bidra til å minimere den potensielle risikoen forbundet med forsettlig eller utilsiktet innånding av denne flyktige forbindelsen.
Forfatterbidrag
TC: Arbeid unnfangelse og manuskriptskriving. OG: Arbeidskonsept, manuskriptskriving og finansiering.
Erklæring om interessekonflikter
Forfatterne erklærer at forskningen ble utført i fravær av kommersielle eller økonomiske forhold som kunne tolkes som en potensiell interessekonflikt.
Anerkjennelser
Vi vil takke Red Tematica Neuro-Biopsicologia Básica y Aplicada (CONACYT 251132) for støtten.