WPROWADZENIE
Przewlekła niewydolność serca (CHF) jest ostatecznym skutkiem powszechnym w większości chorób serca. Z różnych powodów – starzejącej się populacji, zwiększonej przeżywalności wśród pacjentów z chorobami, takimi jak choroba wieńcowa czy nadciśnienie – częstość występowania CHF wzrosła. Farmakologiczne leczenie niewydolności serca posunęło się naprzód, a większość badań klinicznych wykazuje lepsze rokowanie, ale wpływ terapii farmakologicznej na ogólną populację pacjentów z CHF jest niewielki, a wskaźniki śmiertelności i chorobowości utrzymują się. badania obejmowały pacjentów z obniżoną frakcją wyrzutową lewej komory (LVEF) (dysfunkcja skurczowa), podczas gdy 30–50% pacjentów z CHF w badaniach populacyjnych3 i rejestrach szpitalnych4,5 zachowało LVEF. U tych pacjentów dopiero niedawno oceniono wpływ szeregu leków stosowanych w terapii CHF. Przewlekła niewydolność serca z zachowaną funkcją skurczową występuje częściej u starszych pacjentów i kobiet 3,6,7, co może częściowo wyjaśniać złe rokowanie. W ostatnich latach wiele uwagi poświęcono zarówno epidemiologicznym, jak i klinicznym aspektom problemu oraz jego leczeniu, a celem tego artykułu jest przegląd najważniejszych wyników w literaturze.
KONCEPCJA
Początkowo terminem używanym do klasyfikacji pacjentów z niewydolnością serca i prawidłową lub prawie normalną kurczliwością był „rozkurczowa niewydolność serca”. Jednak jest to obecnie uważane za kontrowersyjne i większość autorów preferuje „niewydolność serca z zachowaną funkcją skurczową”. W rutynowej praktyce klinicznej oba terminy reprezentują koncepcję, która prawdopodobnie identyfikuje tych samych pacjentów, chociaż ich rzeczywistość patofizjologiczna może się różnić. Rozpoznanie rozkurczowej niewydolności serca wymaga obecności klinicznego zespołu CHF wraz z obiektywnym wykazaniem izolowanej lub dominującej dysfunkcji rozkurczowej.8 Natomiast niewydolność serca z zachowaną funkcją skurczową rozpoznaje się u pacjentów z klinicznym zespołem CHF i prawidłową lub prawie prawidłową LVEF, bez konieczności wykazywania anomalii rozkurczowej. Biorąc pod uwagę niezliczone ograniczenia nieinwazyjnych badań (echokardiogram dopplerowski, ventriculografia izotopowa) funkcji rozkurczowej oraz szeroki zakres zmiennych parametrów obecnie stosowanych do ich ilościowego określenia (ilościowe określenie stanu serca związanego z wiekiem, obciążeniem wstępnym i następczym, częstość akcji serca, itp.), bardziej rozsądne wydaje się użycie terminu „CHF z zachowaną funkcją skurczową” bez nalegania na obiektywne wykazanie anomalii rozkurczowej. W rzeczywistości niektóre badania pokazują, że wśród pacjentów z CHF zdiagnozowaną zgodnie z kryteriami Framinghama i LVEF > 50%, którzy są poddawani badaniu hemodynamicznemu i echokardiogramowi dopplerowskiemu, 92% ma co najmniej jedną nieprawidłowość rozkurczową w badanie hemodynamiczne; 94% ma co najmniej jedną nieprawidłowość rozkurczową w badaniu dopplerowskim, a 100% co najmniej jedną nieprawidłowość rozkurczową zidentyfikowaną za pomocą jednej lub drugiej z tych metod.9 W konsekwencji badanie funkcji rozkurczowej służy raczej do potwierdzenia diagnozy rozkurczowej CHF niż jej ustalenia .
KRYTERIA DIAGNOSTYCZNE
Podsumujemy teraz ewolucję diagnozy rozkurczowej CHF. Grupa Badawcza Europejskiego Towarzystwa Kardiologicznego ds. Rozkurczowej Niewydolności Serca zaproponowała 3 obowiązkowe kryteria, które powinny występować jednocześnie10: 1) obecność objawów przedmiotowych i podmiotowych CHF; 2) obecność prawidłowej lub tylko nieznacznie nieprawidłowej funkcji skurczowej lewej komory oraz 3) oznaki nieprawidłowego zwiotczenia lewej komory, wypełnienia, rozszerzalności rozkurczowej lub sztywności rozkurczowej. Kryteria te spotkały się z krytyką. Po pierwsze, klinicznej diagnozie CHF (poprzez objawy przedmiotowe i podmiotowe) brakuje czułości i swoistości, co najwyraźniej sprawia, że kluczowe znaczenie ma spełnienie kryteriów Framingham (tabela 1) lub jakiejkolwiek innej równie potwierdzonej klasyfikacji. Po drugie, limit „normalnej” LVEF był bardzo zróżnicowany (40% -50%); Europejska Grupa Badawcza wybrała 45%, ale można argumentować, że frakcja wyrzutowa w zakresie 40% -50% może być uznana za normalną. Ponadto frakcja wyrzutowa może się zmieniać w zależności od tego, kiedy zostanie określona. Na przykład w przypadku niewydolności serca wtórnej do ostrego przemijającego niedokrwienia mięśnia sercowego lub przełomu nadciśnieniowego LVEF określona w pierwszych godzinach można zmniejszyć, ale po 24 godzinach jest ona normalna. Badania pokazują, że u pacjentów z niewydolnością serca i niekontrolowanym nadciśnieniem tętniczym różnice między LVEF oznaczoną na oddziale ratunkowym a LVEF mierzoną po 72 godzinach nie były istotne u tych pacjentów, którzy byli już stabilni klinicznie11. dekompensacja, ponieważ wartości uzyskane w kolejnych dniach są wiarygodne; jedynym wyjątkiem od tej reguły mogą być chorzy z ostrym niedokrwieniem.Trzecia krytyka kryteriów europejskich jest związana z małą rzetelnością, czułością i swoistością oznaczania nieprawidłowości funkcji rozkurczowej, o czym była mowa wcześniej.
Vasan i Levy12 stosują 2 rodzaje kryteriów, aby podzielić diagnozy rozkurczowej CHF na 3 kategorie: ostateczne, prawdopodobne i możliwe (Tabela 2). Kliniczne zastosowanie tych kryteriów jest ograniczone ze względu na ich złożoność oraz fakt, że oba typy są empiryczne i wymagają dających się wykazać nieprawidłowości w funkcji rozkurczowej. W konsekwencji, jak wspomniano wcześniej, większość autorów obecnie unika potrzeby badania funkcji rozkurczowej i definiuje jako rozkurczowe przypadki CHF kliniczne kryteria niewydolności serca i LVEF > 50% lub > 45% 9. Nawet w CHF z zachowaną składową funkcji skurczowej w badaniach CHARM (Candesartan in Heart failure: Assessment of Reduction in Mortality and zachorowalność) kryterium frakcji wyrzutowej zostało zredukowane do 40% .13

METODY DIAGNOSTYCZNE
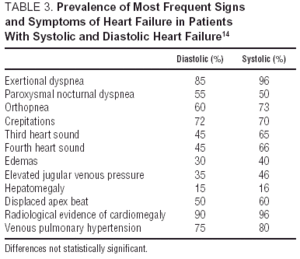
Diagnostyczne wykorzystanie izolowanych objawów a kliniczne objawy niewydolności serca są ograniczone i ustępują, gdy są pogrupowane zgodnie z kryteriami Framingham. Jednak wiarygodność tych objawów i objawów w odróżnieniu skurczowej CHF od rozkurczowej jest słaba (tab. 3). McDermott i wsp.14 nie stwierdzili istotnych różnic w częstości występowania objawów podmiotowych, przedmiotowych lub danych radiologicznych między pacjentami z LVEF 50%. Wbrew oczekiwaniom nie rozróżniono nawet radiologicznych dowodów kardiomegalii. Podobnie elektrokardiogramy nie pozwalają na rozróżnienie między CHF z zachowaną lub obniżoną funkcją skurczową, chociaż normalny elektrokardiogram sprawia, że rozpoznanie niewydolności serca jest mało prawdopodobne. Dlatego też, gdy kryteria kliniczne wskazują na podejrzenie niewydolności serca, konieczne jest wykonanie echokardiografii dopplerowskiej lub alternatywne badanie czynności komory (ventriculografia izotopowa) w celu precyzyjnego określenia frakcji wyrzutowej. Ponadto echokardiografia dostarcza informacji o występowaniu lub braku przerostu lewej komory i może wskazywać na funkcję rozkurczową (chociaż, jak wspomniano wcześniej, nie jest to niezbędne do rozpoznania CHF z zachowaną funkcją skurczową). Badanie hemodynamiczne, „złoty standard” w diagnostyce rozkurczowej CHF, jest zarezerwowane dla określonych przypadków lub gdy istnieją inne wskazania. W przyszłości nowe techniki, takie jak rezonans magnetyczny serca, mogą odgrywać ważną rolę w ocenie anatomii i czynności serca (chociaż obecnie ich zastosowanie jest ograniczone z powodu braku dostępności).
W ostatnich latach oznaczanie peptydów natriuretycznych w mózgu (BNP i NT-proBNP ) stało się bardzo ważne w diagnostyce CHF15. U pacjentów z dysfunkcją rozkurczową stężenia BNP są wysokie, chociaż niektóre badania wskazują, że poziomy peptydów są wyższe u pacjentów z dysfunkcją skurczową oraz pacjentów z mieszaną dysfunkcją skurczową i rozkurczową. Poziomy BNP korelują z nieprawidłowościami wskaźników funkcji rozkurczowej. Inne badania wskazują, że diagnostyczne poziomy BNP są podobne w rozkurczowej CHF i skurczowej CHF16. Ostatnio Bay i wsp17 odkryli, że izolowane oznaczenie NT-proBNP u pacjentów z CHF przy przyjęciu pozwala rozróżnić pacjentów z LVEF > 40% i
Podsumowując wydaje się, że określenie poziomu peptydów natriuretycznych w mózgu może odegrać ważną rolę w przyszłości w badaniu CHF z zachowaną funkcją skurczową. Jest to już oceniane w badaniach klinicznych (I-Preserve).
PROGNOZA
Chociaż tradycyjnie uważano, że rokowanie w CHF było ściśle powiązane z frakcją wyrzutową i że śmiertelność u pacjentów z CHF a obniżona funkcja skurczowa była znacznie większa, co zostało zakwestionowane w wielu ostatnich badaniach. W klasycznym badaniu Senni 3 – 6-letnie przeżycie nie różniło się istotnie między pacjentami z CHF i LVEF 50%, a od 60% do 70% wszystkich pacjentów zmarło w tym okresie. W obu przypadkach przeżycie było znacznie niższe niż oczekiwano w populacji ogólnej w tym samym wieku i tej samej płci (P18 i w naszej własnej grupie5. Varela-Román i wsp. Stwierdzili, że śmiertelność 5-letnia wynosiła 54% u pacjentów z dysfunkcją skurczową i 44% pacjentów z zachowaną LVEF (różnica nieistotna). W naszym badaniu śmiertelność 3-letnia wyniosła 49% u pacjentów z CHF i LVEF 45% (P = 0,19, nieistotna). Wskaźniki ponownych przyjęć były również podobne w obu grupach (48% i 50 Zarówno Permanyer-Miralda i wsp.19, jak i nasze własne badanie5 stwierdzili, że LVEF nie jest niezależnym predyktorem śmiertelności, a czynniki takie jak wiek lub choroby współistniejące mają większe znaczenie dla rokowania.
Wszystkie te dane wydają się wskazywać, że rokowanie w CHF z zachowaną funkcją skurczową jest nieco mniej złowieszcze niż w przypadku CHF z obniżoną funkcją skurczową. Roczna śmiertelność chorych z rozkurczową CHF wynosi 5–8% w porównaniu z 10–15% wśród chorych ze skurczową CHF.8 Śmiertelność w populacji ogólnej bez CHF i w podobnym wieku wynosi 1% rocznie. Obecność choroby wieńcowej, wiek i wartość graniczna LVEF są ważnymi czynnikami rokowania. Po wykluczeniu pacjentów z chorobą niedokrwienną serca roczna śmiertelność z powodu rozkurczowej CHF spada do 2% -3% .20 U pacjentów > 70 lat z CHF śmiertelność jest bardzo podobna, niezależnie od LVEF .21
Jednak w innych badaniach stwierdzono, że śmiertelność i wskaźniki ponownej hospitalizacji są znacznie wyższe u pacjentów z zachowaną lub obniżoną LVEF.22 W Hiszpanii Martínez-Sellés i wsp23 odkryli ostatnio związek między płcią a LVEF w odniesieniu do rokowania . U kobiet z CHF przeżycie nie różni się w odniesieniu do LVEF, ale jest znacznie niższe u mężczyzn z LVEF 30%, ale lepsze u kobiet, gdy LVEF wynosi 40%, miało zaskakująco niski współczynnik śmiertelności, niższy niż u pacjentów z LVEF 13. zmienność obserwowana w badaniach może być związana z różnymi profilami klinicznymi pacjentów, metodami i wartościami odcięcia używanymi do określenia czynności komór oraz różnymi zastosowanymi projektami badawczymi.5 Ponadto pacjenci ze skurczową CHF są zwykle leczeni z większym odsetkiem leki o korzystnym działaniu prognostycznym, takie jak inhibitory ACE, spironolakton i beta-blokery.5,13,18
LECZENIE
Do tej pory tylko jedno monitorowane randomizowane badanie kliniczne na dużą skalę miało miało miejsce w celu porównania leku z podawaniem placebo u pacjentów z CHF i zachowaną czynnością skurczową („zachowany” składnik badania CHARM) .13 W tym badaniu porównano skuteczność dawki 32 mg kandesartanu na dobę z placebo w 3023 pacjentów z CHF i LVEF > 40%. Po średnim okresie obserwacji wynoszącym 36,6 miesiąca, pierwotna łączna częstość występowania (zgon z przyczyn sercowo-naczyniowych lub przyjęcie z powodu CHF) była podobna w obu grupach, z tendencją na korzyść kandesartanu kosztem znacznego zmniejszenia liczby przyjęć z powodu CHF (16% ; P = 0,047). Dane dotyczące śmiertelności z przyczyn sercowo-naczyniowych były bardzo podobne. Roczne wskaźniki śmiertelności i incydentów sercowo-naczyniowych spadły, jak wspomniano wcześniej, a roczna częstość zgonów z przyczyn sercowo-naczyniowych lub przyjęć z powodu CHF wynosiła tylko 8,1% w grupie kandesartanu i 9,1% w grupie placebo, co budzi wątpliwości co do możliwości zastosowania tych wyników do populacji pacjentów z większym ryzykiem wystąpienia zdarzeń.5,18
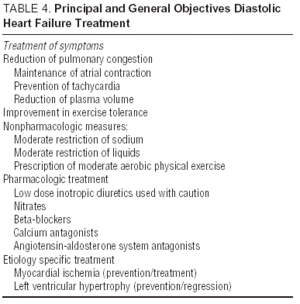
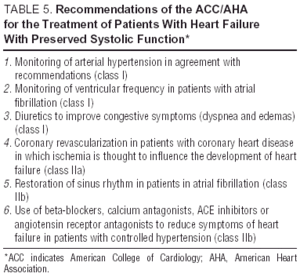
Inne badania nad antagonistami receptora angiotensyny (badanie I-Preserve irbesartanu), inhibitorami ACE (badanie PEP-CHF dotyczące peryndoprylu) lub beta-blokerami są obecnie w toku. Liczba zapisanych pacjentów i długa obserwacja sprawiają, że I-Preserve jest najważniejszym z nich. To badanie porównuje skuteczność irbesartanu w dawce 300 mg / dobę z placebo u 3600 pacjentów z CHF i LVEF > 45% 24. Do czasu udostępnienia danych z randomizowanych badań klinicznych leczenie rozkurczowej CHF lub CHF z zachowaną funkcją skurczową jest po prostu objawowe i etiologiczne, chociaż nie można ignorować korzyści ze stosowania kandesartanu w zmniejszaniu liczby ponownych hospitalizacji wykazanych w badaniu CHARM13. Wytyczne i ogólne cele leczenia rozkurczowej CHF przedstawiono w Tabeli 4. Europejskie i północnoamerykańskie wytyczne dotyczące leczenia CHF koncentrują się na czynnikach podanych w Tabeli 5.25,26 Monitorowanie ciśnienia krwi i częstotliwości komór jest ważne, podobnie jak regresja przerostu lewej komory i monitorowanie mięśnia sercowego niedokrwienie. W konsekwencji zalecane leki mogą być takie same, jak te podawane w przypadku dysfunkcji skurczowej, mimo że patofizjologiczne cele ich stosowania są różne. Badania wykazały, że beta-blokery, antagoniści wapnia i antagoniści angiotensyny wpływają pozytywnie na objawy i wydolność funkcjonalną pacjentów z rozkurczową niewydolnością serca.27,28 Wpływ naparstnicy na pacjentów z rytmem zatokowym jest wątpliwy; w przypadkach niedokrwienia może być ujemne i powodować przeciążenie wapniem podczas rozkurczu, chociaż w badaniu DIG pacjenci z LVEF > 45%, którym podano naparstnicę, miało mniej przyjęć i mniej objawów niż ci, którzy nie były 27,28. Diuretyki są ważne w celu zmniejszenia przekrwienia i złagodzenia objawów, ale należy je stosować ostrożnie iw małych dawkach, aby uniknąć niedociśnienia i innych objawów niskiego rzutu serca. Wskazania do leczenia przeciwzakrzepowego i podawania leków przeciwpłytkowych są takie same, jak u pacjentów ze skurczową CHF.26
W brak nowych wyników z bieżących badań klinicznych i zgodnie z wytycznymi (tabele 4 i 5), skojarzenie leków moczopędnych, leków hipotensyjnych „bradykardizujących” (beta-blokery lub antagoniści wapnia) i antagonistów angiotensyny wydaje się najlepszą strategią farmakologiczną u tych pacjentów26-28 razem z identyfikacją i prawidłowym leczeniem podstawowych procesów (z których najczęstszymi są niedokrwienie mięśnia sercowego i nadciśnienie).
Sekcja sponsorowana przez Laboratorio Dr Esteve