Streptococci to duża grupa Gram-dodatnich, niemotylowych, nie tworzących przetrwalników ziarniaków około 0,5 Rozmiar -1,2 µm. Często rosną parami lub łańcuchami i są negatywne dla oksydazy i katalazy.
Pyogenes ma tendencję do kolonizowania górnych dróg oddechowych i jest wysoce zjadliwy, ponieważ pokonuje system obronny żywiciela. Najczęstsze postacie choroby S. pyogenes obejmują infekcje dróg oddechowych i skóry, a za każdą z nich odpowiadają zwykle różne szczepy.
Ściana komórkowa S. pyogenes jest bardzo złożona i zróżnicowana chemicznie. Antygenowe składniki komórki są czynnikami wirulencji. Zewnątrzkomórkowe składniki odpowiedzialne za proces chorobowy obejmują inwazyny i egzotoksyny. Najbardziej zewnętrzna kapsułka składa się z kwasu hialuronowego, który ma strukturę chemiczną przypominającą tkankę łączną gospodarza, co pozwala bakterii na uniknięcie rozpoznania przez gospodarza jako czynnika urażającego. W ten sposób bakteria unika fagocytozy przez neutrofile lub makrofagi, umożliwiając jej kolonizację. Kwas lipotejchojowy i białka M znajdujące się na błonie komórkowej przechodzą przez ścianę komórkową i wystają na zewnątrz torebki.
Inwazja komórek nabłonka
Charakterystyka S. pyogenes to zdolność organizmu do inwazji komórek nabłonka. Coraz częściej donoszono o niepowodzeniu penicyliny w zwalczaniu S. pyogenes z gardła pacjentów, zwłaszcza nosicieli S. pyogenes. Wyniki jednego z badań silnie sugerują, że jeśli stan nosicielstwa wynika z przeżycia wewnątrznabłonkowych paciorkowców, niepowodzenie penicyliny w zabijaniu spożytych S pyogenów może być związane z brakiem skutecznego wnikania penicyliny do komórek nabłonka. Obserwacje te mogą mieć implikacje kliniczne dla zrozumienia nosicieli i zarządzania infekcją S. pyogenes.
Bakteryjne czynniki wirulencji
Antygeny ściany komórkowej obejmują polisacharyd otoczkowy (substancja C ), peptydoglikan i kwas lipotejchojowy (LTA), białka R i T oraz różne białka powierzchniowe, w tym białko M, białka fimbrii, białka wiążące fibronektynę (np. białko F) i streptokinaza związana z komórką.
Substancja C składa się z rozgałęzionego polimeru L-ramnozy i N-acetylo-D-glukozaminy. Może odgrywać rolę w zwiększonej zdolności inwazyjnej. Białka R i T są używane jako markery epidemiologiczne i nie odgrywają żadnej znanej roli w wirulencji.
Inny czynnik wirulencji, peptydaza C5A, niszczy sygnały chemotaktyczne przez rozszczepienie składnika dopełniacza C5A.
Białko M, głównym czynnikiem zjadliwości jest makrocząsteczka wbudowana w fimbrie obecne na błonie komórkowej wystającej na ścianę komórkową bakterii. Jest to główna przyczyna przesunięcia antygenowego i dryfu antygenowego wśród GAS. (Zobacz obrazek poniżej.)
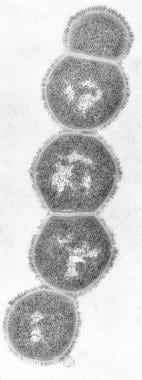 Infekcje Streptococcus grupy A. Białko M.
Infekcje Streptococcus grupy A. Białko M. Białko M wiąże fibrynogen gospodarza i blokuje wiązanie dopełniacza z leżącym u jego podstaw peptydoglikanem. Pozwala to na przetrwanie organizmu poprzez hamowanie fagocytozy. Szczepy zawierające duże ilości białka M są odporne na fagocytozę, szybko namnażają się w tkankach ludzkich i inicjują proces chorobowy. Po ostrej infekcji w niektórych przypadkach rozwijają się przeciwciała specyficzne dla typu M.
Jednakże, chociaż takie przeciwciała chronią przed zakażeniem homologicznym typem białka M, nie nadają odporność na inne typy M. Ta obserwacja jest jednym z czynników stanowiących główną teoretyczną przeszkodę w opracowaniu szczepionki S. pyogenes, ponieważ do tej pory opisano ponad 80 serotypów M.
Ogniska zachorowań na społeczność określone choroby paciorkowcowe są zwykle związane z niektórymi typami M. dlatego też serotypowanie M było bardzo cenne w badaniach epidemiologicznych.
Bakteryjne czynniki przylegania
Sugerowano, że co najmniej 11 różnych składników powierzchniowych GAS odgrywa rolę rola w adhezji. W 1997 roku Hasty i Courtney zaproponowali, by GAS wyrażał różne macierze adhezyn w różnych niszach środowiskowych. Na podstawie ich przeglądu, białko M pośredniczy w adhezji do komórek HEp-2, ale nie do komórek policzkowych u ludzi, podczas gdy FBP54 pośredniczy w adhezji do komórek policzkowych, ale nie do komórek HEp-2. Białko F pośredniczy w adhezji do komórek Langerhansa, ale nie do keratynocytów.
Jedną z teorii proponowanych w odniesieniu do procesu adhezji jest model dwuetapowy. Początkowy krok w przezwyciężaniu elektrostatycznego odpychania bakterii od żywiciela odbywa się za pośrednictwem LTA, która zapewnia słabą, odwracalną adhezję. Drugi etap przybiera formę trwałej, nieodwracalnej adhezji, w której pośredniczą między innymi specyficzne dla tkanki białko M, białko F lub FBP54.Po przyleganiu paciorkowce są odporne na fagocytozę, namnażają się i zaczynają atakować miejscowe tkanki.
GAS wykazuje ogromną i ewoluującą różnorodność molekularną, napędzaną poziomą transmisją między różnymi szczepami. Dotyczy to również porównania z innymi paciorkowcami. Nabycie proroków stanowi znaczną część różnorodności, nadając nie tylko zjadliwość poprzez czynniki wirulencji związane z fagami, ale także zwiększoną przeżywalność bakterii przeciwko obronie gospodarza.
Produkty pozakomórkowe i toksyny
Różne produkty wzrostu zewnątrzkomórkowego i toksyny wytwarzane przez GAS są odpowiedzialne za uszkodzenie komórek gospodarza i odpowiedź zapalną.
Hemolizyny
S pyogenes opracowuje 2 różne hemolizyny. Białka te są odpowiedzialne za strefę hemolizy obserwowaną na płytkach agarowych z krwią, a także są ważne w patogenezie uszkodzenia tkanki u zakażonego żywiciela. Streptolizyna O jest toksyczna dla wielu różnych typów komórek, w tym mięśnia sercowego, i jest wysoce immunogenna. Określenie odpowiedzi przeciwciał na to białko (miano antystreptolizyny O) jest często przydatne w diagnostyce serologicznej niedawnej infekcji.
Streptolizyna S jest kolejnym czynnikiem zjadliwości zdolnym do uszkodzenia leukocytów polimorfojądrowych i organelle subkomórkowe. Jednak w przeciwieństwie do streptolizyny O, nie wydaje się być immunogenny.
Pirogenne egzotoksyny
Rodzina paciorkowców pirogenne egzotoksyny (SPE) obejmują SPE A, B, C i F. Te toksyny są odpowiedzialne za wysypkę szkarlatyny. Inne skutki chorobotwórcze powodowane przez te substancje obejmują pirogenność, cytotoksyczność i zwiększenie wrażliwości na endotoksyny. SPE B jest prekursorem proteazy cysteinowej, innego wyznacznika zjadliwości.
Grupa A izolaty paciorkowców związane ze streptokokowym TSS kodują pewne SPE (tj. A, C, F) zdolne do funkcjonowania jako superantygeny. Te antygeny wywołują wyraźną odpowiedź gorączkową, indukują proliferację limfocytów T oraz indukują syntezę i uwalnianie wielu cytokin, w tym czynnika martwicy nowotworu, interleukiny-1 beta i interleukiny-6. Tę aktywność przypisuje się zdolności superantygenu do jednoczesnego wiązania się z regionem V-beta receptora komórek T oraz z głównymi antygenami zgodności tkankowej klasy II komórek jednojądrzastych prezentujących antygen, co skutkuje rozległą, niespecyficzną proliferacją komórek T i zwiększoną produkcja interleukiny-2.
Nukleazy
Cztery odrębne antygenowo nukleazy (A, B, C, D) pomagają w upłynnienie ropy i pomóc w wytworzeniu substratu do wzrostu.
Inne produkty
Inne produkty zewnątrzkomórkowe obejmują NADazę (leukotoksyczną) , hialuronidaza (która trawi tkankę łączną gospodarza, kwas hialuronowy i własną torebkę organizmu), streptokinazy (proteolityczne) i streptodornaza AD (aktywność deoksyrybonukleazy).
Proteinaza, amylaza i esteraza to dodatkowe czynniki wirulencji paciorkowców, chociaż rola tych białek w patogenezie nie jest w pełni poznana.
Suppur Spektrum chorób atywnych
Paciorkowcowe zapalenie gardła
S pyogenes jest przyczyną do 15-30% przypadków ostrego zapalenia gardła. Choroba Franka występuje na podstawie stopnia zjadliwości bakterii po kolonizacji górnych dróg oddechowych. Dokładna diagnoza jest niezbędna do odpowiedniego doboru antybiotyku.
Liszajec
Piodermia jest najpowszechniejszą formą infekcji skóry wywołanej przez GAS . Nazywany również liszajem paciorkowcowym lub liszajem zakaźnym, występuje najczęściej w klimacie tropikalnym, ale może być również bardzo rozpowszechniony w klimatach północnych, szczególnie w miesiącach letnich. Czynniki ryzyka predysponujące do tej infekcji obejmują niski status społeczno-ekonomiczny; niski poziom higieny ogólnej; oraz miejscowe uszkodzenie skóry spowodowane ukąszeniami owadów, świerzbem, atopowym zapaleniem skóry i drobnymi urazami. Kolonizacja nienaruszonej skóry poprzedza rozwój piodermii o około 10 dni.
Piodermia paciorkowcowa może wystąpić u dzieci należących do pewnych grup ludności oraz w przeludnionych instytucjach. Sposoby przenoszenia to bezpośredni kontakt, zanieczyszczenie środowiska i muchy domowe. Szczepy paciorkowców wywołujące piodermię różnią się od tych, które powodują wysiękowe zapalenie migdałków.
Toksyny bakteryjne powodują proteolizę warstw naskórka i podnaskórkowego, umożliwiając bakteriom szybkie rozprzestrzenianie się wzdłuż warstw skóry i tym samym powodować pęcherze lub ropne zmiany. Inną częstą przyczyną liszajca jest Staphylococcus aureus.
Zapalenie płuc
Inwazyjny GAS może powodować infekcję płuc, często z szybkim postępem na martwicze zapalenie płuc.
Martwicze zapalenie powięzi
Martwicze zapalenie powięzi jest spowodowane inwazją bakterii do tkanki podskórnej, która następnie rozprzestrzenia się przez powierzchowną i głęboką powięź samoloty. W rozprzestrzenianiu się GAS pomagają bakteryjne toksyny i enzymy (np. Lipaza, hialuronidaza, kolagenaza, streptokinaza), interakcje między organizmami (infekcje synergistyczne), miejscowe czynniki tkankowe (np. Zmniejszona dopływ krwi i tlenu) oraz ogólne czynniki gospodarza (np. , stan upośledzenia odporności, przewlekła choroba, zabieg chirurgiczny).
W miarę jak infekcja rozprzestrzenia się w głąb powięzi, dochodzi do okluzji naczyń, niedokrwienia tkanek i martwicy. Chociaż GAS jest często izolowany w przypadkach martwiczego zapalenia powięzi, ten stan chorobowy jest często wywołany wieloma drobnoustrojami.
Zapalenie ucha środkowego i zapalenie zatok
Są to częste ropne powikłania paciorkowcowego zapalenia migdałków gardła. Są spowodowane rozprzestrzenianiem się organizmów przez trąbkę Eustachiusza (zapalenie ucha środkowego) lub przez bezpośrednie rozprzestrzenianie się do zatok (zapalenie zatok).
Spektrum chorób nieuleczalnych
Ostra gorączka reumatyczna
ARF jest opóźnionym, nieopuracyjnym następstwem zapalenia migdałków i gardła wywołanego GAS. Po zapaleniu gardła mija 2-3 tygodnie utajony okres, zanim pojawią się oznaki i objawy ARF. Choroba ma różne objawy kliniczne, w tym zapalenie stawów, zapalenie serca, pląsawicę, guzki podskórne i rumień brzeżny.
Gorączka reumatyczna może być wynikiem predyspozycji genetycznych gospodarza. Gen chorobowy może być przenoszony w sposób autosomalny dominujący lub autosomalny recesywny, z ograniczoną penetracją. Jednak gen choroby nie został jeszcze zidentyfikowany.
Znaczne dowody potwierdzają związek między infekcjami paciorkowcowymi grupy A w górnych drogach oddechowych a ARF, chociaż tylko niektóre serotypy z grupy M (tj. 1, 3, 5, 6, 18, 24) są związane z tą komplikacją. Bardzo śluzowate szczepy, szczególnie szczepy M typ 18, pojawiały się w wielu społecznościach przed pojawieniem się gorączki reumatycznej. Gorączkę reumatyczną obserwuje się najczęściej u dzieci w wieku 5-15 lat (grupa wiekowa najbardziej podatna na infekcje GAS).
Częstość występowania infekcji górnych dróg oddechowych wynosi około 3% dla osób z nieleczoną lub niewystarczająco leczoną infekcją. Okres utajony między zakażeniem GAS a wystąpieniem gorączki reumatycznej waha się od 2 do 4 tygodni. W przeciwieństwie do poststreptococcal glomerulonephritis (PSGN), które może następować po zapaleniu gardła lub piodermii paciorkowcowej, gorączka reumatyczna może wystąpić dopiero po zakażeniu górnych dróg oddechowych.
Pomimo głębokości zgromadzona wiedza na temat mikrobiologii molekularnej Streptococcus pyogenes, patogeneza ARF pozostaje nieznana. Według niektórych hipotez za patogenezę ARF może odpowiadać bezpośredni wpływ pozakomórkowej toksyny paciorkowcowej, w szczególności streptolizyny O. Obserwacje, że streptolizyna O jest kardiotoksyczna w modelach zwierzęcych, potwierdzają tę hipotezę, ale powiązanie tej toksyczności z uszkodzeniem zastawek obserwowanym w ARF było trudne.
Bardziej popularna hipoteza głosi, że nieprawidłowy odpowiedzialna jest odpowiedź immunologiczna gospodarza na niektóre składniki Streptococcus grupy A. Białko M GAS ma wspólne pewne sekwencje aminokwasowe z niektórymi ludzkimi tkankami i zostało to zaproponowane jako źródło reaktywności krzyżowej między organizmem a ludzkim gospodarzem, która może prowadzić do immunopatologicznej odpowiedzi immunologicznej. Stwierdzono również podobieństwo antygenowe między specyficznym dla grupy polisacharydem S pyogenes i glikoproteinami występującymi w ludzkich i bydlęcych zastawkach serca, a pacjenci z ARF mają przedłużone utrzymywanie się tych przeciwciał w porównaniu z grupą kontrolną z niepowikłanym zapaleniem gardła. Wydaje się, że inne antygeny GAS reagują krzyżowo z błonami sarkolemmy serca.
W trakcie odpowiedzi immunologicznej gospodarza na GAS, antygeny żywiciela mogą, w wyniku tej mimikry molekularnej, być mylone jako obce; prowadzi to do kaskady zapalnej, w wyniku której dochodzi do uszkodzenia tkanki. U pacjentów z ARF i pląsawicą Sydenhama, obecne są wspólne przeciwciała przeciwko antygenom znajdującym się w błonie komórkowej S pyogenes i jądrze ogoniastym mózgu, co dodatkowo potwierdza koncepcję nieprawidłowej odpowiedzi autoimmunologicznej w rozwoju ARF.
Zainteresowanie tym, czy takie odpowiedzi autoimmunologiczne odgrywają rolę w patogenezie zespołu znanego jako pediatryczne autoimmunologiczne zaburzenia neuropsychiatryczne związane z infekcjami paciorkowcowymi (PANDAS), było znaczne, chociaż konieczne są dalsze prace w celu ustalenia związku między zakażenia paciorkowcami i te zespoły.
Popreptokokowe zapalenie kłębuszków nerkowych
Kłębuszkowe zapalenie nerek może następować po zakażeniach paciorkowcowych grupy A gardła lub skóry, a częstość występowania różni się w zależności od występowanie tzw. nefrytogennych szczepów paciorkowców z grupy A w zbiorowisku. Typ 12 jest najczęstszym serotypem M, który powoduje PSGN po zapaleniu gardła, a typ M 49 jest serotypem najczęściej związanym z zapaleniem nerek związanym z piodermią. Okres utajony między zakażeniem GAS a wystąpieniem kłębuszkowego zapalenia nerek waha się od 1-2 tygodni.
Wydaje się, że patogeneza ma podłoże immunologiczne. Immunoglobuliny, składniki dopełniacza i antygeny, które reagują z surowicami odpornościowymi paciorkowców, są obecne w kłębuszkach nerkowych we wczesnym stadium choroby, a przeciwciała wywoływane przez paciorkowce nefrytogenne reagują z tkanką nerkową w taki sposób, aby sprzyjać uszkodzeniu kłębuszków nerkowych. W przeciwieństwie do ostrej gorączki reumatycznej, nawroty PSGN są rzadkie. Rozpoznanie PSGN opiera się na historii choroby, wynikach badań fizykalnych i potwierdzających dowodach niedawnej infekcji paciorkowcami.
Zespół wstrząsu toksycznego
Ciężkie infekcje GAS związane ze wstrząsem i niewydolnością narządów zgłaszano z coraz większą częstością, głównie w Ameryce Północnej i Europie.
Występuje znaczne nakładanie się paciorkowcowych TSS i martwiczego zapalenia powięzi wywołanego przez paciorkowce, o ile większość przypadków występuje w związku z zakażeniami tkanek miękkich. Jednak paciorkowcowe TSS mogą również występować w połączeniu z innymi ogniskowymi infekcjami paciorkowcowymi, w tym infekcją gardła.
Wydaje się, że patogeneza streptokokowego TSS jest częściowo związana ze zdolnością pewnych ( tj. A, C, F) paciorkowcowe egzotoksyny ropotwórcze (SPE), które działają jako superantygeny.
Szkarłatna gorączka
Kiedy delikatna, rozproszona rumieniowa wysypka występuje w przebiegu ostrego paciorkowcowego zapalenia gardła, choroba ta nazywana jest szkarlatyną. Wysypka szkarlatyny jest spowodowana pirogennymi egzotoksynami (tj. SPE A, B, C i F). Wysypka w dużym stopniu zależy od ekspresji toksyn; istniejąca wcześniej odporność humoralna na specyficzną toksynę SPE zapobiega klinicznym objawom szkarlatyny.
Szkarłatna gorączka stała się mniej powszechna i mniej zjadliwa niż w ostatnich dziesięcioleciach; jednak zachorowalność jest cykliczna, w zależności od częstości występowania szczepów wytwarzających toksyny i statusu odpornościowego populacji. Sposoby przenoszenia, wiek zachorowań i inne cechy epidemiologiczne są podobne do tych dla paciorkowcowego zapalenia gardła.
Choroby ośrodkowego układu nerwowego
Główne dowody na postreptokokową autoimmunologiczną chorobę ośrodkowego układu nerwowego (OUN) potwierdzają badania pląsawicy Sydenhama, neurologicznej manifestacji gorączki reumatycznej. Doniesienia o zaburzeniach obsesyjno-kompulsywnych (ZO-K), tikach i innych objawach neuropsychiatrycznych występujących w związku z zakażeniami paciorkowcami beta-hemolitycznymi grupy A sugerują, że autoimmunizacja poposiłkowa może wywołać różne następstwa OUN.