US Pharm. 2013; 38 (11) (suplement onkologiczny): 3-6.
STRESZCZENIE: Niedokrwistość jest częstym powikłaniem u pacjentów z rakiem. Przyczyną może być sam guz lub zastosowany schemat chemioterapii. Ciężkość i częstość występowania tego schorzenia różni się w zależności od wielu czynników. Leczenie ma na celu zwiększenie zdolności krwi do przenoszenia tlenu, zmniejszenie zmęczenia i poprawę ogólnej jakości życia pacjenta. Zalecano stosowanie leków stymulujących erytropoezę, suplementację żelaza i transfuzję krwinek czerwonych w różnych warunkach. Chociaż okazało się to korzystne u niektórych pacjentów, optymalna metoda terapeutyczna nie została jeszcze ustalona.
Niedokrwistość jest główną przyczyną zachorowalności u pacjentów z rakiem, związanej ze słabą wydajnością fizyczną, rokowaniem i wynikami leczenia.1 Według Światowej Organizacji Zdrowia ( WHO), anemię definiuje się jako poziom hemoglobiny (Hb) < 12 g / dl u kobiet niebędących w ciąży i < 13 g / dl u mężczyzn w wieku ≥15 lat.2
Epidemiologia
Niedokrwistość jest jednym z najczęstszych objawów u pacjentów chorych na raka. W rzeczywistości wykazano, że od 30% do 90% pacjentów z wszystkimi nowotworami ma anemię, co jest liczbą zależną od rodzaju raka i zastosowanej definicji niedokrwistości.3 Częstość występowania i ciężkość niedokrwistości zależą od wielu czynników: które są wymienione w TABELI 1.4,5

Etiologia
Główna przyczyna niedokrwistości u pacjentów z rakiem jest dwojaka: sam nowotwór i terapia stosowana w leczeniu raka. Komórki rakowe, które naciekają szpik kostny, mogą bezpośrednio hamować hemopoezę i powodować anemię. Ponadto komórki rakowe uwalniają cytokiny, które mogą prowadzić do sekwestracji żelaza, zmniejszając produkcję czerwonych krwinek (RBC). Nowotwory mogą powodować przewlekłą utratę krwi w miejscu guza, co prowadzi do postępującej anemii z powodu raka i uszkodzenia narządów.6
Problem ten jest potęgowany przez utratę krwi, niedobory żywieniowe, hemolizę, zaburzenia endokrynologiczne, choroby dziedziczne, niewydolność nerek lub obecność cytokin zapalnych związanych z rakiem i chorobami przewlekłymi.4,6 Chorzy na raka mają tendencję do utraty apetytu, co prowadzi do niedoborów żywieniowych. U pacjentów z guzami przewodu pokarmowego (GI) do niedoborów prowadzi również nieprawidłowe wchłanianie składników odżywczych. Hemoliza jest następstwem zmian w zdolności krzepnięcia przeciwciał o podłożu immunologicznym. W rezultacie niedokrwistość jest częstą chorobą współistniejącą u pacjentów, u których niedawno zdiagnozowano raka. Prawie połowa pacjentów, u których zdiagnozowano raka ginekologicznego i jedna trzecia pacjentów, u których zdiagnozowano chłoniaka nieziarniczego, ma niedokrwistość w momencie rozpoznania.
Ponadto mielosupresja jest jednym z efektów ubocznych chemioterapii i istotnym czynnikiem przyczyniającym się do anemii . W szczególności radioterapia szkieletu powoduje również toksyczność hematologiczną, a tym samym anemię.6
Objawy
Najczęstszymi objawami niedokrwistości są zmęczenie, duszność wysiłkowa, kołatanie serca, depresja, niewydolność serca, zaburzenia funkcji poznawczych funkcji, zawrotów głowy i niewydolności serca.7,8
Diagnoza
Wielkość problemu niedokrwistości u pacjentów z rakiem jest wzmacniana przez suboptymalne pomiary diagnostyczne, brak standardowej definicji oraz fakt, że przyczyna jest często wieloczynnikowa.6,9 Należy zebrać szczegółowy wywiad dotyczący czasu trwania i czasu do wystąpienia objawów, obecności chorób współistniejących, wywiadu rodzinnego oraz historii narażenia na leki przeciwnowotworowe i promieniowanie. Należy przeprowadzić badanie fizykalne w celu wykrycia omdleń, duszności wysiłkowej, bólu głowy, zawrotów głowy, bólu w klatce piersiowej, zmęczenia, nieprawidłowych miesiączek u kobiet i blad.6
National Cancer Comprehensive Network zaleca, aby u pacjentów z Hb < 11 g / dl lub zmniejszenie liczby HB o 2 g / dl. Jest to przydatne w określaniu, czy obecne są cytopenie. Zalecany jest również wizualny przegląd rozmazu krwi obwodowej w celu potwierdzenia wielkości, kształtu i koloru czerwonych krwinek.6
Patofizjologia
Niedokrwistość jest wynikiem połączenia zmniejszonej liczby krążących erytrocytów , zmniejszona objętość upakowanych komórek i obniżony poziom Hb.6 Może to nastąpić poprzez różne mechanizmy patofizjologiczne, w tym nadmierną utratę krwi, zwiększoną destrukcję erytropoezy i zmniejszoną erytropoezę. żelazo jest niezbędne dla erytropoezy. Erytropoetyna kontroluje nasycenie, różnicowanie i przeżycie komórek erytroidalnych podczas tego procesu.10 EPO jest wytwarzana głównie przez nerki i transportowana do szpiku kostnego.11
Nieprawidłowy metabolizm żelaza lub zatrzymywanie żelaza w makrofagach zmniejsza ilość żelazo, które jest dostępne dla erytropoezy.Zmieniony metabolizm żelaza jest spowodowany głównie przez hepcydynę, białko, które zmniejsza wchłanianie żelaza w jelitach, a także uwalnianie żelaza przez makrofagi. Wytwarzanie hepcydyny jest zwiększane przez cytokiny uwalniane z guzów, zmniejszając w ten sposób ilość krążącego żelaza. Wykazano również, że niektóre schematy chemioterapeutyczne zwiększają produkcję cytokin, takich jak interleukina (IL) -6. 5 Powtarzane cykle chemioterapii mogą nasilać kumulatywne zmniejszenie erytropoezy7.
W miarę zmniejszania się dostarczania tlenu, komórki tkanki organizmu stają się niedotlenione, co skutkuje serią reakcji fizjologicznych, gdy organizm próbuje uzyskać lub utrzymać utlenowanie tkanek.
Uważa się, że normalne wykorzystanie u pacjentów z najadaczem żelaza może zostać przerwane przez interakcję między komórkami nowotworowymi i własny układ odpornościowy gospodarza. Ta interakcja prowadzi do regulacji w górę określonych cytokin prozapalnych, takich jak IL-1, gamainterferon i czynnik martwicy nowotworu alfa (TNF-α), co zmniejsza zróżnicowanie prekursorów erytroidów w szpiku kostnym, zaburza normalne wykorzystanie żelaza i hamuje normalną hipoksję. produkcja napędzanaerytropoetyny. Nefrotoksyczne chemioterapeutyki mogą pogorszyć problem, powodując zaburzenia czynności nerek.
W przypadku przewlekłej niedokrwistości guzy uwalniają czynnik wywołujący ananemię, cząsteczkę, która skraca żywotność erytrocytów. Zaostrza to anemię do tego stopnia, że erytropoie nie mogą zrekompensować gorszego przeżycia czerwonych krwinek.12
Czynniki ryzyka anemii w raku
Zidentyfikowano następujące czynniki ryzyka niedokrwistości w raku9:
- Mielosupresyjna chemioterapia lub radioterapia
- Niskie poziomy Hb (10-12 g / dl) na początku chemioterapii cytotoksycznej
- Podawanie platyny zawierające schematy, co również zwiększa potrzebę wspomagania transfuzji.
Leczenie
Oprócz ogólnej poprawy jakości życia pacjenta, leczenie niedokrwistości jest niezbędne dla wielu Niedokrwistość utrudnia dostarczanie dostatecznej ilości tlenu do wszystkich komórek, w tym komórek nowotworowych.7 Ponieważ niskie natlenienie tkanek wiąże się ze zmniejszoną wrażliwością nowotworów na promieniowanie i inne formy chemioterapii, skuteczność tych metod leczenia jest zmniejszona w przypadku niedokrwistości.13,14
Celem terapii powinno być zwiększenie przenoszenia tlenu g pojemność krwi i leczyć przyczynę. Stany podstawowe, takie jak niedobory żywieniowe, są łatwiejsze do leczenia niż inne, takie jak utajona utrata krwi. Dostępne są różne opcje leczenia pacjentów z rakiem i niedokrwistością. Obejmują one15:
- Odpowiednia terapia uzupełniająca kwasem foliowym i / lub witaminą B12 w celu wyrównania niedoborów żywieniowych
- Środki stymulujące erytropoezę (ESA)
- Suplementacja żelaza
- Transfuzje krwi, które są wskazane dla pacjentów z ostrą, ciężką utratą krwi. W przypadku pacjentów z przewlekłą niedokrwistością preferowane są leki erytropoetyczne.
Środki stymulujące erytropoezę: ESA, w tym rekombinowana ludzka erytropoetyna alfa (rHuEPO; Procrit, Epogen) i darbepoetyna alfa (Aranesp), były tradycyjnie opracowany do leczenia niedokrwistości u pacjentów z przewlekłą niewydolnością nerek. Wykazali podobną skuteczność i ograniczenia, gdy stosowali nieporównywalne dawki u pacjentów z rakiem i niedokrwistością.5 ESA są wskazane w leczeniu pacjentów, u których endogenne poziomy EPO są nienormalnie niskie, ponieważ tryb działania ESA oraz efekty immunologiczne i hematologiczne są podobne do tych w przypadku endogennej EPO.9 Badania przeprowadzone na rHuEPO wykazały, że poprawia on poziom i jakość życia pacjentów oraz zmniejsza zapotrzebowanie na transfuzję.15,16 Zaproponowano, że ESA poprawiają również funkcje poznawcze pacjentów otrzymujących chemioterapię.17
Przegląd systemowy przeprowadzone przez American Cancer Society wykazały, że optymalne korzyści kliniczne z leczenia erytropoetycznego niedokrwistości wywołanej chemioterapią można osiągnąć poprzez wczesną interwencję18. jednak wszystkie inne przyczyny niedokrwistości należy zbadać i skorygować przed zastosowaniem ESAtherapy.
Zarówno darbepoetyna, jak i rHuEPO są wskazane w leczeniu niedokrwistości u pacjentów z nowotworami niemieloidalnymi u osób, które są związane z chemioterapią.5 Amerykańskie Towarzystwo Hematologiczne (ASH) i Amerykańskie Towarzystwo Onkologii Klinicznej (ASCO) zalecają rozpoczęcie leczenia, gdy poziom Hb spadnie poniżej 10 g / dl, a dawkę należy zmniejszyć, jeśli występuje minimalny wzrost Hblevels o 2 g / dl. tygodni.19 Celem terapii powinno być obniżenie Hb do najniższego stężenia, aby uniknąć transfuzji. Jeżeli po 6 do 8 tygodniach leczenia nie zostanie osiągnięty minimalny wzrost o 1 do 2 g / dl Hb, należy przerwać terapię ESA.18 Chociaż trudno jest przewidzieć odpowiedź pacjenta na te terapie na podstawie aktualnych danych, wykazano, że około 50% do 60% pacjentów wykazuje wzrost Hb o 2 g / dl podczas leczenia rHuEPO.9 Leczenie ESA należy przerwać po zakończeniu kurs chemioterapii.20,21
Zalecana dawka darbepoetyny alfa wynosi 2,25 mcg / kg w cotygodniowych wstrzyknięciach podskórnych (sc.). Jeśli poziom Hb nie wzrośnie o co najmniej 1 g / dl po 6 tygodniach, dawkę należy zwiększyć do 4,5 mcg / kg. Jeśli poziom Hb wzrośnie o więcej niż 1 g / dl w okresie 2 tygodni lub jeśli Hb przekroczy 12 g / dl, dawkę darbepoetyny należy zmniejszyć o 40% .20 Darbepoetyny należy przerwać, jeśli poziom Hb wzrośnie powyżej 13 g / dl. 9
Zalecana dawka rHuEPO to 40 000 jednostek podskórnych podawanych raz w tygodniu lub 150 j./kg podskórnie trzy razy w tygodniu u pacjentów z poziomem Hb poniżej 10 g / dl. Dawkę rHuEPO należy zmniejszyć o 25%, jeśli poziom Hb wzrośnie o > 1 g / dl w dowolnym 2-tygodniowym okresie lub osiągnie poziom potrzebny do uniknięcia przetoczenia RBC.21
PZE są pakowane w fiolki, których nie należy wstrząsać, ponieważ ulegną denaturacji.20,21 Zawartości fiolki nie należy rozcieńczać ani łączyć.
Ryzyko związane z terapią ESA powinno być również wzięty pod uwagę. Uważa się, że ESA zwiększają niekorzystne zdarzenia sercowo-naczyniowe, zwiększają ryzyko żylnej choroby zakrzepowo-zatorowej, skracają czas do progresji guza i zmniejszają przeżycie u pacjentów z niedokrwistością dzięki różnym mechanizmom.22,23 Z tego powodu stosowanie ESAs odradza się u pacjentów z rakiem, którzy nie są poddawani leczenie chemioterapią lub radioterapią.24 Wszystkie ESA są dostarczane z ostrzeżeniem w czarnej skrzynce o zwiększeniu ryzyka zgonu, zawału mięśnia sercowego, udaru, żylnej choroby zakrzepowo-zatorowej, zakrzepicy dostępu naczyniowego oraz progresji i nawrotu guza.20,21 Program ESA APPRISE Onkology FDA ma doradzać pacjentom, opiekunom i pracownikom służby zdrowia w zakresie bezpiecznego stosowania ESA.25
Suplementacja żelaza: Suplementacja żelaza, najlepiej pozajelitowo, jest wskazana u pacjentów z niskim poziomem offerytyny (< 30 ng / ml), nasycenie transferyny (TSAT < 15%) i niskie (< 26 pg / komórkę ) zawartość Hb w retikulocytach t (CHr). U pacjentów z rakiem z niedokrwistością rozpoznano dwa rodzaje niedoboru żelaza:
- Bezwzględny niedobór żelaza (AID), który występuje przy przewlekłym krwawieniu z powodu, na przykład, zmian w obrębie przewodu pokarmowego lub narządów płciowych, utraty krwi podczas operacji, odżywiania niedobory i niedokrwistość chorób przewlekłych (ACD). Jest definiowany jako poziom ferrytyny w surowicy < 30 mcg / l i obniżony TSAT o < 15% .1
- Funkcjonalny niedobór żelaza (FID), który pojawia się po dalszym stosowaniu erytropoetyny. Jest to najczęstsza przyczyna niewystarczającej odpowiedzi na terapię ESA, szczególnie u pacjentów z niewydolnością nerek. Dlatego większość pacjentów leczonych ESA będzie ostatecznie wymagać suplementacji żelaza.6
Suplementacja żelaza została wprowadzona, gdy sama terapia ESA wykazała słabe wskaźniki odpowiedzi u pacjentów leczonych chemioterapią.1 Skuteczność połączenia IV. przetestowano terapię żelazem i ESA i ustalono rolę żelaza w funkcjonalnym niedoborze żelaza.1 Chociaż obecne dowody przemawiają za stosowaniem dożylnej suplementacji żelaza w celu poprawy odpowiedzi hemoglobiny u pacjentów z niedokrwistością i chorobą nowotworową, potrzebne są prospektywne badania długoterminowej skuteczności i bezpieczeństwa dożylnego podawania żelaza Ponadto należy ustalić optymalne schematy dawkowania.5
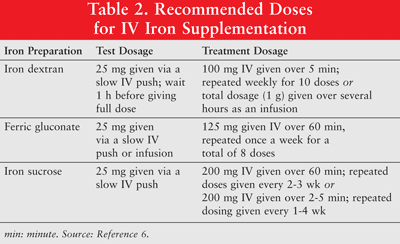
Żelazo można podawać doustnie lub w postaci preparatów pozajelitowych niskocząsteczkowego (LMW) dekstranu żelaza, glukonianu żelaza i sacharozy żelaza. Żelazo podawane pozajelitowo daje lepszą odpowiedź w porównaniu z żelazem podawanym doustnie.6 Z tego powodu to drugie żelazo jest rzadko stosowane u pacjentów z rakiem i niedokrwistością i nie jest omawiane w tym artykule. Zalecane są dawki testowe dla dekstranu żelaza. Pacjentom, którzy wcześniej wykazywali nadwrażliwość na dekstran żelaza lub inne preparaty żelaza dożylnego lub którzy mają alergie na wiele leków, należy również podać dawkę testową. TABELA 2 przedstawia schemat dawkowania w przypadku dożylnej suplementacji żelaza.6
Żelazo podawane pozajelitowo jest związane z niedociśnieniem, nudnościami, wymiotami i / lub biegunką, bólem, nadciśnieniem, dusznością, świądem, bólem głowy i zawrotami głowy. Co więcej, jego podawanie może być niewygodne i kosztowne.9 Ponieważ dekstran żelaza o dużej masie cząsteczkowej (HMW) wiąże się z większą częstością występowania zdarzeń niepożądanych niż dekstran żelaza LMW, ten ostatni jest ogólnie preferowany.6
Czerwony Transfuzja krwinek: RBC są preferowanym produktem krwiopochodnym do transfuzji w celu skorygowania niedokrwistości w przypadkach ostrej niedokrwistości po krwotoku. Niektórzy pacjenci mogą wymagać infuzji, która daje wynik ujemny w kierunku wirusa cytomegalii.Celem zastosowania transfuzji RBC jest leczenie lub zapobieganie niedoborowi zdolności krwi do przenoszenia tlenu, a transfuzja zwykle nie jest wskazana, jeśli Hblevel pacjenta wynosi ≥10 g / dL.6
Transfuzje RBC oferują Zaletą szybkiego wzrostu poziomu Hb i hematokrytu bezpośrednio po wlewie. Szacuje się, że transfuzja 300 ml (1 jednostka) czystych erytrocytów spowoduje średni wzrost o 1 g / dl Hb lub 3% hematokrytu u innej owłosionej osoby dorosłej, u której nie występuje jednoczesna utrata krwi. Prowadzi to do ogólnej, szybkiej poprawy zmęczenia.6
Krew pacjenta musi zostać dopasowana krzyżowo pod kątem zgodności ABO, zanim będzie można przetoczyć erytrocyty. Jeśli pacjent wymaga wielokrotnych wlewów, ryzyko wystąpienia działań niepożądanych można zminimalizować, stosując krew zmniejszającą leukocyty i premedykację antyhistaminą lub acetaminofenem.6
Transfuzja krwinek czerwonych nie jest pozbawiona ryzyka, w tym potencjalnego zakażenia przenoszonego przez transfuzję. leków, reakcji na transfuzję, alloimmunizacji i immunosupresji.9 Inne zagrożenia związane z transfuzją obejmują zastoinową niewydolność serca, nasilone zdarzenia zakrzepowe i przeciążenie żelazem.6 Należy jednak zauważyć, że pacjenci wymagający wlewów krwinek czerwonych w okresie odpowiadającym tylko chemioterapii są bardzo mało prawdopodobni. przeżyć przeciążenie żelazem.6
Perspektywy na przyszłość
Obecnie opracowuje się nowe strategie leczenia anemii u pacjentów z rakiem. Chociaż nie ma substytutu dla ludzkiej krwi, naukowcy są w trakcie opracowywania produktów, które mają zdolność przenoszenia tlenu przez RBC. W przygotowaniu są nośniki tlenu na bazie Hb i perfluorowęglowodory.5
Wniosek
Podsumowując, optymalne podejście do anemii jako ważnej kwestii w onkologii nie zostało jeszcze ustalone. Brak spójności między świadczeniodawcami, jasna definicja anemii w raku i kryteria diagnostyczne – wszystko to przyczynia się do tego problemu.
1. Steinmetz HT. Rola żelaza podawanego dożylnie w leczeniu niedokrwistości u chorych na raka. Ther Adv Hematol. 2012; 3: 177–191.
2. deBenoist B, McLean E, Egli I i wsp. Światowe występowanie anemii 1993–2005: Światowa baza danych WHO na temat anemii. Genewa, Szwajcaria: Światowa Organizacja Zdrowia; 2008.
3. Knight K, Wade S, Balducci L. Występowanie i wyniki anemii w raku: systematyczny przegląd literatury. Jestem J Med. 2004; 116 (dodatek 7A): 11S-26S.
4. Schwartz RN. Niedokrwistość u pacjentów z rakiem: częstość występowania, przyczyny, wpływ, postępowanie i stosowanie wytycznych leczenia i protokołów. Am J Health Syst Pharm. 2007; 64 (3 supl. 2): S5-S13; quiz S28-S30.
5. Calabrich A, Katz A. Leczenie niedokrwistości u pacjentów z rakiem. Future Oncol. 2011; 7: 507-517.
6. Rodgers GM, Becker P, Blinder M i wsp. Niedokrwistość wywołana rakiem i chemioterapią. J Natl Compr Canc Netw. 2012; 10: 628–653.
7. Groopman JE, Itri LM. Niedokrwistość wywołana chemioterapią u dorosłych: częstość występowania i leczenie. J Natl Cancer Inst. 1999; 91: 1616-1634.
8. Ludwig H, Strasser K. Symptomatology of anemia. Semin Oncol. 2001; 28: 7-14.
9. Gillespie TW. Niedokrwistość w raku. Pielęgniarstwo raka. 2003; 26: 119-128.
10. Koeller JM. Wytyczne kliniczne dotyczące leczenia niedokrwistości związanej z rakiem. Farmakoterapia. 1998; 18: 156-169.
11. Cazzola M, Mercuriali F, Brugnara C. Zastosowanie rekombinowanej ludzkiej erytropoetyny poza miejscem powstania mocznicy. Krew. 1997; 89: 424–867.
12. Nowrousian MR, Kasper C, Oberhoff C i wsp. Patofizjologia niedokrwistości związanej z rakiem. W: Smith JF, Boogaerts MA, Ehmer B, red. Erytropoetyna w leczeniu wspomagającym raka. Nowy Jork, Nowy Jork: Marcel Dekker; 1997: 13–34.
13. Vaupel P, Dunst J, Engert A i wsp. Wpływ rekombinowanej ludzkiej erytropoetyny (rHuEPO) na kontrolę guza u pacjentów z niedokrwistością wywołaną rakiem. Onkologie. 2005; 28: 216–221.
14. Zhao KL, Liu G, Jiang GL i wsp. Związek między poziomem hemoglobiny a zachorowalnością i śmiertelnością pacjentów z miejscowo zaawansowanym rakiem przełyku poddawanych radioterapii – analiza wtórna trzech kolejnych badań klinicznych III fazy. Clin Oncol (R Coll Radiol). 2006; 18: 621-627.
15. Glaspy JA. Rozwój czynników erytropoetycznych w onkologii. Expert Opin Emerg Drugs. 2005; 10: 553-567.
16. Adamson JW, Spivak JL. Fizjologiczne podstawy farmakologicznego zastosowania rekombinowanej ludzkiej erytropoetyny w chirurgii i leczeniu raka. Operacja. 1994; 115: 7-15.
17. Ferrario E, Ferrari L, Bidoli P i wsp. Leczenie niedokrwistości związanej z rakiem epoetyną alfa: przegląd. Cancer Treat Rev. 2004; 30: 563-575.
18. Lyman GH, Glaspy J. Czy istnieją korzyści kliniczne z interwencji erytropoetycznej w przypadku niedokrwistości wywołanej chemioterapią? Przegląd systematyczny. Rak. 2006; 106: 223–233.
19. Rizzo JD, Brouwers M, Hurley P i wsp. Aktualizacja wytycznych American Society of Clinical Oncology / American Society of Hematology Clinical Practice dotyczących stosowania epoetyny i darbepoetyny u dorosłych pacjentów z rakiem. J Clin Oncol. 2010; 28: 4996-5010.
20. Informacje dotyczące przepisywania leku Aranesp (darbepoetyna alfa).Thousand Oaks, Kalifornia: Amgen Inc; Maj 2012.
21. Informacje dotyczące przepisywania leku Procrit (epoetyna alfa). Horsham, PA: Janssen Products, LP; Lipiec 2012.
22. Beutel G, Ganser A. Zagrożenia i korzyści stosowania środków stymulujących erytropoezę w leczeniu raka. Semin Hematol. 2007; 44: 157-165.
23. Fenner MH, Ganser A. Erytropoetyna w niedokrwistości związanej z rakiem. Curr Opin Oncol. 2008; 20: 685–689.
24. Smith RE Jr, Aapro MS, Ludwig H, i wsp. Darbepoetinalfa do leczenia niedokrwistości u pacjentów z aktywnym rakiem nieotrzymujących chemioterapii lub radioterapii: wyniki wieloośrodkowego, randomizowanego, podwójnie ślepego badania fazy III, kontrolowanego placebo. J Clin Oncol. 2008; 26: 1040-1050.
25. Program Onkologii APRISE ESA. Amgen and Janssen Products, LP. www.esa-apprise.com. Dostęp 13 października 2013 r.