Klinisk sag
En 45-årig kvinde med en 20-årig historie med Crohns sygdom præsenteret med feber, kulderystelser og træthed i 10 dage. Kort før symptomernes begyndelse gennemgik patienten en ukompliceret koloskopi, hvor hun fik udført 17 biopsier til overvågning eller polypektomi. Under koloskopi var hendes Crohns sygdom i remission, og der blev ikke bemærket nogen slimhindebetændelse.
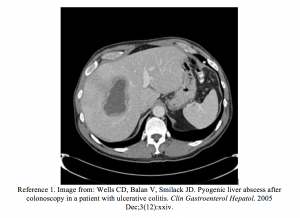
I ED var patientens vitale tegn HR 110, BP 120/80, RR 18, T 102,5. Hun havde mild ømhed i højre øvre del af maven. Laboratorieundersøgelser afslørede et forhøjet antal hvide blodlegemer (15.000) og forhøjet AST og ALT (120/137 U / L) med let forhøjet alkalisk fosfatase på 200 IE / L. En computertomografi (CT) -scanning af maven afslørede flere områder med lav dæmpning i den højre leverlobe i overensstemmelse med leverabscesser. Dræning af bylderne blev dyrket og voksede Streptococcus anginosus. Opløsning af alle læsioner opstod, efter at de blev drænet ved interventionel radiologi, og patienten fik et 6-ugers forløb med intravenøs antibiotika.
Introduktion
Koloskopi er en almindeligt udført procedure til diagnosticering og behandling af en lang række tilstande, herunder kræft, inflammatoriske tarmsygdomme, polypper, blødning og strikturer. Ifølge American Cancer Society anbefales screening af koloskopi hvert 10. år fra 50 år. Hos højrisikopatienter som dem med inflammatorisk tarmsygdom udføres koloskopi oftere. Proceduren er stadig den mest effektive måde at finde og fjerne små præ-kræft polypper på og dermed mindske risikoen for død fra tyktarms- og endetarmskræft.
Generelt er koloskopi meget sikker. En 2008-systematisk gennemgang af 12 undersøgelser på i alt 57.742 koloskopier udført til gennemsnitsrisikoscreening viste en samlet alvorlig bivirkningshastighed på kun 2,8 pr. 1000 procedurer og dødelighed på 0,007% .2 Risikoen for koloskopi er imidlertid ikke konstant på tværs af grupper og nogle komplikationer er mere almindelige end andre. Ældre voksne har øget risiko for alvorlige komplikationer sammenlignet med yngre patienter. I en undersøgelse af 53.220 koloskopier havde patienter i alderen 80 til 84 år en signifikant højere grad af alvorlige komplikationer sammenlignet med patienter i alderen 66 til 69 år. Risikoen for alvorlige komplikationer blev også øget blandt patienter med comorbide tilstande som anamnese med slagtilfælde, KOL, atrieflimren og hjertesvigt.
Pyogen leverabsces (PLA) er en sjælden, men alvorlig komplikation af koloskopi . De fleste komplikationer ved koloskopi vil forekomme inden for 7 dage, men PLA kan præsentere dage eller endda uger senere end det, og historien om nyere koloskopi kan ikke engang fremkaldes, medmindre klinikeren er opmærksom på denne enhed. af PLA, vil disse patienter sandsynligvis blive diagnosticeret i akutafdelingen.
Andre sene komplikationer såsom post-polypektomi elektrokoagulationssyndrom og de mere almindelige problemer med forsinket blødning, uspecifik mavesmerter, reaktioner på sedationsmidler og perforering kan også ses i ED. I modsætning hertil vil gasexplosion eller øjeblikkelig blødning sjældent ses i ED, da disse problemer typisk optræder hurtigt i endoskopipakken, hvor de behandles med det samme. ED-læger skal være opmærksomme på alle mulige komplikationer og deres tidsforløb og have værktøjerne til korrekt diagnose og behandling af den uheldige postkoloskopipatient, der lider af en alvorlig komplikation.
Komplikationer
Pyogenic Leverabscess
PLA er en farlig sygdom med høj sygelighed og dødelighed, der forekommer med en hastighed på 10 til 20 tilfælde pr. 100.000 hospitalsindlæggelser.4-6 Med fremskridt inden for diagnostiske teknikker og interventioner forbedres dødeligheden.7 Imidlertid er patienter stadig i alvorlig fare, især hvis diagnosen er forsinket, som det ofte er, fordi patienter kan præsentere ikke specifikt. En retrospektiv undersøgelse af 63 patienter med PLA viste, at feber var almindelig (59%), men andre tegn og symptomer såsom højre øvre kvadrantsmerter og peritoneale tegn var til stede hos henholdsvis kun 39% og 14%. 8 Diagnose i denne undersøgelse var forsinkede ofte i gennemsnit en uge fra symptomdebut.
Koloskopi er en sjælden, men sandsynligvis også underkendt udfældning af PLA. Det menes, at tavse mikroperforeringer under proceduren fører til infektion, som kan frø leveren gennem portalcirkulationen. Tilsvarende kan andre intra-abdominale infektioner såsom diverticulitis potentielt forårsage PLA, hvis det inficerede område drænes af portalvenen.9 Leverclearance af bakterier via portalnetværket er et normalt fænomen hos raske patienter, men galdeobstruktion, dårlig perfusion og høj bakteriel belastning (som i tilfælde af infektion eller flere biopsier under koloskopi, der udså blodbanen), kan prædisponere for spredning og byld dannelse. Litteraturen beskriver ca. 34% af PLA-tilfælde som kryptogene, men en del af disse kan meget vel være patienter med nyere koloskopi, der ikke blev anerkendt som en risikofaktor for sygdomsprocessen.8
De fleste PLA-isolater er polymikrobielle og består af normal enterisk flora. Blodkulturer er positive i 33-65% af tilfældene, men abscesskulturer er næsten alle positive.10 De mest isolerede mikroorganismer er Streptococcus-arter (37%), Eserichia Coli (33%), Bacteroides-arter (24%), Klebsiella pneumoniae (18%) og mikroaerofile streptokokker (12%). 10-11 Strep anginosus, der findes i denne patients tilfælde, er en fakultativ anaerob gram-positiv coccus og en af de mere almindelige organismer, der findes i PLA.
Hurtig diagnose af PLA er kritisk, for selvom diagnose og terapi forbedres, forbliver dødeligheden på 10%. 5,7 Infektiøse komplikationer ved koloskopi generelt er sjældne, men igen er årsagsforholdet sandsynligvis også underkendt. Koloskopi er blevet impliceret i mindst et par tilfælde af PLA.12-14 Men forbigående systemisk bakteriæmi, set i 4% af koloskopier, ser ikke ud til at øge risikoen for infektion i sig selv.15 I stedet antages infektionen i PLA at sprede sig via faktiske mikroperforeringer.
Selvom det vides, at oprigtige perforeringer er relativt sjældne (mindre end 0,1% af koloskopier), er forekomsten og patofysiologien af mikroperforeringer ikke helt kendt.16-17 Bevæbnet med viden om denne kliniske enhed, en kliniker, der fremkalder en god historie og har et højt mistænkningsindeks, kan hurtigere diagnosticere PLA hos en patient med nyere koloskopi.
Infektion
Det er almindeligt accepteret, at forbigående bakteriæmi efter koloskopi forekommer i ca. 4% af procedurerne, selvom intervallet rapporteres som 0-25%, og risikofaktorer for bakteriæmi er ikke defineret.18 Højere priser for bakteriæmi forekommer under rutinemæssige daglige aktiviteter såsom tandbørstning og tygge mad. Selvom tegn eller symptomer på systemisk infektion hos patienter med forbigående bakteriæmi er sjældne, kan patienter føle feber, kulderystelser og klager, der efterligner alt fra øvre luftveje til abdominale infektioner.18
Selvom forbigående bakteræmi er en accepteret risiko for koloskopi , er der ingen dokumenteret fordel for rutinemæssig antibiotikaprofylakse, og de fleste patienter vil ikke have taget peri-procedure antibiotika.18 Nuværende retningslinjer fra American Society for Gastroenterology (ASGE) er enige med American Heart Association (AHA) og anbefaler mod antibiotikaprofylakse for patienter, der gennemgår rutinemæssig koloskopi.19
Det kan være svært at skelne mellem symptomer på forbigående bakteriæmi og ægte infektion.18 Generelt garanterer patienter med infektiøse symptomer i dagene efter koloskopi laboratorieundersøgelser inklusive blodkulturer og afhængigt af indekset for mistanke om perforering, abdominal billeddannelse.20-21 Hvis mistanke om perforering er lav eller diagnoserne s er udelukket, kan IV-hydrering og antibiotika gives, hvis det er berettiget af patientens kliniske status.
Blødning
Blødning efter polypeptomi kan enten være øjeblikkelig eller forsinket. Umiddelbar blødning er forbundet med polypektomi-teknikker, der ikke bruger kauteri, eller når der anvendes blandet strøm til proceduren. Forsinket blødning ses mere almindeligt i ED, da øjeblikkelig blødning ofte opdages på tidspunktet for proceduren og behandles af endoskopisten. Forsinket blødning kan ses op til 7 dage efter proceduren. Det antages at forekomme på grund af sloughing af en eschar, der dækkede et blodkar eller på grund af udvidelse af zonen for termisk nekrose til ikke-skadet væv, hvilket kan resultere i blødning, hvis det involverer et blodkar.19,22
Flere store undersøgelser har rapporteret blødning i 1 til 6 pr. 1000 koloskopier (0,1% -0,6%). 22 En undersøgelse, der analyserede over 50.000 koloskopier, fandt imidlertid, at frekvensen af GI-blødning var signifikant forskellig afhængigt af, om der blev udført polypektomi. Post-polypectomy blødning forekommer ved 1-2%, med højere priser set med fjernelse af større polypper. Risikoen for blødning efter polypektomi kan øges hos patienter med trombocytopeni eller koagulopatier.23
Kendte risikofaktorer for blødning efter koloskopi inkluderer polyppestørrelse, antal fjernede polypper, historie med nylig antikoagulantanvendelse eller polyp histologi.22 Mærkeligt nok fandt flere, store undersøgelser ikke anvendelse af aspirin forbundet med blødning efter polypeptomi.24-26
Patienter med forsinket blødning kan være tegn på blødning eller anæmi, herunder træthed, svaghed , bleghed, kraftig blødning eller blodpropper ved aftørring, takykardi, brystsmerter og åndenød.Patienter kan beskrive hæmatochezia eller melena afhængigt af placeringen af blødningen.
Indledende behandling af en patient med mistanke om blødning inkluderer adressering af grundlæggende luftvej, vejrtrækning og cirkulation med 2 store borings-IV’er, krystalloidvæsker og hjerteovervågning. Patienter med grov lavere gastrointestinalt blødning kan dekompensere hurtigt og skal have en aktiv type og skærm i tilfælde af transfusion.
Billedbehandling er ikke altid nødvendig, og hvis det er muligt, skal beslutningen om billeddannelse træffes sammen med GI konsulter, helst den læge, der udførte koloskopi. Gentag koloskopi er ofte den valgte diagnostiske og terapeutiske procedure. American College of Radiology giver den højeste hensigtsmæssighed til koloskopi, selvom den også inkluderer CTA i underlivet / bækkenet og Tc-99m RBC-scanning underliv / bækken som muligt passende trin i diagnosen.27
Hvis patienten er ustabil, og den udførende endoskopist er utilgængelig, bør ED-lægen konsultere generel interventionel radiologi (IR), GI og kirurgi.
Perforering
Kolonoskopisk perforering (CP) er en af de mest alvorlige og frygtede komplikationer af koloskopi. Selvom det er sjældent, resulterer CP i høj sygelighed og dødelighed. 28-32 Perforering kan skyldes mekaniske kræfter mod tarmvæggen, barotrauma eller elektrokauteri og kan føre til dannelse af byld, fisteldannelse, intra-abdominal sepsis, forlænget hospitalsophold og endda død.
CP forekommer i ca. 0,016% af diagnostiske koloskopier, men kan ses hos op til 5% af terapeutiske koloskopier.33-35 Afhængigt af hvad der faktisk blev gjort under koloskopi, kan risikoen for perforering være højere eller lavere end gennemsnittet, så det kan være nyttigt at bestemme risikoen for at opnå den operative rapport eller historie fra endoskopisten.
CP-risiko ved forskellige koloskopiske procedurer: 1,36-37
-Screeningskoloskopi: 0,01-0,1%
-Anastomotisk strikturudvidelse: 0-6%
-Crohn-sygdomsstrikurudvidelse: 0-18%
-Stent placering: 4%
-Kolonisk dekompressionsrørplacering: 2%
-Kolonisk endoskopisk slimhinderesektion 0-5%
Bortset fra begivenhederne under procedure, specifikke risikofaktorer for CP inkluderer avanceret alder, multiple comorbiditeter, divertikulose, obstruktion, resektion af polypper, polypper, der er større end 1 cm i størrelse eller dem, der findes i højre tyktarm, nedsat mobilitet i tyktarmen, eksisterende svaghed i tyktarmen , tidligere ufuldstændigt forsøg på koloskopi eller endoskopisk uerfarenhed.20
Patienter med CP kan præsentere med pludselige, forværrede mavesmerter, efterfulgt af den falsk beroligende fuldstændige spredning af smerte, når perforeringen dekomprimerer det betændte organ. Da gastrointestinalt indhold fortsætter med at smitte ind i bughinden, udvikler forværrede smerter og peritoneale symptomer. Imidlertid vil symptomerne variere afhængigt af perforationens placering og størrelse, graden af fækalt siv i peritoneum og patientens alder og comorbiditeter.
Især kan perforeringer også være retroperitoneal svarende til placeringen af den stigende og nedadgående tyktarm og lever- og miltbøjninger. Selvom det mest almindelige symptom på en perforation i tyktarmen er mavesmerter, kan ældre patienter have en stump respons. Andre symptomer inkluderer feber, kvalme, opkastning, dyspnø, brystsmerter, scapular smerter og nakkesmerter. Især retroperitoneale perforeringer kan have minimale eller atypiske symptomer, og vitale tegn kan vise takykardi og feber, men kan også være normale.20
Indledende behandling af en mistanke om perforering inkluderer opmærksomhed på luftvejene, vejrtrækning, cirkulation med 2 store boring IV’er, krystalloide væsker og hjerteovervågning. Der skal opnås laboratorier inklusive CBC, CMP, lipase, type og skærm. Patienten skal være strengt NPO med empiriske IV-antibiotika. Stat-billeddannelse med CT-mave / bækken eller abdominal røntgen, hvis ustabil, skal bestilles sammen med en statisk kirurgisk konsultation.21
Post-polypectomy syndrom
Post-polypectomy syndrom, også kendt som post-polypektomi elektrokoagulationssyndrom eller transmural forbrændingssyndrom, resultat af elektrokoagulationsskade på tarmvæggen, hvilket skaber en transmural forbrænding og fokal peritonitis uden åben perforation.38 Den rapporterede forekomst varierer fra 3 pr. 100.000 (0,003%) til 1 ud af 1000 (0,1% ). Post-polypektomisyndrom blev rapporteret hos 6 patienter ud af 16.318 koloskopier udført mellem 1994 og 2002 i et stort integreret sundhedssystem.39 Risikofaktorer for denne usædvanlige komplikation er ukendte.
Patienter med post-polypektomisyndrom er normalt til stede inden for 12 timer efter koloskopi med feber, takykardi og mavesmerter. Imidlertid kan symptomernes begyndelse blive forsinket med op til 5-7 dage efter proceduren. 40 Patienter har ofte leukocytose og kan udvise stivhed og takykardi, som alle efterligner kolonperforering.41
Men i modsætning til perforering, som kan kræve nye operationer, behandles patienter med post-polypektomisyndrom generelt konservativt med intravenøs væske, smertekontrol og gradvis fremskridt i kosten med eller uden antibiotika målrettet mod gram- negative og anaerobe patogener.42 Mindre alvorlige tilfælde kan endda håndteres poliklinisk med orale antibiotika og klare væsker i 1-2 dage. 42-43
Da disse patienter kan skelnes fra patienter med perforering, enhver patient, der mistænkes for post-polypektomisyndrom, garanterer laboratorier og billeddannelse. Ved post-polypektomisyndrom udviser CT-scanning normalt fokal fortykning af tyggevæggen med omgivende fedtstrengning uden ekstramural luft, selvom CT i milde tilfælde kan være negativ.42 Uanset billeddannelsesresultat, som med perforering, hvis post-polypectomy syndrom mistænkes, bør patienten have en kirurgisk konsultation.
Perler
- Koloskopi er en udbredt screeningstest hos patienter over 50 år. Komplikationer kan være tidlige eller forsinkede. EM-læger skal være opmærksomme på de mulige komplikationer og deres forventede tidslinje for nøjagtigt at diagnosticere og håndtere enhver mulig præsenterende komplikation. pyogen leverabsces.
- Historie om patientfaktorer og selve proceduren (underliggende tilstande, medicin, om polypper blev fjernet, hvis der blev brugt kauteri, om der var øjeblikkelig blødning) kan lede diagnose og behandling i ED.
- Pyogen leverabsces kan forekomme 1-2 uger efter koloskopi med smerter og feber i højre øvre kvadrant.
- Meget af tyktarmen er retroperitoneal. Retroperitoneale perforeringer kan forårsage vage og atypiske symptomer, så mistankeindekset skal være højt.
- Post-polypektomisyndrom kan efterligne perforering og kan normalt differentieres ved billeddannelse.
Referencer / Yderligere læsning:
- Wells CD, Balan V, Smilack JD. Pyogen leverabsces efter koloskopi hos en patient med colitis ulcerosa. Clin Gastroenterol Hepatol. 2005 Dec; 3 (12): xxiv.
- Whitlock, E.P., Lin, J.S., Liles, E. et al. Screening for kolorektal kræft: en målrettet, opdateret systematisk gennemgang af US Preventive Services Task Force. Ann Intern Med. 2008; 149: 638–658.
- Warren JL, Klabunde CN, Mariotto AB, Meekins A, Topor M, Brown ML, Ransohoff. Bivirkninger efter ambulant koloskopi i Medicare-befolkningen. Ann Intern Med. 2009; 150 (12): 849.
- Johannsen EC, Sifri CD, Madoff LC. Pyogene leverabscesser.Infekt Dis Clin North Am. 2000; 14: 547–63.
- Meddings L, Myers RP, Hubbard J, et al. En befolkningsbaseret undersøgelse af pyogene leverabscesser i USA: Incidens, dødelighed og tidsmæssige tendenser. Am J Gastroenterol. 2010; 105: 117-24.
- Kaplan GG, Gregson DB, Laupland KB. Befolkningsbaseret undersøgelse af epidemiologi af og risikofaktorer for pyogen leverabsces. Clin Gastroenterol Hepatol. 2004; 2: 1032-8.
- Petri A, Höhn J, Hódi Z, Wolfárd A, Balogh A. Pyogen leverabscess – 20 års erfaring. Sammenligning af behandlingsresultater i to perioder. Langenbecks Arch Surg. 2002; 387: 27–31.
- Pang TC, Fung T, Samra J, Hugh TJ, Smith RC. Pyogen leverabsces: En revision af 10 års erfaring. Verden J Gastroenterol. 2011; 17: 1622-30.
- Murarka S, Pranav F, Dandavate V. DisseminatedStreptococcus anginosus fra sigmoid diverticulitis. J Glob Infect Dis. 2011; 3: 79-81.
- Branum GD, Tyson GS, Branum MA, Meyers WC. Leverabscess. Ændringer i etiologi, diagnose og ledelse. Ann Surg. 1990 212 december (6): 655-62.
- Gyorffy EJ, Frey CF, Silva J Jr, McGahan J. Pyogen leverabsces. Diagnostiske og terapeutiske strategier. Ann Surg. 1987 20. december (6): 699-705.
- Bonenfant F, Rousseau É, Farand P. Streptococcus anginosuspyogen leverabsces efter en screeningskoloskopi. Canadian Journal of Infectious Diseases & Medicinsk mikrobiologi. 2013; 24 (2): e45-e46.
- Ian G. Harnik. Pyogen leverabsces præsenteret efter ondartet polypektomi. Dig Dis Sci. 2007; 52: 3524–5.
- Paraskeva KD, Bury RW, Isaacs P.Streptococcus milleri leverabscesser: En usædvanlig komplikation efter koloskopisk fjernelse af en påvirket fiskeben. Gastrointest Endosc. 2000; 51: 357–8.
- Low DE, Shoenut JP, Kennedy JK, et al. Prospektiv vurdering af risikoen for bakteriæmi med koloskopi og polypektomi. Dig Dis Sci. 1987; 32: 1239–43.
- Becker F, Nusko G, Welke J, Hahn EG, Mansmann U. Opfølgning efter kolorektal polypektomi: En fordel-risikoanalyse af tyske overvågningsanbefalinger. Int J Colorectal Dis. 2007; 22: 929–39.
- Macrae FA, Tan KG, Williams CB. Mod sikrere koloskopi: En rapport om komplikationerne ved 5000 diagnostiske eller terapeutiske koloskopier. Tarm. 1983; 24: 376-83.
- Nelson, D.B.Infektionssygdomme komplikationer af GI endoskopi: del II, eksogene infektioner. Gastrointest Endosc. 2003; 57: 695-711.
- Khashab, M.A., Chithadi, K.V., Acosta, R.D. et al. Antibiotisk profylakse til mave-endoskopi. ASGE Standards of Practice Committee. Gastrointest Endosc. 2015; 81: 81-89.
- Lohsiriwat V. Kolonoskopisk perforering: Incidens, risikofaktorer, styring og resultat. World Journal of Gastroenterology: WJG. 2010; 16 (4): 425-430.
- American College of Radiology ACR-passende kriterier: Akut (ikke-lokaliseret)
- Ko, C.W. og Dominitz, J.A. Komplikationer af koloskopi: størrelse og ledelse. Gastrointest Endosc Clin N Am. 2010; 20: 659–671.
- Warren JL, Klabunde CN, Mariotto AB, et al. Bivirkninger efter ambulant koloskopi i Medicare-befolkningen. Ann Intern Med 2009; 150: 849-57.
- Hui, A.J., Wong, R.M., Ching, J.Y. et al. Risiko for blødning med koloskopisk polypektomi med antikoagulantia og blodplader: analyse af 1657 tilfælde. Gastrointest Endosc. 2004; 59: 44–48.
- Sawhney, M.S., Salfiti, N., Nelson, D.B. et al. Risikofaktorer for alvorlig forsinket blødning efter postolypektomi. Endoskopi. 2008; 40: 115–119
- Yousfi, M., Gostout, C.J., Baron, T.H. et al. Postpolypectomy nedre gastrointestinal blødning: aspirins potentielle rolle. Am J Gastroenterol. 2004; 99: 1785–1789.
- American College of Radiology ACR-passende kriterier: Radiologisk håndtering af blødning i nedre mave-tarmkanalen. https://acsearch.acr.org/docs/69457/Narrative/ (Adgang til 16. juli 2017).
- Lohsiriwat V, Sujarittanakarn S, Akaraviputh T, Lertakyamanee N, Lohsiriwat D, Kachinthorn U. Kolonoskopisk perforering: En rapport fra World Gastroenterology Organization endoscopy træningscenter i Thailand. Verden J Gastroenterol. 2008; 14: 6722-6725.
- Iqbal CW, Cullinane DC, Schiller HJ, Sawyer MD, Zietlow SP, Farley DR. Kirurgisk styring og resultater af 165 koloskopiske perforeringer fra en enkelt institution. Arch Surg. 2008; 143: 701-706; diskussion 706-707.
- Teoh AY, Poon CM, Lee JF, Leong HT, Ng SS, Sung JJ, Lau JY. Resultater og forudsigere for dødelighed og stomidannelse i kirurgisk styring af koloskopiske perforeringer: en multicenter-gennemgang. Arch Surg. 2009; 144: 9–13.
- Lüning TH, Keemers-Gels ME, Barendregt WB, Tan AC, Rosman C. Kolonoskopiske perforeringer: en gennemgang af 30.366 patienter. Kirurgisk endosc. 2007; 21: 994–997.
- Mai CM, Wen CC, Wen SH, Hsu KF, Wu CC, Jao SW, Hsiao CW. Iatrogent kolonperforering ved koloskopi: en dødelig komplikation for patienter med høj risiko for bedøvelse. Int J Colorectal Dis. 2010 apr; 25 (4): 449-54.
- Rathgaber SW, Wick TM. Koloskopi færdiggørelse og komplikationsrater i en gastroenterologisk praksis i samfundet. Gastrointest Endosc. 2006; 64: 556-562.
- Damore LJ, Rantis PC, Vernava AM, Longo WE. Koloskopiske perforeringer. Etiologi, diagnose og ledelse. Dis Colon Rectum. 1996; 39: 1308–1314.
- Repici A, Pellicano R, Strangio G, Danese S, Fagoonee S, Malesci A. Endoskopisk slimhinderesektion til tidlig kolorektal neoplasi: patologisk basis, procedurer og resultater. Dis Colon Rectum. 2009; 52: 1502-1515.
- Chukmaitov A, Bradley CJ, Dahman B, et al. Forening af polypektomiteknikker, endoskopistvolumen og facilitetstype med koloskopikomplikationer. Gastrointest Endosc. 2013; 77: 436.
- Fisher DA, Maple DT, et al. Komplikationer af koloskopi. ASGE Standards of Practice Committee Gastrointest Endosc. 2011; 74: 745. Mavesmerter og feber eller mistanke om maveabscess; Variant 1: Postoperativ patient med feber. https://acsearch.acr.org/docs/69356/Narrative/ (Adgang til 17. juli 2017).
- Hirasawa K, Sato C, Makazu M, et al. Koagulationssyndrom: Forsinket perforering efter endoskopisk kolorektal behandling. World Journal of Gastrointestinal Endoscopy. 2015; 7 (12): 1055-1061.
- Levin TR, Zhao W, Conell C, Seeff LC, Manninen DL, Shapiro JA, Schulman J. Komplikationer af koloskopi i et integreret sundhedsvæsen. Ann Intern Med. 2006; 145 (12): 880.
- Kim HW. Hvad er forskellen mellem postpolypektomifeber og postpolypektomikoagulationssyndrom? Clin Endosc. 2014; 47 (3): 205–6.
- Bestand C, Ihle P, Sieg A, Schubert I, Hoffmeister M, Brenner H Bivirkninger, der kræver hospitalsindlæggelse inden for 30 dage efter ambulant screening og ikke-screening af koloskopier. Gastrointest Endosc. 2013 mar; 77 (3): 419-29.
- Sethi A, sang LMWK. Bivirkninger relateret til endoskopisk endoskopisk slimhinderesektion og polypektomi. Gastrointest Endosc Clin N Am. 2015; 25 (1): 55–69.
- Benson BC, Myers JJ, Laczek JT. Postpolypectomy elektrokoagulationssyndrom: En efterligner af colon perforering. Sagsrepræsentant Emerg Med. 2013; 2013 687931.