Dette kursus blev offentliggjort i marts 2016-udgaven og udløber den 31.3.19. Forfatterne har ingen kommercielle interessekonflikter at afsløre. Denne 2-kredit timers selvstudie-aktivitet formidles elektronisk.
MÅL
Efter at have læst dette kursus skal deltageren være i stand til at:
- Diskutere de forskellige typer lægemidler, der kan forårsage tandkødsforstørrelse.
- Identificer de kliniske træk ved tandkødsforstørrelse.
- Forklar etiologien og risikofaktorerne for lægemiddelinduceret tandkødsudvidelse
udvidelsen. - Angiv de tilgængelige muligheder for behandling af denne tilstand.
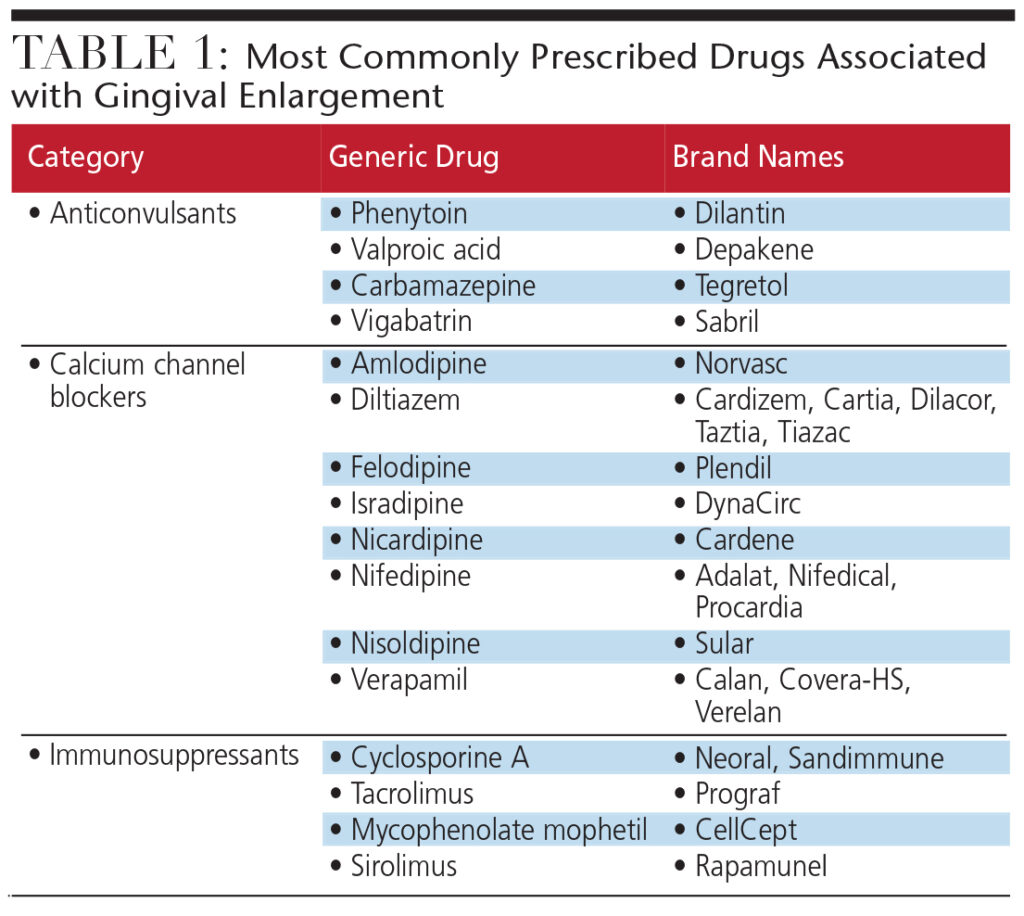
Bakterier, vira, neoplasmer og visse lægemidler kan påvirke tandkøds sundhed negativt. Tandkødsforstørrelse øger risikoen for infektion, karies og periodontal sygdom og påvirker smilestetik negativt. Initieret af både systemiske og inflammatoriske faktorer, er tandkødsforstørrelse ofte forårsaget af almindelig receptpligtig medicin. Disse lægemidler – antikonvulsiva, calciumkanalblokkere (CCB’er) og immunsuppressiva – fremmer ændringer i fibroblastfunktionen, hvilket fører til en stigning i den ekstracellulære matrix af gingival bindevæv (tabel 1). For at gendanne normal fibroblastfunktion og tandkøds sundhed kan et andet lægemiddel muligvis erstattes af den krænkende medicin. Når substitution ikke er mulig, kan kirurgisk excision af tandkødsvæv give midlertidig lindring til patienter, der er ramt af lægemiddelinduceret tandkødsforstørrelse.
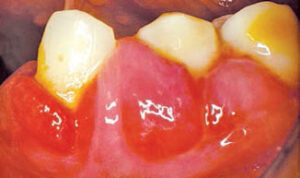
Opdagelsen af phenytoin i 1938 af Merritt og Putnam gav et stort gennembrud i styringen af patienter med epilepsi.1 Kort efter dets introduktion begyndte imidlertid rapporter, der forbinder phenytoin til tandkødsovervækst, at dukke op.2 Følsomhed over for dette lægemiddel er ikke universel, da forekomsten af godartet udvidelse varierer blandt befolkningens undergrupper. Gingivalforstørrelse induceret af antikonvulsiva er signifikant højere blandt børn og institutionaliserede patienter. For ikke-institutionaliserede patienter er forekomsten af tandkødsovervækst forårsaget af phenytoin ca. 50%, og tilstanden påvirker oftest de maxillære forreste tænder (figur 1) .3 Gingivalforstørrelse vises typisk to måneder til tre måneder efter, at den første dosis af phenytoin er taget , der når sin maksimale sværhedsgrad ca. 12 måneder til 18 måneder senere.
Siden 1938 er der indført adskillige antikonvulsive midler – herunder valproinsyre, carbamazepin, phenobarbital og vigabatrin – i et forsøg på at overvinde de negative virkninger af phenytoin . Tilfælde af tandkødsforstørrelse er også blevet bemærket med disse stoffer, men sådanne rapporter er sjældne og dårligt dokumenterede.
På grund af dens effektivitet til at kontrollere krampeanfald, såvel som dens lave omkostninger og bred tilgængelighed, phenytoin er stadig det valgte lægemiddel til behandling af epilepsi – især til grand mal, temporal lap og psykomotoriske anfald. Mange patienter er tilbageholdende med at erstatte den med en ny klasse antikonvulsiva, hvilket gør det bydende nødvendigt, at oral sundhedspersonale anerkender den øgede risiko og er parat til at tackle phenytoin-induceret tandkødsforstørrelse i disse patientpopulationer.
CALCIUM CHANNEL BLOCKERS
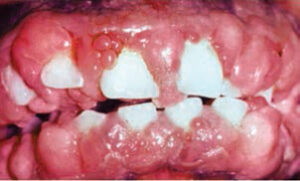
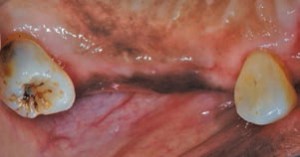
Denne klasse af lægemidler anvendes i vid udstrækning til håndtering af hypertension, angina og supraventrikulær hjertearytmi. Disse lægemidler får deres vigtigste terapeutiske virkning ved at forhindre calciumiontilstrømning gennem cellemembraner. Ikke alle CCB’er påvirker imidlertid tandkødet på samme måde. Nifedipin er den hyppigst implicerede CCB i lægemiddelinduceret tandkødsovervækst (figur 2 til figur 4). 4 Lederman et al rapporterede først sine negative orale virkninger i 1984, og efterfølgende undersøgelser viste, at forekomsten af bivirkninger varierede fra 14% til 83% .5–7
Forekomsten af negative gingivaleffekter er signifikant lavere med verapamil og amlodipin (henholdsvis 4,2% og 3,3%).8,9 Talrige rapporter har også associeret tandkødsudvidelse med den nye generation af CCB’er, såsom felodipin, nicardipin, manidipin og diltiazem.
IMMUNOSUPPRESSANTER
Immunsuppressiva reducerer forekomsten og sværhedsgraden af allotransplantatafstødning efter transplantationer af større organer (fx lever, bugspytkirtel, hjerte eller lunge) såvel som til styring af autoimmune tilstande, såsom reumatoid arthritis .
Siden opdagelsen af Borel et al i 1977 er cyclosporin A blevet det mest almindeligt ordinerede lægemiddel til forebyggelse af organafstødning.10 Det kan desværre udøve alvorlige bivirkninger, herunder nefrotoksicitet, induktion af en diabetisk tilstand , kronisk hovedpine og vanærende tandkødsforstørrelse (figur 5). Den første offentliggørelse af tandkødsovervækst blev rapporteret hos nyretransplanterede patienter fire uger til seks uger efter den indledende dosis.11 Forstørrelsen var mere udtalt på tandkødets labiale aspekt og var forbundet med signifikant blødning. Når tænderne blev trukket kirurgisk ud, blev forstørrelsen imidlertid permanent elimineret. Forekomsten af cyclosporin A-associeret tandkødsforstørrelse varierer fra 8% til 81%, hvor børn og unge har størst risiko. 12,13
Nye immunsuppressive lægemidler, såsom tacrolimus, mycophenolatmophetil og sirolimus, har givet alternative muligheder for behandling af organtransplantationspatienter uden risiko for tandkødsovervækst.14
KLINISKE FUNKTIONER
Mens den orale manifestation af hver type lægemiddelinduceret tandkødsforstørrelse er ens, det er ikke en diagnostisk faktor. At holde en detaljeret patienthistorie hjælper tandlæger med at opnå en nøjagtig diagnose. I deres indledende faser kan læsioner fremstå som en fast nodulær forstørrelse af de interdentale papiller og kan forekomme i mundhulen. Tandkødsovervækst påvirker mere almindeligt den forreste region, med større udtale på ansigts- / bukkale overflader end palatale / lingualoverflader. 15 Udvidelsen kan variere fra en mild stigning i interproximale tandkødspapiller til svær udvidelse af både marginale og papillære væv. I alvorlige tilfælde forstørres hele papiller og det omgivende væv, hvilket giver tandkødsvævet et lobuleret udseende (figur 6).
Forstørrelsen kan strække sig koronalt og interferere med mastikation og tale; derudover kan det i tilfælde af forreste tænder føre til æstetiske problemer. Overgroet væv skaber lommer, der kan rumme patogene mikrober uden for rækkevidde af en tandbørste eller tandtråd.
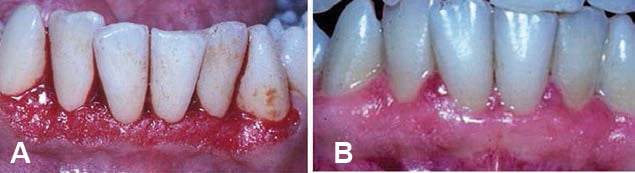
Selvom disse lægemidler ikke direkte påvirker den underliggende alveolære knogle, kan tandkødsforstørrelsen blive overlejret blandt patienter med allerede eksisterende parodontitis, eller patienter kan få det samtidig. Gingivalforstørrelse kan præsentere med forskellige former, der spænder fra ikke-betændt, fast og fibrøs tandkød til tandkødsvæv domineret af ødem, erytem og blødning. markant klinisk markør til at hjælpe oral sundhedspersonale med at nå en nøjagtig diagnose. Disse læsioner efterligner adskillige patologiske tilstande, der manifesterer sig på samme måde. Udvidelsen kan være lokaliseret eller generaliseret. Lokal tandkødsovervækst kan være forårsaget af en parodontal byld, fibroma eller et pyogent granulom (vævsovervækst forårsaget af irritation, traumer eller hormonelle udsving, såsom oplevet under graviditet). Den lokale karakter af disse læsioner – sammen med de kliniske tegn og symptomer og patientens medicinske og tandhistorie – hjælper med at skelne dem fra tandkødsforstørrelse forårsaget af medicinbrug.
Generaliseret tandkødsforstørrelse udgør en vanskelig diagnostisk udfordring hos nogle patienter. Den mest almindelige faktor, der er involveret i størstedelen af tandkødsforstørrelsen, er oral biofilm, som skal behandles som plak-induceret tandkødsovervækst med skalering og rodplanning kombineret med god egenpleje. Hvis læsionerne vedvarer tre uger til fire uger efter behandlingen, skal patienten henvises til en læge for at udelukke systemisk sygdom som en årsagsfaktor. Udiagnosticeret eller dårligt kontrolleret diabetes er en væsentlig synder, der forårsager generaliseret inflammatorisk tandkødsforstørrelse og betydelig periodontal ødelæggelse.
Andre systemiske sygdomme, der kan forårsage tandkødsforstørrelse, inkluderer akut leukæmi, Wegeners granulomatose og skørbugt. Hurtig tandkødsovervækst ledsaget af blødning kan indikere tilstedeværelsen af akut myeoblastisk leukæmi, kronisk myeloid leukæmi, akut lymfocytisk leukæmi eller kronisk lymfocytisk leukæmi. Blandt patienter diagnosticeret med akut myeloblastisk leukæmi oplever 5% tandkødsforstørrelse som den første komplikation.16,17 Leukæmi er en ondartet sygdom, og dens vellykkede opløsning afhænger af tidlig diagnose og behandling. Oral sundhedspersonale bør henvise patienter til en læge, når der konstateres en hurtig fremskridt af tilvækst.16,17
I Wegeners granulomatose ser tandkødet ud hævet og lysrødt med en granulær overflade beskrevet som “jordbærgummi. ” Der er mistanke om differentiel diagnose gennem denne karakteristiske kliniske manifestation, men den skal bekræftes ved biopsi. Skørbug, resultatet af C-vitaminmangel, er ret sjælden, men patienter, der er ramt af denne tilstand, kan opleve svær tandkøds hævelse og blødning ledsaget af mobile tænder. Klinikere kan stole på en høj dosis af C-vitamin og ikke-kirurgisk periodontal behandling for at løse tandkødsforstørrelse i denne patientgruppe.
Desuden kan generaliseret tilvækst skyldes en sjælden genetisk tilstand kaldet arvelig tandkødsfibromatose, som er kendetegnet ved en progressiv forstørrelse af tandkødet. Disse tilfælde kræver normalt kirurgisk indgreb for at fjerne det overskydende fibrotisk tandkødsvæv, men læsionens gentagelse er uforudsigelig. Den fibrotiske natur af disse læsioner sammen med patientens medicinske og familiehistorie kan skelne dem fra lægemiddel -induceret tandkødsovervækst.
ETIOLOGI OG RISIKOFAKTORER
Patogenesen af lægemiddelinduceret ed gingival udvidelse forstås ikke fuldt ud. Det kan skyldes en reduktion af kollagennedbrydning ved collagenase eller resultatet af overproduktion af ekstracellulært grundstof.18,19 Andre mulige veje er tilstedeværelsen af en delmængde af tandkødsfibroblaster, der er genetisk modtagelige for disse medikamenter.20 Johnson et al. Har rapporteret den synergistiske virkning af proinflammatoriske cytokiner (IL-1b og IL-6) i forbedring af kollagensyntese ved humane tandkødsfibroblaster som en anden mulig faktor involveret i denne udvidelse.21
Biofilm er en fælles risikofaktor for alle former af inflammatorisk periodontal sygdom, og dens tilstedeværelse forværrer lægemiddelinduceret tandkødsforstørrelse. Andre risikofaktorer kan omfatte køn, da mænd er tre gange mere tilbøjelige til at udvikle tandkødsovervækst end kvinder.22 Alder er omvendt korreleret med phenytoin- og cyclosporin A-induceret tandkødsforstørrelse, da børn og teenagere har en højere forekomst af disse læsioner end voksne .23 Med hensyn til dosering er der modstridende rapporter om en sammenhæng mellem sværhedsgraden af udvidelsen og den daglige indtagelse af nogen af disse lægemiddelklasser. Størstedelen af rapporterne har ikke fundet en signifikant sammenhæng mellem lægemiddeldosering og sværhedsgraden af tandkødsforstørrelse.18
BEHANDLING
Den mest effektive behandling for lægemiddelinduceret tandkødsforstørrelse er at trække fornærmende stof. Medicinske udbydere kan erstatte CCB’er med betablokkere, diuretika eller angiotensinkonverterende enzymhæmmere, for eksempel – hvoraf ingen påvirker det orale væv. Phenytoin kan erstattes af carbamazepin, ethosuximid eller natriumvalproat. 24 Cyclosporin A kan erstattes med tacrolimus. På trods af disse muligheder er læger og patienter ofte tilbageholdende med at skifte til et andet regime, især når sygdommen er godt kontrolleret, eller andre muligheder allerede er blevet undersøgt. Hvis skift af medicin ikke er en mulighed, kan nogle læsioner håndteres nonsurgically. Mild læsioner af CCB-induceret tandkødsforstørrelse reagerer positivt på skalering og rodplanning og antimikrobielle mundskylle.
God mundhygiejne er afgørende for at forhindre yderligere betændelse og opretholde positive resultater opnået med professionel pleje, herunder periodisk ikke-kirurgisk periodontal behandling.Hvad angår phenytoin-induceret forstørrelse, er tandkødsresponsen på skalering og rodplanning ikke så gunstig på grund af det høje indhold af kollagen i læsionerne, hvilket forhindrer signifikant vævskrympning.
Kirurgiske udskæringer af det forstørrede væv ved tandkødsektomi kan eliminere pseudo-lommer, hvilket genopretter vævsarkitektur, udseende og funktion. Denne procedure udføres med knive, kirurgiske knive, elektrokirurgiske enheder eller lasere (figur 7). Gentagelse af lægemiddelinduceret tandkødsforstørrelse er rapporteret i tilfælde behandlet med enten kirurgiske eller ikke-kirurgiske metoder – især hvis ophør af det krænkende lægemiddel kun var midlertidigt eller ikke en mulighed i første omgang. Gentagelse kan forekomme så tidligt som tre til seks måneder efter interventionen og påvirker så mange som 40% af patienterne.25 Gentagelse er mere almindelig blandt dem med dårlig mundhygiejne eller som mangler adgang til professionel pleje (Figur 8).
Lægemiddelinduceret tandkødsforstørrelse er en almindelig tilstand, der kan være forårsaget af en række forskellige lægemidler. Disse læsioner mangler skelne kliniske markører fra plak-associerede læsioner og kan være vanskelige at diagnosticere. En detaljeret medicinsk historie vil hjælpe klinikere med hensyn til etiologi, diagnose og behandlingsmuligheder for patienter, der præsenterer med lægemiddelinduceret tandkødsforstørrelse.
- Merritt HH, Putnam TJ. Vartegnartikel 17. september 1938: Sodium diphenyl hydantoinate til behandling af krampeanfald. JAMA. 1984; 251: 1062-1067.
- Kimball OP. Behandling af epilepsi med natriumdiphenylhydantoinat. JAMA. 1939; 112: 1244-1245.
- Casetta I, Granieri E, Desidera M, et al. Phenytoin-induceret tandkødsovervækst: En samfundsbaseret tværsnitsundersøgelse i Ferrara, Italien. Neuroepidemiologi. 1997; 16: 296-303.
- Butler RT, Kalkwarf KL, Kaldahl WB. Lægemiddelinduceret tandkødshyperplasi: phenytoin, cyclosporin og nifedipin. J Am Dent Assoc. 1987; 114: 56–60.
- Lederman D, Lumerman H, Reuben S, Freedman PD. Gingival hyperplasi forbundet med nifedipinbehandling. Rapport om en sag. Oral kirurgi Oral Med Oral Pathol. 1984; 57: 620-622.
- Barak S, Engelberg IS, Hiss J. Gingival hyperplasi forårsaget af nifedipin. Histopatologiske fund. J Periodontol. 1987; 58: 639-642.
- Fattore L, Stablein M, Bredfeldt G, Semla T, Moran M, Doherty-Greenberg JM. Gingival hyperplasi: en bivirkning af nifedipin og diltiazem. Spec Care Tandlæge. 1991; 11: 107-109.
- Miller CS, Damm DD. Forekomst af verapamil-induceret tandkødshyperplasi i en tandpopulation. J Periodontol. 1992; 63: 453-456.
- Jorgensen MG. Udbredelse af amlodipin-relateret tandkødshyperplasi. J Periodontol. 1997; 68: 676-678.
- Borel JF, Feurer C, Magnée C, Stähelin H. Virkninger af det nye anti-lymfocytiske peptid cyclosporin A hos dyr. Immunologi. 1977; 32: 1017–1025.
- Rateitschak-Plüss EM, Hefti A, Lörtscher R, Thiel G. Indledende observation, at cyclosporin-A inducerer tandkødsforstørrelse hos mennesker. J Clin periodontol. 1983; 10: 237-246.
- Friskopp J, Klintmalm G. Gingival-udvidelsen. En sammenligning mellem cyclosporin- og azathioprinbehandlede renale allotransplantatmodtagere. Swed Dent J. 1986; 10: 85-96.
- Pernu HE, Pernu LM, Huttunen KR, Nieminen PA, Knuuttila ML. Gingival tilvækst blandt nyretransplantationsmodtagere relateret til immunsuppressiv medicin og mulige lokale baggrundsfaktorer. J Periodontol. 1992; 63: 548–553.
- Keown PA. Nye immunsuppressive strategier. Curr Opin Nephrol Hypertens. 1998; 7: 659–663.
- Marshall RI, Bartold PM. En klinisk gennemgang af lægemiddelinduceret tandkødsovervækst. Aust Dent J. 1999; 44: 219-232.
- Demirer S, Ozdemir H, Sencan M, Marakoglu I. Gingival hyperplasi som en tidlig diagnostisk oral manifestation i akut monocytisk leukæmi: en sagsrapport. Eur J Dent. 2007; 1: 111–114.
- Wu J, Fantasia JE, Kaplan R. Orale manifestationer af akut myelomonocytisk leukæmi: en sagsrapport og gennemgang af klassificeringen af leukæmier. J Periodontol. 2002; 73: 664-668.
- Barclay S, Thomason JM, Idle JR, Seymour RA. Forekomsten og sværhedsgraden af nifedipin-induceret tandkødsovervækst. J Clin periodontol. 1992; 19: 311–314.
- Lucas RM, Howell LP, Wall BA. Nifedipin-induceret tandkødshyperplasi. En histokemisk og ultrastrukturel undersøgelse. J Periodontol. 1985; 56: 211-215.
- Pernu HE, Knuuttila MLE, Huttenen KRH, Tiilikainen ASK. Lægemiddelinduceret tandkødsovervækst og klasse I1 store histokompatibilitetsantigener. Transplantation. 1994; 57: 1811-1813.
- Johnson RB, Zebrowski EJ, Dai X. Synergistisk forbedring af kollagen proteinsyntese ved humane tandkødsfibroblaster eksponeret for nifedipin og interleukin-1-beta in vitro. J Oral Pathol Med. 2000; 29: 8-12.
- Ellis JS, Seymour RA, Steele JG, Robertson P, Butler TJ, Thomason JM. Forekomst af tandkødsovervækst induceret af calciumkanalblokkere: en samfundsbaseret undersøgelse. J Periodontol. 1999; 70: 63–67.
- Daley TD, Wysocki GP, dag C.Kliniske og farmakologiske korrelationer i cyclosporin-induceret tandkødshyperplasi. Oral kirurgi Oral Med Oral Pathol. 1986; 62: 417-421.
- Seymour RA, Smith DG, Turnbull DN. Virkningen af phenytoin og natriumvalproat på parodontal sundhed hos voksne epileptiske patienter. J Clin periodontol. 1985; 12: 413-419.
- Ilgenli T, Atilla G, Baylas H. Effektivitet af periodontal behandling hos patienter med lægemiddelinduceret tandkødsovervækst. Langsigtede resultater. J Periodontol. 1999; 70: 967–972.