Caso clínico
Se presentó una mujer de 45 años con una historia de 20 años de enfermedad de Crohn. con fiebre, escalofríos y fatiga durante 10 días. Poco antes del inicio de los síntomas, la paciente se sometió a una colonoscopia sin complicaciones durante la cual se le realizaron 17 biopsias para vigilancia o polipectomía. Durante la colonoscopia, la enfermedad de Crohn estaba en remisión y no se observó inflamación de la mucosa.
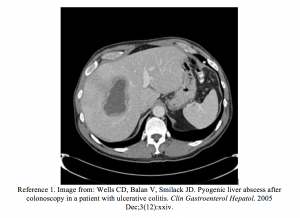
En el servicio de urgencias, los signos vitales de la paciente eran HR 110, BP 120/80, RR 18, T 102,5. Tenía dolor leve en el abdomen superior derecho. Los estudios de laboratorio revelaron un recuento elevado de glóbulos blancos (15.000) y AST y ALT elevados (120/137 U / L), con fosfatasa alcalina ligeramente elevada de 200 UI / L. Una tomografía computarizada (TC) del abdomen reveló múltiples áreas de baja atenuación en el lóbulo hepático derecho compatibles con abscesos hepáticos. Se cultivó el drenaje de los abscesos y creció Streptococcus anginosus. La resolución de todas las lesiones se produjo después de que se drenaron mediante radiología intervencionista y se administró al paciente un ciclo de antibióticos intravenosos durante 6 semanas.
Introducción
La colonoscopia es un procedimiento que se realiza comúnmente en el diagnóstico y tratamiento de una amplia gama de afecciones, que incluyen cáncer, enfermedades inflamatorias del intestino, pólipos, hemorragias y estenosis. Según la Sociedad Estadounidense del Cáncer, la colonoscopia de detección se recomienda cada 10 años a partir de los 50 años.1 En pacientes de alto riesgo, como aquellos con enfermedad inflamatoria intestinal, la colonoscopia se realiza con más frecuencia. El procedimiento sigue siendo la forma más eficaz de encontrar y extirpar pequeños pólipos precancerosos y, por lo tanto, disminuir el riesgo de muerte por cáncer de colon y recto.
En general, la colonoscopia es muy segura. Una revisión sistemática de 2008 de 12 estudios que totalizaron 57.742 colonoscopias realizadas para la detección de riesgo promedio mostró una tasa general de eventos adversos graves de solo 2.8 por cada 1000 procedimientos y una mortalidad del 0.007%. son más comunes que otros. Los adultos mayores tienen un mayor riesgo de sufrir complicaciones graves en comparación con los pacientes más jóvenes. En un estudio de 53.220 colonoscopias, los pacientes de 80 a 84 años tuvieron una tasa significativamente mayor de complicaciones graves en comparación con los pacientes de 66 a 69 años. El riesgo de complicaciones graves también aumentó entre los pacientes con afecciones comórbidas, como antecedentes de accidente cerebrovascular, EPOC, fibrilación auricular e insuficiencia cardíaca.
El absceso hepático piógeno (PLA) es una complicación rara pero grave de la colonoscopia . La mayoría de las complicaciones de la colonoscopia se presentarán dentro de los 7 días, pero el PLA puede presentarse días o incluso semanas después de eso, y es posible que ni siquiera se obtengan los antecedentes de una colonoscopia reciente a menos que el médico tenga conocimiento de esta entidad.4-6 Debido a la naturaleza tardía de PLA, es probable que estos pacientes sean diagnosticados en el departamento de emergencias.
Otras complicaciones tardías como el síndrome de electrocoagulación pospolipectomía y los problemas más comunes de hemorragia tardía, dolor abdominal inespecífico, reacciones a agentes sedantes , y la perforación también se puede ver en el servicio de urgencias. Por el contrario, la explosión de gas o el sangrado inmediato rara vez se observarán en el servicio de urgencias, ya que estos problemas suelen presentarse rápidamente en la sala de endoscopia, donde se abordan de forma urgente. Los médicos de urgencias deben estar al tanto de todas las posibles complicaciones y su evolución temporal y tener las herramientas para diagnosticar y tratar correctamente al desafortunado paciente poscolonoscopia que sufre una complicación grave.
Complicaciones
Piógeno Absceso hepático
El PLA es una enfermedad peligrosa con alta morbilidad y mortalidad que se presenta a una tasa de 10 a 20 casos por cada 100.000 ingresos hospitalarios.4-6 Con los avances en las técnicas de diagnóstico e intervenciones, la mortalidad está mejorando7. Sin embargo, los pacientes todavía están en grave peligro, especialmente si el diagnóstico se retrasa, como suele ocurrir, porque los pacientes pueden presentarse de manera inespecífica. Un estudio retrospectivo de 63 pacientes con PLA mostró que la fiebre era común (59%), pero otros signos y síntomas como dolor en el cuadrante superior derecho y signos peritoneales estaban presentes en solo 39% y 14%, respectivamente.8 El diagnóstico en este estudio fue a menudo se retrasa un promedio de una semana desde el inicio de los síntomas.
La colonoscopia es un desencadenante de PLA poco frecuente pero probablemente poco reconocido. Se cree que las microperforaciones silenciosas durante el procedimiento provocan una infección que puede sembrar el hígado a través de la circulación portal. De manera similar, otras infecciones intraabdominales, como la diverticulitis, pueden potencialmente causar PLA si el área infectada es drenada por la vena porta.9 El aclaramiento hepático de bacterias a través de la red portal es un fenómeno normal en pacientes sanos, pero la obstrucción biliar, la mala perfusión y la alta carga bacteriana (como en el caso de una infección o múltiples biopsias durante la colonoscopia sembrando el torrente sanguíneo) pueden predisponer a la proliferación y al absceso. formación. La literatura describe aproximadamente el 34% de los casos de PLA como criptogénicos, pero una parte de estos bien pueden ser pacientes con una colonoscopia reciente que no fue reconocida como un factor de riesgo para el proceso de la enfermedad.8
La mayoría de los aislados de PLA son polimicrobianos y compuesto por flora entérica normal. Los hemocultivos son positivos en el 33-65% de los casos, pero los cultivos de abscesos son casi todos positivos.10 Los microorganismos aislados con mayor frecuencia son especies de Streptococcus (37%), Eserichia Coli (33%), especies de Bacteroides (24%), Klebsiella pneumoniae (18%) y estreptococos microaerófilos (12%). 10-11 El estreptococo anginoso, encontrado en el caso de este paciente, es un coco grampositivo anaerobio facultativo y uno de los organismos más comunes que se encuentran en el PLA.
El diagnóstico oportuno de PLA es fundamental, porque incluso a medida que mejoran el diagnóstico y la terapia, la mortalidad permanece en el 10% .5,7 Las complicaciones infecciosas de la colonoscopia en general son raras, pero de nuevo, la relación causal probablemente tampoco se reconoce. La colonoscopia se ha implicado en al menos algunos casos de PLA.12-14 Pero la bacteriemia sistémica transitoria, que se observa en el 4% de las colonoscopias, no parece aumentar el riesgo de infección per se.15 Más bien, se cree que la infección en PLA se propaga a través de microperforaciones reales.
Si bien se sabe que las perforaciones francas son relativamente raras (menos del 0,1% de las colonoscopias), la incidencia y la fisiopatología de las microperforaciones no se conocen por completo16-17. entidad, un médico que obtiene una buena historia y tiene un alto índice de sospecha puede diagnosticar más rápidamente PLA en un paciente con colonoscopia reciente.
Infección
Se acepta comúnmente que la bacteriemia transitoria después de la colonoscopia ocurre en aproximadamente el 4% de los procedimientos, aunque el rango se informa como 0-25%, y los factores de riesgo de bacteriemia no están definidos.18 Se producen tasas más altas de bacteriemia durante las actividades diarias de rutina, como cepillarse los dientes y masticar alimentos. Aunque los signos o síntomas de infección sistémica en pacientes con bacteriemia transitoria son raros, los pacientes pueden sentir fiebre, escalofríos y quejas que imitan todo, desde infecciones respiratorias superiores hasta infecciones abdominales.18
Aunque la bacteriemia transitoria es un riesgo aceptado de la colonoscopia , no hay ningún beneficio comprobado para la profilaxis antibiótica de rutina, y la mayoría de los pacientes no habrán tomado antibióticos antes del procedimiento.18 Las pautas actuales de la Sociedad Estadounidense de Gastroenterología (ASGE) están de acuerdo con la Asociación Estadounidense del Corazón (AHA) y recomiendan contra la profilaxis antibiótica para pacientes sometidos a una colonoscopia de rutina.19
Puede ser difícil diferenciar los síntomas de bacteriemia transitoria de una infección verdadera.18 En general, los pacientes con síntomas infecciosos en los días posteriores a la colonoscopia justifican estudios de laboratorio que incluyan hemocultivos y, según índice de sospecha de perforación, imagenología abdominal.20-21 Si la sospecha de perforación es baja o el diagnóstico Si el estado clínico del paciente lo justifica, se puede administrar hidratación intravenosa y antibióticos.
Sangrado
El sangrado pospolipectomía puede ser inmediato o retrasado. El sangrado inmediato se asocia con técnicas de polipectomía que no usan cauterio o cuando se usa corriente mezclada para el procedimiento. El sangrado tardío se observa con más frecuencia en el servicio de urgencias, ya que el sangrado inmediato a menudo se detecta en el momento del procedimiento y el endoscopista lo trata. Se puede observar un sangrado tardío hasta 7 días después del procedimiento. Se cree que ocurre debido al desprendimiento de una escara que cubría un vaso sanguíneo o debido a la extensión de la zona de necrosis térmica a tejido no lesionado, lo que podría resultar en sangrado si involucra un vaso sanguíneo19,22
Varios estudios grandes han reportado hemorragia en 1 a 6 por 1000 colonoscopias (0.1% -0.6%). 22 Sin embargo, un estudio que analizó más de 50,000 colonoscopias encontró que la tasa de hemorragia GI fue significativamente diferente dependiendo de si se realizó polipectomía. El sangrado pospolipectomía ocurre en 1-2%, con tasas más altas observadas con la extirpación de pólipos más grandes. El riesgo de hemorragia pospolipectomía puede aumentar en pacientes con trombocitopenia o coagulopatías.23
Los factores de riesgo conocidos de hemorragia poscolonoscopia incluyen el tamaño del pólipo, la cantidad de pólipos extirpados, antecedentes de uso reciente de anticoagulantes o pólipos. histología.22 Curiosamente, múltiples estudios grandes no encontraron el uso de aspirina asociado con hemorragia pospolipectomía.24-26
Los pacientes con hemorragia tardía pueden presentar cualquier signo de hemorragia o anemia, incluyendo fatiga, debilidad , palidez, sangrado abundante o coágulos al limpiarse, taquicardia, dolor de pecho y dificultad para respirar.Los pacientes pueden describir hematoquecia o melena, dependiendo de la ubicación de la hemorragia.
El tratamiento inicial de un paciente con sospecha de hemorragia incluye tratar las vías respiratorias básicas, la respiración y la circulación con 2 IV de gran calibre, líquidos cristaloides y monitorización cardíaca. Los pacientes con hemorragia digestiva baja grave pueden descompensarse rápidamente y deben tener un tipo activo y una prueba de detección en caso de que se requiera una transfusión.
No siempre es necesario obtener imágenes y, si es posible, la decisión de realizar la imagen debe tomarse junto con la prueba gastrointestinal. consultar, preferiblemente al médico que realizó la colonoscopia. La colonoscopia repetida es a menudo el procedimiento diagnóstico y terapéutico de elección. El Colegio Americano de Radiología otorga la calificación más alta de adecuación a la colonoscopia, aunque también incluye la ATC del abdomen / pelvis y la exploración del abdomen / pelvis con Tc-99m RBC como posibles pasos apropiados en el diagnóstico.27
Si el paciente es inestable y el endoscopista que lo realiza no está disponible, el médico de urgencias debe consultar radiología intervencionista general (RI), GI y cirugía.
Perforación
La perforación colonoscópica (PC) es una de las las complicaciones más graves y temidas de la colonoscopia. Aunque es poco común, la PC produce una alta morbilidad y mortalidad28-32. La perforación puede resultar de fuerzas mecánicas contra la pared intestinal, barotrauma o electrocauterio y puede conducir a la formación de abscesos, fístulas, sepsis intraabdominal, estancia hospitalaria prolongada e incluso muerte.
La parálisis cerebral ocurre en aproximadamente el 0.016% de las colonoscopias de diagnóstico, pero se puede observar hasta en el 5% de las colonoscopias terapéuticas.33-35 Dependiendo de lo que se haya hecho realmente durante la colonoscopía, el riesgo de perforación puede ser mayor o más bajo que el promedio, por lo que obtener el informe quirúrgico o el historial del endoscopista puede ser útil para determinar el riesgo.
Riesgo de PC para diversos procedimientos colonoscópicos: 1,36-37
-Colonoscopia de cribado: 0,01-0,1%
-Dilatación de la estenosis anastomótica: 0-6%
-Dilatación de la estenosis de la enfermedad de Crohn: 0-18%
-Stent Colocación: 4%
-Colocación del tubo de descompresión colónico: 2%
-Resección endoscópica de mucosa colónica 0-5%
Aparte de los eventos durante el procedimiento, los factores de riesgo específicos de parálisis cerebral incluyen edad avanzada, comorbilidades múltiples, diverticulosis, obstrucción, resección de pólipos, pólipos de más de 1 cm de tamaño o los que se encuentran en el colon derecho, movilidad reducida del colon, debilidad existente en la pared colónica , intento previo incompleto de colonoscopia, o inexperiencia del endoscopista.20
Los pacientes con PC pueden presentar un dolor abdominal repentino que empeora, seguido de una disipación completa y falsamente tranquilizadora del dolor a medida que la perforación descomprime el órgano inflamado. A medida que el contenido GI continúa derramándose en el peritoneo, se desarrolla un empeoramiento del dolor y los síntomas peritoneales. Sin embargo, los síntomas variarán según la ubicación y el tamaño de la perforación, el grado de filtración fecal en el peritoneo y la edad del paciente y las comorbilidades.
En particular, las perforaciones también pueden ser retroperitoneales, correspondientes a la ubicación del colon ascendente y descendente y de los ángulos hepático y esplénico. Aunque el síntoma más común de una perforación colónica es el dolor abdominal, los pacientes ancianos pueden tener una respuesta embotada. Otros síntomas incluyen fiebre, náuseas, vómitos, disnea, dolor de pecho, dolor escapular y dolor de cuello. Las perforaciones retroperitoneales en particular pueden tener síntomas mínimos o atípicos, y los signos vitales pueden mostrar taquicardia y fiebre, pero también pueden ser normales.20
El manejo inicial de una perforación sospechada incluye atención a las vías respiratorias, respiración, circulación con 2 IV de gran calibre, líquidos cristaloides y monitor cardíaco. Deben obtenerse análisis de laboratorio que incluyan CBC, CMP, lipasa y el tipo y la detección. El paciente debe ser estrictamente NPO con antibióticos intravenosos empíricos. Se deben solicitar imágenes estadísticas con tomografía computarizada del abdomen / pelvis o radiografía abdominal, si es inestable, junto con una consulta quirúrgica.21
Síndrome pospolipectomía
Síndrome pospolipectomía, también conocido como El síndrome de electrocoagulación pospolipectomía o síndrome de quemadura transmural, es el resultado de una lesión por electrocoagulación en la pared intestinal, que crea una quemadura transmural y una peritonitis focal sin perforación franca38. La incidencia informada varía de 3 por 100.000 (0,003%) a 1 en 1000 (0,1%). ). Se notificó síndrome pospolipectomía en 6 pacientes de las 16,318 colonoscopias realizadas entre 1994 y 2002 en un gran sistema de salud integrado39. Se desconocen los factores de riesgo de esta complicación poco común.
Los pacientes con síndrome pospolipectomía suelen presentar dentro de las 12 horas posteriores a la colonoscopia con fiebre, taquicardia y dolor abdominal. Sin embargo, la aparición de los síntomas puede retrasarse hasta 5-7 días después del procedimiento40. Los pacientes a menudo tienen leucocitosis y pueden presentar rigidez y taquicardia, todas las cuales imitan una perforación colónica.41
Sin embargo, a diferencia de la perforación, que puede requerir cirugía de urgencia, los pacientes con síndrome pospolipectomía generalmente se tratan de forma conservadora con líquidos intravenosos, control del dolor y avance gradual de la dieta, con o sin antibióticos dirigidos a gram- patógenos negativos y anaeróbicos.42 Los casos menos graves incluso pueden tratarse de forma ambulatoria con antibióticos orales y líquidos claros durante 1 a 2 días.42-43
Como estos pacientes pueden ser indistinguibles de los pacientes con perforación, cualquier paciente con sospecha de síndrome pospolipectomía requiere exámenes de laboratorio e imágenes. En el síndrome pospolipectomía, la tomografía computarizada generalmente mostrará un engrosamiento focal de la pared colónica con hebras de grasa circundante sin aire extramural, aunque en casos leves, la tomografía computarizada puede ser negativa42. Si se sospecha, el paciente debe tener una consulta quirúrgica.
Perlas
- La colonoscopia es una prueba de detección ampliamente utilizada en pacientes mayores de 50 años. Las complicaciones pueden ser tempranas o tardías. Los médicos de emergencias médicas deben conocer las posibles complicaciones y su cronograma esperado para poder diagnosticar y manejar con precisión cualquier posible complicación que se presente.
- Las complicaciones incluyen hemorragia, perforación, síndrome pospolipectomía, infección, explosión de gas y absceso hepático piógeno.
- Los antecedentes sobre los factores del paciente y el procedimiento en sí (afecciones subyacentes, medicamentos, si se extirparon pólipos, si se usó cauterio, si hubo sangrado inmediato) pueden orientar el diagnóstico y el manejo en el servicio de urgencias.
- El absceso hepático piógeno puede presentarse de 1 a 2 semanas después de la colonoscopia con dolor en el cuadrante superior derecho y fiebre.
- Gran parte del colon es retroperitoneal. Las perforaciones retroperitoneales pueden causar síntomas vagos y atípicos, por lo que el índice de sospecha debe ser alto.
- El síndrome pospolipectomía puede simular una perforación y generalmente se puede diferenciar mediante imágenes.
Referencias / lectura adicional:
- Wells CD, Balan V, Smilack JD. Absceso hepático piógeno tras colonoscopia en un paciente con colitis ulcerosa. Clin Gastroenterol Hepatol. 2005 Dec; 3 (12): xxiv.
- Whitlock, E.P., Lin, J.S., Liles, E. et al. Detección de cáncer colorrectal: una revisión sistemática actualizada y dirigida para el Grupo de Trabajo de Servicios Preventivos de EE. UU. Ann Intern Med. 2008; 149: 638–658.
- Warren JL, Klabunde CN, Mariotto AB, Meekins A, Topor M, Brown ML, Ransohoff. Eventos adversos después de una colonoscopia ambulatoria en la población de Medicare. Ann Intern Med. 2009; 150 (12): 849.
- Johannsen EC, Sifri CD, Madoff LC. Abscesos hepáticos piógenos Infectar Dis Clin North Am. 2000; 14: 547–63.
- Meddings L, Myers RP, Hubbard J, et al. Un estudio poblacional de abscesos hepáticos piógenos en los Estados Unidos: incidencia, mortalidad y tendencias temporales. Soy J Gastroenterol. 2010; 105: 117–24.
- Kaplan GG, Gregson DB, Laupland KB. Estudio poblacional de la epidemiología y los factores de riesgo del absceso hepático piógeno. Clin Gastroenterol Hepatol. 2004; 2: 1032-8.
- Petri A, Höhn J, Hódi Z, Wolfárd A, Balogh A. Absceso hepático piógeno – 20 años de experiencia. Comparación de resultados de tratamiento en dos períodos. Langenbecks Arch Surg. 2002; 387: 27–31.
- Pang TC, Fung T, Samra J, Hugh TJ, Smith RC. Absceso hepático piógeno: una auditoría de 10 años de experiencia. Mundial J Gastroenterol. 2011; 17: 1622–30.
- Murarka S, Pranav F, Dandavate V. DisseminatedStreptococcus anginosus de la diverticulitis sigmoidea. J Glob Infect Dis. 2011; 3: 79–81.
- Branum GD, Tyson GS, Branum MA, Meyers WC. Absceso hepático Cambios en la etiología, el diagnóstico y el manejo. Ann Surg. 1990 Dic. 212 (6): 655-62.
- Gyorffy EJ, Frey CF, Silva J Jr, McGahan J. Absceso hepático piógeno. Estrategias diagnósticas y terapéuticas. Ann Surg. 1987 Dec. 206 (6): 699-705.
- Bonenfant F, Rousseau É, Farand P. Absceso hepático por Streptococcus anginosuspyogenic después de una colonoscopia de detección. Revista canadiense de enfermedades infecciosas & Microbiología médica. 2013; 24 (2): e45-e46.
- Ian G. Harnik. Absceso hepático piógeno que se presenta después de polipectomía maligna.Dig Dis Sci. 2007; 52: 3524–5.
- Paraskeva KD, Bury RW, Isaacs P.Streptococcus milleri Abscesos hepáticos: una complicación inusual después de la extirpación colonoscópica de una espina de pescado impactada. Gastrointest Endosc. 2000; 51: 357–8.
- Baja DE, Shoenut JP, Kennedy JK, et al. Evaluación prospectiva del riesgo de bacteriemia con colonoscopia y polipectomía. Dig Dis Sci. 1987; 32: 1239–43.
- Becker F, Nusko G, Welke J, Hahn EG, Mansmann U. Seguimiento después de polipectomía colorrectal: análisis de beneficio-riesgo de las recomendaciones de vigilancia alemanas. Int J Colorrectal Dis. 2007; 22: 929–39.
- Macrae FA, Tan KG, Williams CB. Hacia una colonoscopia más segura: informe sobre las complicaciones de 5000 colonoscopias diagnósticas o terapéuticas. Intestino. 1983; 24: 376–83.
- Nelson, D.B.Complicaciones de enfermedades infecciosas de la endoscopia GI: parte II, infecciones exógenas. Gastrointest Endosc. 2003; 57: 695–711.
- Khashab, M.A., Chithadi, K.V., Acosta, R.D. et al. Profilaxis antibiótica para endoscopia GI. Comité de Estándares de Práctica de ASGE. Gastrointest Endosc. 2015; 81: 81-89.
- Lohsiriwat V. Perforación colonoscópica: Incidencia, factores de riesgo, manejo y resultado. Revista mundial de gastroenterología: WJG. 2010; 16 (4): 425-430.
- Criterios de adecuación del ACR del American College of Radiology: agudo (no localizado)
- Ko, C.W. y Dominitz, J.A. Complicaciones de la colonoscopia: magnitud y manejo. Gastrointest Endosc Clin N Am. 2010; 20: 659–671.
- Warren JL, Klabunde CN, Mariotto AB, et al. Eventos adversos después de una colonoscopia ambulatoria en la población de Medicare. Ann Intern Med 2009; 150: 849-57.
- Hui, A.J., Wong, R.M., Ching, J.Y. et al. Riesgo de hemorragia por polipectomía colonoscópica con anticoagulantes y antiagregantes plaquetarios: análisis de 1657 casos. Gastrointest Endosc. 2004; 59: 44–48.
- Sawhney, M.S., Salfiti, N., Nelson, D.B. et al. Factores de riesgo de hemorragia pospolipectomía tardía grave. Endoscopia. 2008; 40: 115-119
- Yousfi, M., Gostout, C.J., Baron, T.H. et al. Hemorragia digestiva baja pospolipectomía: papel potencial de la aspirina. Soy J Gastroenterol. 2004; 99: 1785–1789.
- Criterios de idoneidad del ACR del American College of Radiology: Manejo radiológico del sangrado del tracto gastrointestinal inferior. https://acsearch.acr.org/docs/69457/Narrative/ (Consultado el 16 de julio de 2017).
- Lohsiriwat V, Sujarittanakarn S, Akaraviputh T, Lertakyamanee N, Lohsiriwat D, Kachinthorn U. Perforación colonoscópica: un informe del centro de formación en endoscopia de la Organización Mundial de Gastroenterología en Tailandia. Mundial J Gastroenterol. 2008; 14: 6722–6725.
- Iqbal CW, Cullinane DC, Schiller HJ, Sawyer MD, Zietlow SP, Farley DR. Manejo quirúrgico y resultados de 165 perforaciones colonoscópicas de una sola institución. Arch Surg. 2008; 143: 701–706; discusión 706-707.
- Teoh AY, Poon CM, Lee JF, Leong HT, Ng SS, Sung JJ, Lau JY. Resultados y predictores de mortalidad y formación de estomas en el manejo quirúrgico de perforaciones colonoscópicas: una revisión multicéntrica. Arch Surg. 2009; 144: 9–13.
- Lüning TH, Keemers-Gels ME, Barendregt WB, Tan AC, Rosman C. Perforaciones colonoscópicas: una revisión de 30,366 pacientes. Surg Endosc. 2007; 21: 994–997.
- Mai CM, Wen CC, Wen SH, Hsu KF, Wu CC, Jao SW, Hsiao CW. Perforación de colon iatrogénica por colonoscopia: una complicación fatal para pacientes con alto riesgo anestésico. Int J Colorrectal Dis. Abril de 2010; 25 (4): 449-54.
- Rathgaber SW, Wick TM. Tasas de finalización y complicaciones de la colonoscopia en una práctica comunitaria de gastroenterología. Gastrointest Endosc. 2006; 64: 556–562.
- Damore LJ, Rantis PC, Vernava AM, Longo WE. Perforaciones colonoscópicas. Etiología, diagnóstico y manejo. Dis Colon Rectum. 1996; 39: 1308–1314.
- Repici A, Pellicano R, Strangio G, Danese S, Fagoonee S, Malesci A. Resección endoscópica de la mucosa para la neoplasia colorrectal temprana: bases patológicas, procedimientos y resultados. Dis Colon Rectum. 2009; 52: 1502–1515.
- Chukmaitov A, Bradley CJ, Dahman B, et al. Asociación de técnicas de polipectomía, volumen endoscopista y tipo de instalación con complicaciones de la colonoscopia. Gastrointest Endosc. 2013; 77: 436.
- Fisher DA, Maple DT, et al. Complicaciones de la colonoscopia. Comité de Estándares de Práctica de la ASGE Gastrointest Endosc. 2011; 74: 745. Dolor abdominal y fiebre o sospecha de absceso abdominal; Variante 1: Paciente postoperatorio con fiebre. https://acsearch.acr.org/docs/69356/Narrative/ (Consultado el 17 de julio de 2017).
- Hirasawa K, Sato C, Makazu M, et al. Síndrome de coagulación: perforación tardía después de tratamientos endoscópicos colorrectales. Revista mundial de endoscopia gastrointestinal. 2015; 7 (12): 1055-1061.
- Levin TR, Zhao W, Conell C, Seeff LC, Manninen DL, Shapiro JA, Schulman J. Complications of colonoscopy in an Integrated Health Care System. Ann Intern Med. 2006; 145 (12): 880.
- Kim HW. ¿Cuál es la diferencia entre la fiebre pospolipectomía y el síndrome de coagulación pospolipectomía? Clin Endosc. 2014; 47 (3): 205–6.
- Stock C, Ihle P, Sieg A, Schubert I, Hoffmeister M, Brenner H Eventos adversos que requieren hospitalización dentro de los 30 días posteriores a la detección ambulatoria y colonoscopias sin detección. Gastrointest Endosc. 2013 Mar; 77 (3): 419-29.
- Sethi A, Song LMWK. Eventos adversos relacionados con la resección endoscópica de la mucosa colónica y la polipectomía. Gastrointest Endosc Clin N Am. 2015; 25 (1): 55–69.
- Benson BC, Myers JJ, Laczek JT. Síndrome de electrocoagulación pospolipectomía: un imitador de la perforación colónica. Representante de caso Emerg Med. 2013; 2013 687931.