US Pharm. 2018; 43 (7): 22-26.
SOMMARIO: Le statine sono una classe di farmaci ampiamente utilizzati per la prevenzione primaria e secondaria degli eventi cardiovascolari. Con sei statine disponibili genericamente, la selezione di un agente appropriato può essere determinata in base a fattori specifici del farmaco, comprese considerazioni sul dosaggio, interazioni farmacologiche ed eventi avversi. È possibile sviluppare piani di cura del paziente personalizzati sulla base di dati provenienti da importanti studi clinici, differenze nelle linee guida e attuali raccomandazioni per la gestione di due eventi avversi principali associati all’uso di statine.
La pietra angolare del trattamento della dislipidemia implica l’uso di Inibitori della 3-idrossi-3-metilglutaril-coenzima A reduttasi, più comunemente noti come statine. Con una varietà di opzioni generiche sul mercato e forti prove a sostegno del loro uso, le statine sono alcuni dei farmaci più ampiamente prescritti al mondo.1 Tuttavia, l’uso frequente di questi agenti ha portato a un controllo continuo della loro sicurezza e al dibattito in corso sulla loro ruolo nella terapia. Questo articolo, che si concentra sulle statine generiche, metterà in evidenza il dibattito sul ruolo delle statine nella terapia, discuterà del corretto utilizzo ed esplorerà le prove che circondano due principali eventi avversi.
Delle sette diverse statine sul mercato, sei sono disponibili genericamente (TABELLA 1) .2-7 Tre formulazioni di marca disponibili sono pitavastatina (Livalo), simvastatina sospensione orale (FloLipid) e lovastatina a rilascio prolungato (Altoprev) .8-10 Il ruolo degli agenti di marca nella terapia è limitato dato l’ampia disponibilità di opzioni generiche.
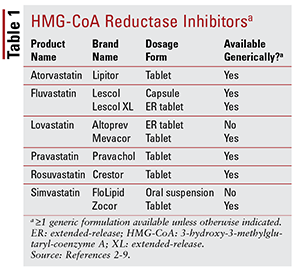
Atorvastatina e simvastatina sono anche disponibili genericamente in diversi prodotti combinati. Questi includono la combinazione di atorvastatina e amlodipina, un bloccante dei canali del calcio (CCB) indicato per l’ipertensione, e la combinazione di simvastatina ed ezetimibe, un inibitore dell’assorbimento del colesterolo intestinale indicato anche per l’ipercolesterolemia.11,12 Statine co-formulate e prodotti a base di niacina (niacina / lovastatina e niacina / simvastatina) sono state rimosse dal mercato nel 2016 sulla base della mancanza di prove che l’aggiunta di niacina nei pazienti trattati con statine riduce ulteriormente gli esiti cardiovascolari (CV) oltre a quanto visto con le statine da sole.13
RACCOMANDAZIONI PER IL TRATTAMENTO
Le statine si sono ripetutamente dimostrate efficaci per ridurre i livelli di colesterolo LDL (LDL-C) e trigliceridi mentre aumentavano i livelli di colesterolo HDL (HDL-C ).14 Inoltre, hanno dimostrato di migliorare significativamente esiti orientati al paziente, come eventi cardiovascolari maggiori (CVE), sia nella prevenzione primaria che secondaria.15-19
Diverse linee guida terapeutiche molto dibattute discutono il ruolo delle statine nel trattamento della hy perlipidemia. Queste includono le linee guida dell’American College of Cardiology / American Heart Association (ACC / AHA) del 2013 e le linee guida dell’American Academy of Clinical Endocrinology (AACE) del 2017.14,20 Entrambe le linee guida suggeriscono che dopo l’implementazione di modifiche dello stile di vita, inclusa la cessazione del fumo, l’adesione a un regime di esercizio fisico e seguendo una dieta salutare per il cuore, le statine sono la terapia di prima linea per la prevenzione primaria e secondaria della malattia cardiovascolare (CVD) .14,20 Le linee guida differiscono, tuttavia, nel modo in cui determinare quali statine sono appropriate per quale pazienti.
La linea guida ACC / AHA del 2013 ha introdotto quattro gruppi di trattamento da prendere di mira per la terapia con statine:
1. Pazienti con precedente CVD aterosclerotica (ASCVD), compresi quelli con un evento precedente (cioè, sindromi coronariche acute, storia di infarto miocardico, angina stabile o instabile, rivascolarizzazione coronarica o altra arteriosa, ictus, attacco ischemico transitorio o malattia arteriosa periferica presunta origine aterosclerotica).
2. Pazienti senza storia di un evento ASCVD che hanno un livello di C-LDL di 190 mg / dL o superiore. L’età non è una base per l’esclusione da questo criterio.
3. Pazienti di età compresa tra 40 e 75 anni con diabete ma senza storia di un evento ASCVD e un livello di LDL-C tra 70 e 189 mg / dL. Pazienti di età compresa tra 40 e 75 anni senza diabete che non hanno una storia di un evento ASCVD e un livello di C-LDL compreso tra 70 e 189 mg / dL.20
La linea guida ACC / AHA ha anche introdotto l’idea di raggruppare le statine per intensità (cioè, la loro capacità prevista di abbassare il C-LDL) (TABELLA 2) .20 Sulla base del gruppo di trattamento (come definito sopra), la linea guida raccomanda intensità specifiche di statine per particolari situazioni cliniche (TABELLA 3) .20 Diversi gruppi di trattamento richiedono il calcolo di un punteggio di rischio ASCVD utilizzando uno stimatore di rischio ASCVD. Questo strumento online tiene conto dell’età, del sesso, della razza, della pressione arteriosa sistolica, del colesterolo totale, del C-HDL e della storia medica del paziente significativa per il trattamento dell’ipertensione, del diabete o del fumo.21 Una volta inseriti tutti gli input, i 10 del paziente -Viene calcolato il rischio annuale di un evento ASCVD.
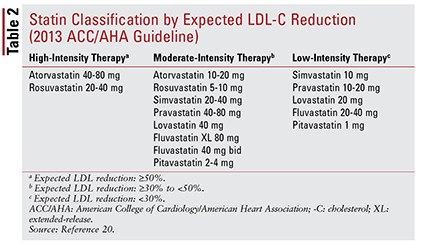
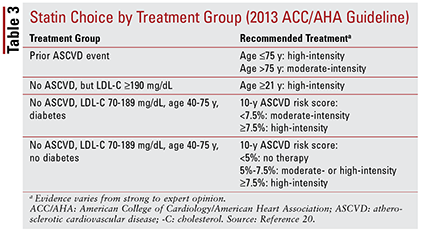
Queste raccomandazioni non si applicano automaticamente a determinati sottogruppi di pazienti. Ad esempio, l’uso di statine negli anziani dovrebbe essere affrontato con cautela. Sebbene l’uso di statine per la prevenzione secondaria nei pazienti anziani conferisca un beneficio significativo, il suo uso per la prevenzione primaria non è chiaro.22-24 Inoltre, non è stato riscontrato che i pazienti con insufficienza cardiaca sperimentino gli stessi benefici dalla terapia con statine di quelli senza insufficienza cardiaca.25 in base a questi risultati, le raccomandazioni per il trattamento includono la limitazione dell’inizio di statine ad alta intensità a pazienti di età inferiore ai 75 anni e possibilmente la prevenzione di statine in pazienti con insufficienza cardiaca.20 Nel complesso, la decisione di utilizzare statine in questi gruppi non è chiara e dovrebbe coinvolgere una conversazione in corso tra fornitore e paziente sui potenziali rischi e benefici della terapia.20
Contrariamente alla raccomandazione ACC / AHA del 2013 di iniziare la terapia secondo la classificazione del gruppo di trattamento, la linea guida AACE 2017 raccomanda che i singoli pazienti siano trattati sulla base dei risultati di laboratorio.14 Secondo questa linea guida, il rischio del paziente è determinato da una varietà di fattori principali, aggiuntivi, a e fattori di rischio non tradizionali. Gli individui vengono quindi classificati in uno dei cinque gruppi a rischio, ciascuno con un obiettivo di C-LDL e non-C-HDL corrispondente (TABELLA 4). Sulla base dei livelli attuali e degli obiettivi individualizzati, le statine da sole o in combinazione con altri agenti devono essere iniziate in base alla capacità prevista di abbassare il C-LDL o non-HDL-C.14

Il trattamento di combinazione che prevede l’aggiunta di un secondo agente alla terapia in corso con statine rimane un argomento alquanto controverso. Mentre studi e linee guida precedenti hanno ridotto al minimo l’aggiunta di altri agenti alla terapia di base con statine, studi recenti e dichiarazioni di consenso, tra cui uno dell’ACC / AHA, supportano l’uso di ezetimibe, evolocumab o alirocumab, gli ultimi due dei quali sono la proproteina convertasi subtilisina / kexin tipo 9 inibitori, come terapia aggiuntiva per la prevenzione secondaria.20,26-31 Detto questo, le statine rimangono la terapia di prima linea universale sia nella prevenzione primaria che in quella secondaria; il ruolo definitivo di altri agenti specifici rimane poco chiaro.
SELEZIONE DELLE STATINE
La scelta della terapia con statine inizia con l’approccio terapeutico preferito dal medico, sia che si tratti del metodo ACC / AHA di trattamento con statine gruppi o il metodo AACE di obiettivi LDL-C o non-HDL-C. Da lì, le proprietà di ciascuna statina devono essere prese in considerazione per determinare l’opzione migliore per il singolo paziente. Non tutte le statine sono uguali ed esistono diverse differenze chiave che possono influenzare la selezione dei pazienti, comprese considerazioni sul dosaggio, interazioni farmacologiche ed eventi avversi (EA).
Dosaggio
Sebbene la maggior parte delle statine possa essere assunta indipendentemente dai pasti, la lovastatina a rilascio immediato (IR) deve essere assunta con il pasto serale a causa della maggiore biodisponibilità.4 Tuttavia, è vero il contrario per la lovastatina a rilascio prolungato, che non deve essere assunta con il cibo a causa della ridotta biodisponibilità. .8 Inoltre, sebbene tutte le statine possano essere somministrate una volta al giorno, fluvastatina IR e lovastatina possono richiedere il dosaggio due volte al giorno.3,4 Infine, mentre atorvastatina, pravastatina e rosuvastatina possono essere somministrate in qualsiasi momento della giornata, fluvastatina, lovastatina e La simvastatina deve essere assunta la sera.3,4,7 La simvastatina, in particolare, ha dimostrato di avere un’efficacia significativamente diversa se assunta la sera rispetto alla mattina.32
Interazioni farmacologiche
Ogni statina è diversa preoccupazioni riguardanti le interazioni farmaco-farmaco e farmaco-cibo a causa delle specifiche vie attraverso le quali ciascuna viene metabolizzata (TABELLA 5). Esistono troppe interazioni farmacologiche per discuterne in dettaglio; pertanto, solo alcuni selezionati sono descritti di seguito.
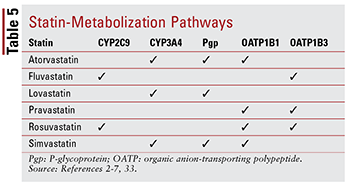
Fibrata: sebbene la combinazione di un fibrato e una statina non hanno dimostrato di alterare in modo significativo i risultati clinici, ai pazienti può ancora essere prescritto gemfibrozil, fenofibrato o acido fenofibrico insieme a una statina per combattere l’ipertrigliceridemia gravemente non controllata.14,20,26,33 Poiché entrambe queste classi sono associati a tossicità muscolare, la terapia di combinazione aumenta significativamente questo rischio rispetto alla sola terapia.33 Questa tossicità additiva è più frequente con gemfibrozil che con altri fibrati.33 Pertanto, l’uso di gemfibrozil è controindicato con la simvastatina e deve essere evitato con altri statine.7,20 Se si usano insieme una statina e un fibrato, è preferibile fenofibrato o acido fenofibrico.20,33 Tuttavia, se deve essere usato gemfibrozil, fluvastatina o, con attento monitoraggio, atorvastatina o rosuvastatina (massimo 10 mg al giorno ): È l’agente di scelta.33
Amiodarone: questo agente antiaritmico indicato per la fibrillazione ventricolare è un noto inibitore della glicoproteina P (Pgp) e del sistema enzimatico CYP450, in particolare CYP3A4 e, in misura minore, CYP2C9.33,34 Come un risultato, esistono dosaggi massimi raccomandati per lovastatina (massimo 40 mg al giorno) e simvastatina (massimo 20 mg al giorno) quando utilizzati con amiodarone.4,7,33 Sebbene l’atorvastatina sia metabolizzata attraverso il CYP3A4, non è necessario alcun aggiustamento del dosaggio (analogamente ad altre statine) perché i dati non suggeriscono eventi avversi gravi quando atorvastatina e amiodarone sono usati in concomitanza.2,33
CCB: sia i CCB diidropiridinici (amlodipina) che quelli non diidropiridinici (diltiazem, verapamil) hanno dimostrato di avere interazioni farmacologiche significative con le statine . Analogamente ad amiodarone, amlodipina, diltiazem e verapamil inibiscono il CYP3A4.33,35-37 L’amlodipina ha anche un effetto inibitorio su Pgp.33,35 Sulla base degli eventi avversi riportati in letteratura, si raccomanda una dose massima giornaliera di 20 mg per lovastatina utilizzato con amlodipina, diltiazem o verapamil.4,33 Si raccomanda inoltre di non superare i 20 mg di simvastatina se utilizzata con amlodipina, ma una dose inferiore di 10 mg deve essere somministrata se utilizzata con diltiazem e verapamil.7,33 Nessun dosaggio specifico esistono raccomandazioni con atorvastatina, sebbene si debba usare cautela quando viene somministrata con uno dei CCB non diidropiridinici.2,33
Reazioni avverse al farmaco
Le statine sono generalmente ben tollerate; tuttavia, i tassi di interruzione rimangono alti.38 L’interruzione della terapia con statine e la mancata ripresa della terapia con statine dopo il verificarsi di reazioni avverse al farmaco sono associate ad un aumento dei tassi di CVE.39 Le preoccupazioni dei pazienti sulla sicurezza delle statine alla luce di due principali eventi avversi correlati alle statine – miotossicità e diabete di nuova insorgenza: possono portare alla sospensione delle statine.
Miotossicità: le statine sono state a lungo associate a tossicità correlata ai muscoli, inclusa mialgia (dolore muscolare senza creatinchinasi elevata), miopatia (termine generale per muscolo malattia) e miosite (infiammazione muscolare), le ultime due delle quali comportano un aumento significativo della CK.40,41 Tutte le statine condividono un avvertimento per il raro ma grave effetto collaterale della rabdomiolisi.2-7 Spesso, tuttavia, la miotossicità attribuita alle statine è per effetto nocebo; vale a dire, una persona crede che un farmaco causerà danni e successivamente il farmaco causerà il danno previsto.42,43 Pertanto, per garantire il miglior risultato, i farmacisti devono essere esperti in questo effetto collaterale comunemente riportato e nella sua corretta gestione.
Non è corretto presumere che tutte le segnalazioni di sintomi muscolari siano dovute all’effetto nocebo; un controllo adeguato della storia medica passata del paziente (PMH), della descrizione del dolore e dell’associazione con la terapia con statine è imperativo.44 In primo luogo, un esame della PMH per gli aumenti della CK e altre potenziali cause di dolore o debolezza muscolare consente al medico di trattare un’alternativa fisiopatologia sottostante o fattori corretti che possono alterare il metabolismo delle statine. Le cause comuni includono vecchiaia, interazioni farmacologiche, funzionalità renale o epatica compromessa, aumento dell’attività fisica e carenza di vitamina D.20,41
Successivamente, il medico deve confrontare la presentazione del paziente con i sintomi comunemente osservati indotti dalle statine . La tossicità muscolare indotta dalle statine di solito si presenta come dolore, tenerezza, crampi e debolezza, di solito nei muscoli delle gambe.20,41 Questi sintomi sono tipicamente peggiori dopo l’esercizio e non si risolvono senza l’interruzione dell’agente incriminato.41
L’ultimo passaggio consiste nel determinare se esiste una relazione causale tra i sintomi e l’uso di statine. Quando si sospetta che una statina sia la causa di sintomi da lievi a moderati, si raccomanda la sospensione temporanea. Se i sintomi non si risolvono dopo circa 2 settimane, è probabile che la statina non sia la causa e deve essere ripresa alla dose originale. Tuttavia, se i sintomi si risolvono, deve essere eseguita una nuova analisi della stessa statina alla stessa dose o a una dose inferiore. Se si verificano sintomi simili, si deve presumere che la statina sia la causa e sospendere il trattamento. Dopo la risoluzione dei sintomi, deve essere iniziata una dose bassa di una statina alternativa e titolata alla dose massima tollerata.20,41 L’accettazione e la comprensione da parte del paziente di questo processo sono importanti perché l’effetto nocebo potrebbe altrimenti portare a ulteriori reazioni percepite.
Esistono molte altre strategie per gestire e prevenire questi sintomi. In primo luogo, a causa di una maggiore probabilità di sintomi, il medico può scegliere di evitare le statine più lipofile (lovastatina e simvastatina) a favore di statine più idrofile (fluvastatina, pravastatina e rosuvastatina) .44 La simvastatina 80 mg non deve mai essere iniziata come nuova terapia in qualsiasi paziente a causa di una frequenza insolitamente alta di sintomi muscolari associati alle statine.7,45 Terapie alternative, come il coenzima Q10, non hanno dimostrato un beneficio costante, ma possono essere prese in considerazione nei pazienti che manifestano sintomi psicologicamente indotti.41,44,46 Infine, può essere preso in considerazione il dosaggio a intervalli prolungati, che comporta il dosaggio di statine più volte alla settimana anziché una volta al giorno. Questo approccio migliora l’aderenza e il profilo lipidico nei pazienti con precedente intolleranza alle statine.47-49
Diabete di nuova insorgenza: un importante evento avverso associato all’uso di statine è il diabete di nuova insorgenza. È stato dimostrato che le statine aumentano il rischio di sviluppo del diabete, sebbene esistano diversi avvertimenti importanti.50 In primo luogo, sebbene questo possa essere considerato una sorta di effetto di classe, il vero rischio di ciascuna statina specifica è ancora sconosciuto.51,52 Nel più grande meta -analisi fino ad oggi, pravastatina aveva il rischio più basso, simvastatina e atorvastatina avevano un rischio moderato e rosuvastatina aveva il più alto rischio di causare diabete di nuova insorgenza.53 Nessuno di questi risultati era statisticamente significativo, tuttavia.53 Inoltre, la scoperta che il diabete il rischio aumenta quando la dose di statine aumenta è stata incoerente.54
Il diabete indotto da statine è più diffuso nelle persone già ad alto rischio di sviluppare il diabete.50,54 Ciò include i pazienti più anziani e quelli con prediabete o metabolismo 50,55 Un risultato consistente è stato che, per ogni nuovo caso di diabete incidente causato dalle statine, diversi CVE possono essere prevenuti nei pazienti ad alto rischio.50 Pertanto, i farmacisti dovrebbero consigliare un Chi fa uso di statine a rischio moderato o alto di complicanze CV che il rischio di sviluppare il diabete è più che compensato dai benefici di riduzione del rischio CV. Tuttavia, il rapporto rischio-beneficio non è chiaro nei pazienti con un rischio molto basso di CVE.50
CONCLUSIONE
Sebbene la terapia con statine non sia priva di rischi, i suoi benefici nel ridurre gli esiti CV ne ha fatto la pietra angolare della prevenzione delle CVE. Le linee guida disponibili differiscono ampiamente, ma l’unica costante è che le statine dovrebbero essere la terapia di prima linea per la prevenzione primaria e secondaria in quasi tutti i pazienti. La diffusa disponibilità generica di statine ha reso questi agenti sempre più accessibili. Comprendendo che non tutte le statine sono uguali, il farmacista può aiutare a garantire il miglior risultato possibile per ogni paziente.
1. IMS Institute for Healthcare Informatics. Uso e spesa di medicinali negli Stati Uniti: revisione del 2015 e prospettive per il 2020. https://morningconsult.com/wp-content/uploads/2016/04/IMS-Institute-US-Drug-Spending-2015.pdf. Accesso 18 marzo 2018.
2. Foglietto illustrativo di Lipitor (atorvastatina). New York, NY: Pfizer, Inc; Giugno 2017.
3. Foglietto illustrativo di Lescol / Lescol XL (fluvastatina). East Hanover, NJ: Novartis Pharmaceuticals Corp; Agosto 2017.
4. Foglietto illustrativo di Mevacor (lovastatina). Whitehouse Station, NJ: Merck & Co, Inc; Febbraio 2014.
5. Foglietto illustrativo di Pravachol (pravastatina). Princeton, NJ: Bristol-Myers Squibb Company; Luglio 2016.
6. Foglietto illustrativo di Crestor (rosuvastatina). Wilmington, DE: AstraZeneca Pharmaceuticals LP; Agosto 2017.
7. Foglietto illustrativo di Zocor (simvastatina). Whitehouse Station, NJ: Merck & Co, Inc; Febbraio 2015.
8. Foglietto illustrativo Altoprev (lovastatina). Zugo, Svizzera: Covis Pharma; Aprile 2017.
9. Foglietto illustrativo FloLipid (simvastatina). Brooksville, FL: Salerno Pharmaceuticals LP; Luglio 2017.
10. Foglietto illustrativo di Livalo (pitavastatina). Montgomery, AL: Kowa Pharmaceuticals America, Inc; Novembre 2016.
11. Foglietto illustrativo caduet (amlodipina / atorvastatina). New York, NY: Pfizer Inc; Ottobre 2017.
12. Foglietto illustrativo di Vytorin (ezetimibe / simvastatina). Whitehouse Station, NJ: Merck & Co, Inc; Febbraio 2018.
13. AbbVie Inc .; ritiro dell’approvazione di nuove domande di farmaci per Advicor e Simcor. www.federalregister.gov/documents/2016/04/18/2016-08894/abbvie-inc-withdrawal-of-approval-of-new-drug-applications-for-advicor-and-simcor. Accesso 18 marzo 2018.
14. Jellinger PS, Handelsman Y, Rosenblit PD, et al. Linee guida dell’American Association of Clinical Endocrinologists e dell’American College of Endocrinology per la gestione della dislipidemia e la prevenzione delle malattie cardiovascolari. Endocr Pract. 2017; 23 (suppl 2): 1-87.
15. LaRosa JC, Grundy SM, Waters DD, et al. Riduzione intensiva dei lipidi con atorvastatina in pazienti con malattia coronarica stabile. N Engl J Med. 2005; 352: 1425-1435.
16. Ridker PM, Danielson E, Fonseca FA, et al. Rosuvastatina per prevenire eventi vascolari in uomini e donne con elevata proteina C reattiva. N Engl J Med. 2008; 359: 2195-2207.
17. Mihaylova B, Emberson J, Blackwell L, et al. Gli effetti dell’abbassamento del colesterolo LDL con la terapia con statine nelle persone a basso rischio di malattie vascolari: meta-analisi dei dati individuali di 27 studi randomizzati. Lancetta. 2012; 380: 581-590.
18. Baigent C, Landray MJ, Reith C, et al. Gli effetti dell’abbassamento del colesterolo LDL con simvastatina più ezetimibe in pazienti con malattia renale cronica (Study of Heart and Renal Protection): uno studio randomizzato controllato con placebo. Lancetta. 2011; 377: 2181-2192.
19. Cannon CP, Braunwald E, McCabe CH, et al.Riduzione lipidica intensiva rispetto a moderata con statine dopo sindromi coronariche acute. N Engl J Med. 2004; 350: 1495-1504.
20. Stone NJ, Robinson JG, Lichtenstein AH, et al. 2013 Linee guida ACC / AHA sul trattamento del colesterolo nel sangue per ridurre il rischio cardiovascolare aterosclerotico negli adulti: un rapporto dell’American College of Cardiology / American Heart Association Task Force on Practice Guidelines. Circolazione. 2014; 129 (25 suppl 2): S1-S45.
21. American College of Cardiology. Stimatore del rischio ASCVD Plus. http://tools.acc.org/ASCVD-Risk-Estimator. Accesso 18 marzo 2018.
22. Wenger NK, Lewis SJ, Herrington DM, et al. Risultati dell’uso di atorvastatina ad alto o basso dosaggio in pazienti di età pari o superiore a 65 anni con malattia coronarica stabile. Ann Intern Med. 2007; 147: 1-9.
23. Shepherd J, Blauw GJ, Murphy MB, et al. Pravastatina in soggetti anziani a rischio di malattie vascolari (PROSPER): uno studio controllato randomizzato. Lancetta. 2002; 360: 1623-1630.
24. Teng M, Lin L, Zhao YJ, et al. Statine per la prevenzione primaria delle malattie cardiovascolari nei pazienti anziani: revisione sistematica e meta-analisi. Invecchiamento dei farmaci. 2015; 32: 649-661.
25. Kjekshus J, Apetrei E, Barrios V, et al. Rosuvastatina in pazienti anziani con insufficienza cardiaca sistolica. N Engl J Med. 2007; 357: 2248-2261.
26. Ginsberg HN, Elam MB, Lovato LC, et al. Effetti della terapia lipidica di combinazione nel diabete mellito di tipo 2. N Engl J Med. 2010; 362: 1563-1574.
27. Kastelein JJ, Akdim F, Stroes ES, et al. Simvastatina con o senza ezetimibe nell’ipercolesterolemia familiare. N Engl J Med. 2008; 358: 1431-1443.
28. Cannon CP, Blazing MA, Giugliano RP, et al. Ezetimibe aggiunto alla terapia con statine dopo sindromi coronariche acute. N Engl J Med. 2015; 372: 2387-2397.
29. Sabatine MS, Giugliano RP, Keech AC, et al. Evolocumab e risultati clinici in pazienti con malattie cardiovascolari. N Engl J Med. 2017; 376: 1713-1722.
30. Lloyd-Jones DM, Morris PB, Ballantyne CM, et al. 2017 aggiornamento focalizzato del 2016 ACC Expert Consensus Decision Pathway sul ruolo delle terapie senza statine per l’abbassamento del colesterolo LDL nella gestione del rischio di malattie cardiovascolari aterosclerotiche: un rapporto dell’American College of Cardiology Task Force on Expert Consensus Decision Pathways J Am Coll Cardiol. 2017; 70: 1785-1822.
31. Risultati ODYSSEY: i risultati suggeriscono che l’uso dell’inibitore PCSK9 riduce gli eventi CV, LDL-C nei pazienti con ACS. American College of Cardiology. www.acc.org/latest-in-cardiology/articles/2018/03/05/15/53/sat-9am-odyssey-outcomes-cv-outcomes-with-alirocumab-after-acs-acc-2018. Accesso 20 giugno 2018.
32. Wallace A, Chinn D, Rubin G. Assunzione di simvastatina al mattino rispetto alla sera: studio controllato randomizzato. BMJ. 2003; 327: 788.
33. Wiggins BS, Saseen JJ, Page RL, et al. Raccomandazioni per la gestione delle interazioni farmaco-farmaco clinicamente significative con statine e agenti selezionati utilizzati in pazienti con malattie cardiovascolari: una dichiarazione scientifica dell’American Heart Association. Circolazione. 2016; 134: e468-e495.
34. Foglietto illustrativo Pacerone (amiodarone). Maple Grove, MN: Upsher-Smith Laboratories LLC; Luglio 2017.
35. Foglietto illustrativo di Norvasc (amlodipina). New York, NY: Pfizer Inc; Ottobre 2017.
36. Foglietto illustrativo Cardizem (diltiazem). Bridgewater, NJ: Valeant Pharmaceuticals; Novembre 2016.
37. Foglietto illustrativo di Calan (verapamil). New York, NY: Pfizer Inc; Settembre 2017.
38. Riaz H, Khan AR, Khan MS, et al. Meta-analisi di studi clinici controllati randomizzati controllati con placebo sulla prevalenza dell’intolleranza alle statine. Sono J Cardiol. 2017; 120: 774-781.
39. Zhang H, Plutzky J, Shubina M, Turchin A. Prescrizioni continue di statine dopo reazioni avverse e risultati dei pazienti: uno studio di coorte. Ann Intern Med. 2017; 167: 221-227.
40. Tomaszewski M, Stepien KM, Tomaszewska J, Czuczwar SJ. Miopatie indotte da statine. Pharmacol Rep. 2011; 63: 859-866.
41. Stroes ES, Thompson PD, Corsini A, et al. Sintomi muscolari associati alle statine: impatto sulla terapia con statine – Dichiarazione del Consensus Panel della European Atherosclerosis Society sulla valutazione, eziologia e gestione. Eur Heart J. 2015; 36: 1012-1022.
42. Gupta A, Thompson D, Whitehouse A, et al. Eventi avversi associati alla terapia con statine in cieco, ma non in cieco, nell’Anglo-Scandinavian Cardiac Outcomes Trial – Lipid-Lowering Arm (ASCOT-LLA): uno studio randomizzato in doppio cieco controllato con placebo e la sua estensione non randomizzata non in cieco fase. Lancetta. 2017; 389: 2473-2481.
43. Pedro-Botet J, Rubiés-Prat J. Sintomi muscolari associati alle statine: attenzione all’effetto nocebo. Lancetta. 2017; 389: 2445-2446.
44. Laufs U, Filipiak KJ, Gouni-Berthold I, et al. Aspetti pratici nella gestione dei sintomi muscolari associati alle statine (SAMS). Ateroscler Suppl. 2017; 26: 45-55.
45. Comunicazione della FDA sulla sicurezza dei farmaci: nuove restrizioni, controindicazioni e limitazioni di dose per Zocor (simvastatina) per ridurre il rischio di lesioni muscolari www.fda.gov/Drugs/DrugSafety/ucm256581.htm. Accesso 18 marzo 2018.
46.Banach M, Serban C, Sahebkar A, et al. Effetti del coenzima Q10 sulla miopatia indotta da statine: una meta-analisi di studi randomizzati controllati. Mayo Clin Proc. 2015; 90: 24-34.
47. Goldberg AS, DeGorter MK, Ban MR, et al. Efficacia e concentrazioni plasmatiche del farmaco con dosaggio non giornaliero di rosuvastatina. Può J Cardiol. 2013; 29: 915-919.
48. Matalka MS, Ravnan MC, Deedwania PC. La dose giornaliera alternativa di atorvastatina è efficace nel trattamento di pazienti con iperlipidemia? Studio di atorvastatina (ADDAS) a confronto con il dosaggio giornaliero alternativo. Am Heart J. 2002; 144: 674-677.
49. Copher HR, Stewart RD. Dosaggio giornaliero rispetto alla somministrazione a giorni alterni di simvastatina in pazienti con ipercolesterolemia. Farmacoterapia. 2002; 22: 1110-1116.
50. Rochlani Y, Kattoor AJ, Pothineni NV, et al. Bilanciamento della prevenzione primaria e della prevenzione del diabete mellito indotto dalle statine. Sono J Cardiol. 2017; 120: 1122-1128.
51. Corrao G, Ibrahim B, Nicotra F, et al. Statine e rischio di diabete: evidenze da un ampio studio di coorte basato sulla popolazione. Cura del diabete. 2014; 37: 2225-2232.
52. Lim S, Oh PC, Sakuma I, Koh KK. Come bilanciare benefici cardiorenometabolici e rischi delle statine. Aterosclerosi. 2014; 235: 644-648.
53. Navarese EP, Buffon A, Andreotti F, et al. Meta-analisi dell’impatto di diversi tipi e dosi di statine sul diabete mellito di nuova insorgenza. Sono J Cardiol. 2013; 111: 1123-1130.
54. Crandall JP, Mather K, Rajpathak SN, et al. Uso di statine e rischio di sviluppare il diabete: risultati del Programma di prevenzione del diabete. BMJ Open Diabetes Res Care. 2017; 5: e000438.
55. Ganda OP. Diabete indotto da statine: incidenza, meccanismi e implicazioni. F1000Res. 2016; 5.