US Pharm. 2018; 43 (7): 22-26.
REZUMAT: Statinele sunt o clasă de medicamente utilizate pe scară largă pentru prevenirea primară și secundară a evenimentelor cardiovasculare. Cu șase statine disponibile generic, selecția unui agent adecvat poate fi determinată pe baza factorilor specifici medicamentului, inclusiv considerații de dozare, interacțiuni medicamentoase și evenimente adverse. Planurile individualizate de îngrijire a pacienților pot fi dezvoltate pe baza datelor din studii clinice importante, a diferențelor de orientări și a recomandărilor actuale de management pentru două evenimente adverse majore asociate cu utilizarea statinelor.
Piatra de temelie a tratamentului cu dislipidemie implică utilizarea 3-hidroxi-3-metilglutaril-coenzima A Inhibitori ai reductazei, mai frecvent cunoscuți ca statine. Cu o varietate de opțiuni generice de pe piață și dovezi puternice care susțin utilizarea lor, statinele sunt unele dintre cele mai prescrise medicamente din lume.1 Cu toate acestea, utilizarea frecventă a acestor agenți a condus la o examinare continuă a siguranței lor și la dezbateri continue despre rol în terapie. Acest articol, care se concentrează pe statinele generice, va evidenția dezbaterea despre rolul statinelor în terapie, va discuta despre utilizarea corectă și va explora dovezile care înconjoară două evenimente adverse majore.
Dintre cele șapte statine diferite de pe piață, șase sunt disponibile generic (TABELUL 1) .2-7 Trei formulări disponibile de marcă sunt pitavastatina (Livalo), suspensia orală de simvastatină (FloLipid) și lovastatina cu eliberare prelungită (Altoprev). 8-10 Rolul agenților de marcă în terapie este limitat, dat fiind disponibilitatea pe scară largă a opțiunilor generice.
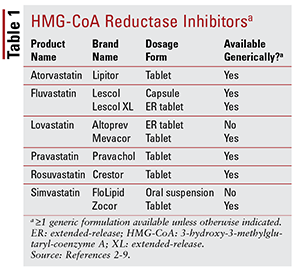
Atorvastatina și simvastatina sunt de asemenea disponibile generic în mai multe produse combinate. Acestea includ combinația de atorvastatină și amlodipină, un blocant al canalelor de calciu (CCB) indicat pentru hipertensiune arterială, și combinația de simvastatină și ezetimib, un inhibitor de absorbție a colesterolului intestinal indicat și pentru hipercolesterolemie.11,12 Statine coformulate și produse niacinice (niacină / lovastatină și niacină / simvastatină) au fost eliminate de pe piață în 2016 pe baza lipsei de dovezi că adăugarea niacinei la pacienții tratați cu statină reduce și mai mult rezultatele cardiovasculare (CV) dincolo de ceea ce se observă numai cu statine.13
RECOMANDĂRI DE TRATAMENT
Statinele s-au dovedit în mod repetat eficiente pentru reducerea nivelului de LDL-colesterol (LDL-C) și trigliceride, crescând în același timp nivelul HDL-colesterolului (HDL-C). rezultate orientate spre pacient, cum ar fi evenimente CV majore (CVE), atât în prevenirea primară, cât și în cea secundară.15-19
Mai multe orientări de tratament puternic dezbătute discută rolul statinelor în tratamentul h perlipidemie. Acestea includ ghidul Colegiului American de Cardiologie din 2013 / Asociația Americană a Inimii (ACC / AHA) și ghidul Academiei Americane de Endocrinologie Clinică (AACE) din 2017.14,20 Ambele ghiduri sugerează că, după implementarea modificărilor stilului de viață, inclusiv renunțarea la fumat, un regim de exerciții și, în urma unei diete sănătoase pentru inimă, statinele sunt terapie de primă linie atât pentru prevenirea primară cât și pentru prevenirea secundară a bolii CV (BCV) .14,20 Orientările diferă, totuși, în modul de determinare a statinelor care sunt potrivite pentru care pacienți.
Ghidul ACC / AHA 2013 a introdus patru grupuri de tratament care urmează să fie vizate pentru terapia cu statine:
1. Pacienții cu BCV aterosclerotică anterioară (ASCVD), inclusiv cei cu un eveniment anterior (de exemplu, sindroame coronariene acute, antecedente de infarct miocardic, angină stabilă sau instabilă, revascularizare coronariană sau de altă natură arterială, accident vascular cerebral, atac ischemic tranzitor sau boală arterială periferică a prezumției origine aterosclerotică).
2. Pacienți fără antecedente de eveniment ASCVD care au un nivel LDL-C de 190 mg / dL sau mai mare. Vârsta nu este o bază pentru excluderea de la acest criteriu.
3. Pacienți cu vârsta cuprinsă între 40 și 75 de ani cu diabet zaharat, dar fără antecedente de eveniment ASCVD și cu un nivel LDL-C între 70 și 189 mg / dL.
4. Pacienții cu vârsta cuprinsă între 40 și 75 de ani fără diabet, care nu au antecedente de eveniment ASCVD și un nivel LDL-C între 70 și 189 mg / dL.20
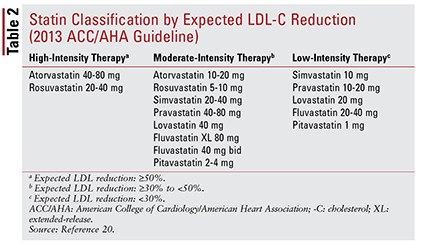
Ghidul ACC / AHA a introdus, de asemenea, ideea grupării statinelor după intensitate (adică, capacitatea lor scăzută de scădere a LDL-C) (TABELUL 2) .20 Pe baza grupului de tratament (așa cum este definit mai sus), ghidul recomandă intensități specifice ale statinelor pentru situații clinice particulare (TABELUL 3) .20 Mai multe grupuri de tratament necesită calcularea unui scor de risc ASCVD folosind un estimator de risc ASCVD. Acest instrument online ia în considerare vârsta, sexul, rasa, tensiunea arterială sistolică, colesterolul total, HDL-C și antecedentele medicale ale pacientului semnificative pentru tratamentul hipertensiunii arteriale, diabetul sau fumatul.21 Odată ce toate intrările au fost introduse, pacientul 10 -se calculează riscul de a experimenta un eveniment ASCVD.
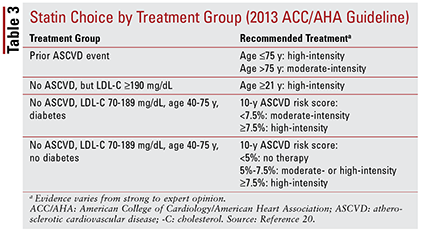
Aceste recomandări nu se aplică automat anumitor subgrupuri de pacienți. De exemplu, utilizarea statinelor la adulții în vârstă trebuie abordată cu prudență. Deși utilizarea statinelor pentru prevenirea secundară la pacienții vârstnici conferă un beneficiu semnificativ, utilizarea sa pentru prevenirea primară este neclară.22-24 În plus, pacienții cu insuficiență cardiacă nu s-au dovedit a avea aceleași beneficii din terapia cu statine ca și cei fără insuficiență cardiacă. pe baza acestor constatări, recomandările de tratament includ limitarea inițierii statinelor de intensitate ridicată la pacienții cu vârsta sub 75 de ani și, eventual, evitarea statinelor la pacienții cu insuficiență cardiacă.20 În general, decizia de utilizare a statinelor în aceste grupuri nu este clară și ar trebui să implice o conversație continuă între furnizor și pacient despre riscurile și beneficiile potențiale ale terapiei.20
Contrar recomandării ACC / AHA din 2013 de a iniția terapia în conformitate cu clasificarea grupului de tratament, ghidul AACE din 2017 recomandă ca pacienții individuali să fie tratat pe baza descoperirilor de laborator.14 Conform acestui ghid, riscul pacientului este determinat de o varietate de mari, suplimentare, a și factori de risc netradiționali. Persoanele sunt apoi clasificate în unul din cele cinci grupuri de risc, fiecare având un obiectiv LDL-C corespunzător și non-HDL-C (TABELUL 4). Pe baza nivelurilor actuale și a obiectivelor individualizate, statinele singure sau în combinație cu alți agenți ar trebui inițiate pe baza abilității scăzute de scădere a LDL-C– sau non-HDL-C.14

Tratamentul combinat care implică adăugarea unui al doilea agent la terapia cu statine în curs rămâne un subiect oarecum controversat. În timp ce studiile și ghidurile anterioare au minimizat adăugarea altor agenți la terapia cu statine de fond, studii recente și declarații de consens – inclusiv unul din ACC / AHA – susțin utilizarea ezetimibului, evolocumabului sau alirocumabului, ultimele două fiind proprotein convertaza subtilizină / inhibitori de tip kexin 9, ca terapie suplimentară pentru prevenirea secundară.20,26-31 Acestea fiind spuse, statinele rămân terapie universală de primă linie atât în prevenirea primară, cât și în cea secundară; rolul definitiv al altor agenți specifici rămâne neclar.
SELECȚIA STATINELOR
Alegerea terapiei cu statine începe cu abordarea de tratament preferată a clinicianului, indiferent dacă aceasta este metoda ACC / AHA de tratament cu statine grupuri sau metoda AACE a obiectivelor LDL-C sau non-HDL-C. De acolo, trebuie luate în considerare proprietățile fiecărei statine pentru a determina cea mai bună opțiune pentru fiecare pacient. Nu toate statinele sunt egale și există mai multe diferențe cheie care pot influența selecția pacientului, inclusiv considerații de dozare, interacțiuni medicamentoase și evenimente adverse (AE).
Dozare
Deși majoritatea statinelor pot trebuie luată fără a lua în considerare mesele, lovastatina cu eliberare imediată (IR) trebuie luată împreună cu masa de seară din cauza biodisponibilității crescute.4 Cu toate acestea, opusul este adevărat pentru lovastatina cu eliberare prelungită, care nu trebuie luată cu alimente din cauza biodisponibilității scăzute .8 În plus, deși toate statinele pot fi administrate o dată pe zi, fluvastatina IR și lovastatina pot necesita doze de două ori pe zi.3,4 În cele din urmă, în timp ce atorvastatina, pravastatina și rosuvastatina pot fi administrate în orice moment al zilei, fluvastatina, lovastatina și simvastatina trebuie administrată seara.3,4,7 Simvastatina, în special, sa dovedit a avea o eficacitate semnificativ diferită atunci când este luată seara, spre deosebire de dimineață.32
Interacțiuni medicamentoase
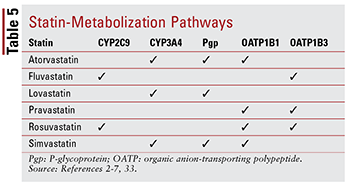
Fiecare statină are diferite îngrijorări cu privire la interacțiunile medicament-medicament și medicamente-alimente din cauza căilor specifice prin care fiecare este metabolizat (TABELUL 5). Există prea multe interacțiuni medicamentoase pentru a discuta fiecare în detaliu; prin urmare, doar câteva selectate sunt descrise mai jos.
Fibrează: Deși combinația nu s-a demonstrat că un fibrat și o statină modifică semnificativ rezultatele clinice, pacienților li se poate prescrie gemfibrozil, fenofibrat sau acid fenofibric împreună cu o statină pentru a viza hipertrigliceridemia sever necontrolată.14,20,26,33 Deoarece ambele clase sunt asociate cu toxicitate musculară, terapia combinată crește semnificativ acest risc în comparație cu terapia singură.33 Această toxicitate aditivă este mai frecvent observată la gemfibrozil decât la alți fibrați.33 Prin urmare, utilizarea gemfibrozilului este contraindicată cu simvastatină și trebuie evitată cu alte statine.7,20 Dacă se utilizează împreună o statină și un fibrat, se preferă fenofibratul sau acidul fenofibric.20,33 Totuși, dacă trebuie utilizat gemfibrozil, fluvastatina – sau, cu o monitorizare atentă, atorvastatina sau rosuvastatina (maxim 10 mg pe zi) ) – este agentul ales.33
Amiodaronă: acest agent antiaritmic indicat pentru fibrilația ventriculară este un inhibitor cunoscut al glicoproteinei P (Pgp) și al sistemului enzimatic CYP450, în special CYP3A4 și, într-o măsură mai mică, CYP2C9.33,34 Ca rezultat, există doze maxime recomandate pentru lovastatină (maximum 40 mg pe zi) și simvastatină (maximum 20 mg pe zi) când se utilizează cu amiodaronă. 4,7,33 Deși atorvastatina este metabolizată prin CYP3A4, nu este necesară ajustarea dozelor (similar cu alte statine) deoarece datele nu sugerează AE serioase atunci când atorvastatina și amiodarona sunt utilizate concomitent.2,33
CCB: Atât dihidropiridina (amlodipină), cât și nondihidropiridina CCB (diltiazem, verapamil) s-au dovedit a avea interacțiuni medicamentoase semnificative cu statinele . Similar cu amiodarona, amlodipina, diltiazemul și verapamilul inhibă CYP3A4.33,35-37 Amlodipina are, de asemenea, un efect inhibitor asupra Pgp.33,35. Pe baza AE raportate în literatură, se recomandă o doză zilnică maximă de 20 mg pentru lovastatină atunci când utilizat cu amlodipină, diltiazem sau verapamil.4,33 De asemenea, se recomandă ca simvastatina să nu depășească 20 mg atunci când este utilizată cu amlodipină, dar trebuie administrată o doză mai mică de 10 mg atunci când este utilizată cu diltiazem și verapamil.7,33 Fără dozare specifică recomandări există cu atorvastatină, deși trebuie administrată precauție atunci când este administrată cu oricare dintre CCB nondihidropiridinice.2,33
Reacții adverse la medicamente
Statinele sunt în general bine tolerate; cu toate acestea, ratele de întrerupere rămân ridicate.38 Întreruperea tratamentului cu statine și eșecul reluării terapiei cu statine după apariția reacțiilor adverse la medicamente sunt asociate cu rate crescute de CVEs.39 Preocupările pacienților cu privire la siguranța statinelor în lumina a două AE majore legate de statină – miotoxicitate și diabet cu debut nou – pot duce la întreruperea statinelor.
Miotoxicitate: statinele au fost asociate de mult timp cu toxicitate musculară, inclusiv mialgie (durere musculară fără creatin kinază crescută), miopatie (termen general pentru mușchi) boală) și miozita (inflamația musculară), dintre care ultimele două implică creșteri semnificative ale CK. 40,41 Toate statinele au un avertisment cu privire la efectul secundar rar, dar grav al rabdomiolizei.2-7 Adesea, totuși, miotoxicitatea atribuită statinelor este datorită efectului nocebo; adică, o persoană consideră că un medicament va provoca daune și ulterior medicamentul va provoca daunele anticipate.42,43 Prin urmare, pentru a asigura cel mai bun rezultat, farmaciștii trebuie să fie bine versați în legătură cu acest efect secundar raportat în mod obișnuit și în gestionarea corectă a acestuia.
Este incorect să presupunem că toate raportările de simptome musculare se datorează efectului nocebo; verificarea adecvată a istoricului medical trecut al pacientului (PMH), descrierea durerii și asocierea cu terapia cu statine este imperativă.44 În primul rând, o examinare a PMH pentru creșteri ale CK și alte cauze potențiale ale durerii sau slăbiciunii musculare permite clinicianului să trateze alternative fiziopatologia de bază sau factorii corecți care pot modifica metabolismul statinelor. Cauzele frecvente includ bătrânețea, interacțiunile medicamentoase, funcția renală sau hepatică afectată, activitatea fizică crescută și deficiența de vitamina D.20,41
Apoi, clinicianul ar trebui să compare prezentarea pacientului cu simptomele frecvent observate induse de statină. . Toxicitatea musculară indusă de statină se prezintă de obicei ca durere, sensibilitate, crampe și slăbiciune, de obicei la nivelul mușchilor picioarelor.20,41 Aceste simptome sunt de obicei mai grave după exerciții și nu se rezolvă fără întreruperea agentului ofensator.41
Ultimul pas este de a determina dacă există o relație de cauzalitate între simptome și utilizarea statinelor. Când se suspectează o statină ca fiind cauza simptomelor ușoare până la moderate, se recomandă întreruperea temporară. Dacă simptomele nu se rezolvă după aproximativ 2 săptămâni, probabil că statina nu este cauza și ar trebui reinitiată la doza inițială. Cu toate acestea, dacă simptomele se rezolvă, trebuie efectuat un proces din nou cu aceeași statină la aceeași doză sau cu o doză mai mică. Dacă sunt prezentate simptome similare, se presupune că statina este cauza și trebuie întreruptă. După rezolvarea simptomelor, trebuie inițiată o doză mică de statină alternativă și titrată la doza maximă tolerată.20,41. Acceptarea și înțelegerea de către pacient a acestui proces sunt importante, deoarece efectul nocebo poate duce la reacții percepute în continuare.
Există câteva alte strategii pentru gestionarea și prevenirea acestor simptome. În primul rând, datorită unei probabilități mai mari de simptome, medicul poate alege să evite cele mai lipofile statine (lovastatină și simvastatină) în favoarea statinelor mai hidrofile (fluvastatină, pravastatină și rosuvastatină) .44 Simvastatina 80 mg nu trebuie inițiată niciodată ca nouă terapie la orice pacient din cauza unei frecvențe neobișnuit de ridicate a simptomelor musculare asociate cu statine.7,45 Terapiile alternative, cum ar fi coenzima Q10, nu au demonstrat beneficii consistente, dar pot fi luate în considerare la pacienții care prezintă simptome induse psihologic.41,44,46 În cele din urmă, poate fi luată în considerare dozarea cu interval prelungit, care implică dozarea medicamentelor cu statine de mai multe ori pe săptămână decât o dată pe zi. Această abordare îmbunătățește aderența și profilurile lipidice la pacienții cu intoleranță anterioară la statine.47-49
Diabet cu debut nou: un AE important asociat cu utilizarea statinelor este diabetul cu debut nou. S-a demonstrat că statinele cresc riscul de dezvoltare a diabetului, deși există mai multe avertismente importante.50 În primul rând, deși acest lucru poate fi considerat un efect de clasă, riscul real al fiecărei statine specifice este încă necunoscut.51,52 În cea mai mare meta -analiza până în prezent, pravastatina a avut cel mai mic risc, simvastatina și atorvastatina au avut un risc moderat, iar rosuvastatina a avut cel mai mare risc de a provoca diabet nou debut.53 Niciuna dintre aceste constatări nu a fost semnificativă statistic, totuși.53 În plus, constatarea că riscul crește pe măsură ce doza de statine crește a fost inconsistentă.54
Diabetul indus de statină este cel mai răspândit la persoanele cu risc crescut de a dezvolta diabet.50,54 Aceasta include pacienții mai în vârstă și cei cu prediabet sau metabolici sindrom.50,55 O constatare consecventă a fost că, pentru fiecare caz nou de diabet incident cauzat de statine, mai multe CVE pot fi prevenite la pacienții cu risc mai mare50. Prin urmare, farmaciștii ar trebui să consulte un consumatori de statine serioase cu risc moderat sau ridicat de complicații ale CV, riscul de a dezvolta diabet este mai mult decât compensat de beneficiile de reducere a riscului CV. Cu toate acestea, raportul risc-beneficiu este neclar la pacienții cu un risc foarte scăzut de CVEs.50
CONCLUZIE
Deși terapia cu statine nu este lipsită de riscuri, beneficiile sale în reducerea rezultatelor CV au avut a făcut-o piatra de temelie a prevenirii CVE. Liniile directoare disponibile diferă mult, dar singura constantă este că statinele ar trebui să fie terapie de primă linie pentru prevenirea primară și secundară la aproape fiecare pacient. Disponibilitatea generică pe scară largă a statinelor a făcut ca acești agenți să fie din ce în ce mai accesibili. Înțelegând că nu toate statinele sunt la fel, farmacistul poate contribui la asigurarea celui mai bun rezultat posibil pentru fiecare pacient.
1. IMS Institute for Healthcare Informatics. Utilizarea și cheltuielile medicamentelor în SUA: o revizuire a anului 2015 și perspectivele pentru 2020. https://morningconsult.com/wp-content/uploads/2016/04/IMS-Institute-US-Drug-Spending-2015.pdf. Accesat la 18 martie 2018.
2. Lipitor (atorvastatină) prospect. New York, NY: Pfizer, Inc; Iunie 2017.
3. Prospect Lescol / Lescol XL (fluvastatină). East Hanover, NJ: Novartis Pharmaceuticals Corp; August 2017.
4. Prospect Mevacor (lovastatină). Stația Whitehouse, NJ: Merck & Co, Inc; Februarie 2014.
5. Prospect Pravachol (pravastatin). Princeton, NJ: Compania Bristol-Myers Squibb; Iulie 2016.
6. Prospect Crestor (rosuvastatin). Wilmington, DE: AstraZeneca Pharmaceuticals LP; August 2017.
7. Prospect Zocor (simvastatin). Stația Whitehouse, NJ: Merck & Co, Inc; Februarie 2015.
8. Prospect Altoprev (lovastatină). Zug, Elveția: Covis Pharma; Aprilie 2017.
9. Prospect FloLipid (simvastatină). Brooksville, FL: Salerno Pharmaceuticals LP; Iulie 2017.
10. Prospect Livalo (pitavastatin). Montgomery, AL: Kowa Pharmaceuticals America, Inc; Noiembrie 2016.
11. Prospect Caduet (amlodipină / atorvastatină). New York, NY: Pfizer Inc; Octombrie 2017.
12. Prospect Vytorin (ezetimibe / simvastatin). Stația Whitehouse, NJ: Merck & Co, Inc; Februarie 2018.
13. AbbVie Inc .; retragerea aprobării noilor cereri de medicamente pentru Advicor și Simcor. www.federalregister.gov/documents/2016/04/18/2016-08894/abbvie-inc-withdrawal-of-approval-of-new-drug-applications-for-advicor-and-simcor. Accesat la 18 martie 2018.
14. Jellinger PS, Handelsman Y, Rosenblit PD și colab. Asociația Americană a Endocrinologilor Clinici și liniile directoare ale Colegiului American de Endocrinologie pentru gestionarea dislipidemiei și prevenirea bolilor cardiovasculare. Practica endocrină. 2017; 23 (supl. 2): 1-87.
15. LaRosa JC, Grundy SM, Waters DD și colab. Scăderea intensivă a lipidelor cu atorvastatină la pacienții cu boală coronariană stabilă. N Engl J Med. 2005; 352: 1425-1435.
16. Ridker PM, Danielson E, Fonseca FA și colab. Rosuvastatina pentru prevenirea evenimentelor vasculare la bărbați și femei cu proteine C reactive crescute. N Engl J Med. 2008; 359: 2195-2207.
17. Mihaylova B, Emberson J, Blackwell L și colab. Efectele scăderii colesterolului LDL cu terapia cu statine la persoanele cu risc scăzut de boală vasculară: meta-analiză a datelor individuale din 27 de studii randomizate. Lancet. 2012; 380: 581-590.
18. Baigent C, Landray MJ, Reith C și colab. Efectele scăderii colesterolului LDL cu simvastatină plus ezetimib la pacienții cu afecțiuni renale cronice (Studiul protecției cardiace și renale): un studiu randomizat controlat cu placebo. Lancet. 2011; 377: 2181-2192.
19. Cannon CP, Braunwald E, McCabe CH și colab.Scăderea intensivă a lipidelor moderată cu statine după sindroame coronariene acute. N Engl J Med. 2004; 350: 1495-1504.
20. Stone NJ, Robinson JG, Lichtenstein AH și colab. 2013 Ghidul ACC / AHA privind tratamentul colesterolului din sânge pentru a reduce riscul cardiovascular aterosclerotic la adulți: un raport al Colegiului American de Cardiologie / American Heart Association Task Force on Practice Guidelines. Circulaţie. 2014; 129 (25 supl. 2): S1-S45.
21. Colegiul American de Cardiologie. ASCVD Risk Estimator Plus. http://tools.acc.org/ASCVD-Risk-Estimator. Accesat la 18 martie 2018.
22. Wenger NK, Lewis SJ, Herrington DM și colab. Rezultatele utilizării dozei mari sau mici de atorvastatină la pacienții cu vârsta de 65 de ani sau peste cu boală coronariană stabilă. Ann Intern Med. 2007; 147: 1-9.
23. Shepherd J, Blauw GJ, Murphy MB și colab. Pravastatină la persoanele în vârstă cu risc de boală vasculară (PROSPER): un studiu controlat randomizat. Lancet. 2002; 360: 1623-1630.
24. Teng M, Lin L, Zhao YJ și colab. Statine pentru prevenirea primară a bolilor cardiovasculare la pacienții vârstnici: revizuire sistematică și meta-analiză. Îmbătrânirea drogurilor. 2015; 32: 649-661.
25. Kjekshus J, Apetrei E, Barrios V, și colab. Rosuvastatină la pacienții vârstnici cu insuficiență cardiacă sistolică. N Engl J Med. 2007; 357: 2248-2261.
26. Ginsberg HN, Elam MB, Lovato LC și colab. Efectele terapiei combinate lipidice în diabetul zaharat de tip 2. N Engl J Med. 2010; 362: 1563-1574.
27. Kastelein JJ, Akdim F, Stroes ES și colab. Simvastatină cu sau fără ezetimib în hipercolesterolemie familială. N Engl J Med. 2008; 358: 1431-1443.
28. Cannon CP, Blazing MA, Giugliano RP și colab. Ezetimibul a fost adăugat la terapia cu statine după sindroame coronariene acute. N Engl J Med. 2015; 372: 2387-2397.
29. Sabatine MS, Giugliano RP, Keech AC, și colab. Evolocumab și rezultatele clinice la pacienții cu boli cardiovasculare. N Engl J Med. 2017; 376: 1713-1722.
30. Lloyd-Jones DM, Morris PB, Ballantyne CM și colab. Actualizarea axată pe 2017 a căii de decizie a consensului expertului 2016 ACC privind rolul terapiilor non-statinice pentru scăderea colesterolului LDL în gestionarea riscului de boli cardiovasculare aterosclerotice: un raport al Colegiului American de Cardiologie Task Force on Expert Consensus Decision Pathways. J Am Coll Cardiol. 2017; 70: 1785-1822.
31. ODYSSEY Rezultate: rezultatele sugerează utilizarea inhibitorului PCSK9 reduce evenimentele CV, LDL-C la pacienții cu SCA. Colegiul American de Cardiologie. www.acc.org/latest-in-cardiology/articles/2018/03/05/15/53/sat-9am-odyssey-outcomes-cv-outcomes-with-alirocumab-after-acs-acc-2018. Accesat la 20 iunie 2018.
32. Wallace A, Chinn D, Rubin G. Luând simvastatină dimineața în comparație cu seara: studiu controlat randomizat. BMJ. 2003; 327: 788.
33. Wiggins BS, Saseen JJ, Page RL și colab. Recomandări pentru gestionarea interacțiunilor medicamentoase semnificative clinic cu statinele și agenții selectați utilizați la pacienții cu boli cardiovasculare: o declarație științifică a American Heart Association. Circulaţie. 2016; 134: e468-e495.
34. Prospect paceronă (amiodaronă). Maple Grove, MN: Upsher-Smith Laboratories LLC; Iulie 2017.
35. Prospect Norvasc (amlodipină). New York, NY: Pfizer Inc; Octombrie 2017.
36. Prospect Cardizem (diltiazem). Bridgewater, NJ: Valeant Pharmaceuticals; Noiembrie 2016.
37. Prospect Calan (verapamil). New York, NY: Pfizer Inc; Septembrie 2017.
38. Riaz H, Khan AR, Khan MS și colab. Metaanaliza studiilor randomizate controlate placebo controlate cu privire la prevalența intoleranței la statine. Sunt J Cardiol. 2017; 120: 774-781.
39. Zhang H, Plutzky J, Shubina M, Turchin A. Continuarea prescripțiilor de statine după reacțiile adverse și rezultatele pacienților: un studiu de cohortă. Ann Intern Med. 2017; 167: 221-227.
40. Tomaszewski M, Stepien KM, Tomaszewska J, Czuczwar SJ. Miopatii induse de statină. Pharmacol Rep. 2011; 63: 859-866.
41. Stroes ES, Thompson PD, Corsini A și colab. Simptome musculare asociate cu statine: impact asupra terapiei cu statine – Declarația grupului de consens al societății europene de ateroscleroză privind evaluarea, etiologia și managementul. Eur Heart J. 2015; 36: 1012-1022.
42. Gupta A, Thompson D, Whitehouse A și colab. Evenimente adverse asociate cu terapia cu statine neorbită, dar nu cu terapia orbită cu statine, în testul Anglo-Scandinavian Cardiac Outcomes Trial — Lipid-Downing Arm (ASCOT-LLA): un studiu randomizat dublu-orb controlat cu placebo și extensia sa ne-orbială non-randomizată fază. Lancet. 2017; 389: 2473-2481.
43. Pedro-Botet J, Rubiés-Prat J. Simptome musculare asociate statinei: feriți-vă de efectul nocebo. Lancet. 2017; 389: 2445-2446.
44. Laufs U, Filipiak KJ, Gouni-Berthold I și colab. Aspecte practice în gestionarea simptomelor musculare asociate cu statine (SAMS). Ateroscler Supliment. 2017; 26: 45-55.
45. Comunicarea FDA privind siguranța medicamentelor: noi restricții, contraindicații și limitări ale dozelor pentru Zocor (simvastatină) pentru a reduce riscul de vătămare musculară. www.fda.gov/Drugs/DrugSafety/ucm256581.htm. Accesat la 18 martie 2018.
46.Banach M, Serban C, Sahebkar A și colab. Efectele coenzimei Q10 asupra miopatiei induse de statine: o meta-analiză a studiilor controlate randomizate. Mayo Clin Proc. 2015; 90: 24-34.
47. Goldberg AS, DeGorter MK, Ban MR, și colab. Eficacitatea și concentrațiile plasmatice ale medicamentelor cu dozarea nediligenă a rosuvastatinei. Poate J Cardiol. 2013; 29: 915-919.
48. Matalka MS, Ravnan MC, Deedwania PC. Este eficientă doza zilnică alternativă de atorvastatină în tratarea pacienților cu hiperlipidemie? Ziua alternativă versus dozarea zilnică a studiului de atorvastatină (ADDAS). Am Heart J. 2002; 144: 674-677.
49. Copher HR, Stewart RD. Dozarea zilnică versus administrarea alternativă a zilei de simvastatină la pacienții cu hipercolesterolemie. Farmacoterapie. 2002; 22: 1110-1116.
50. Rochlani Y, Kattoor AJ, Pothineni NV, și colab. Echilibrarea prevenirii primare și prevenirea diabetului zaharat indusă de statine. Sunt J Cardiol. 2017; 120: 1122-1128.
51. Corrao G, Ibrahim B, Nicotra F și colab. Statinele și riscul de diabet: dovezi dintr-un studiu de cohortă amplu bazat pe populație. Îngrijirea diabetului. 2014; 37: 2225-2232.
52. Lim S, Oh PC, Sakuma I, Koh KK. Cum se echilibrează beneficiile cardiorenometabolice și riscurile statinelor. Ateroscleroza. 2014; 235: 644-648.
53. Navarese EP, Buffon A, Andreotti F și colab. Metaanaliza impactului diferitelor tipuri și doze de statine asupra diabetului zaharat cu debut nou. Sunt J Cardiol. 2013; 111: 1123-1130.
54. Crandall JP, Mather K, Rajpathak SN și colab. Utilizarea statinelor și riscul de a dezvolta diabet: rezultate din Programul de prevenire a diabetului. BMJ Open Diabetes Res Care. 2017; 5: e000438.
55. Ganda OP. Diabetul indus de statină: incidență, mecanisme și implicații. F1000Res. 2016; 5.