Acest curs a fost publicat în numărul din martie 2016 și expiră la 31.03.19. Autorii nu au conflicte comerciale de interese de dezvăluit. Această activitate de auto-studiu de 2 ore de credit este mediată electronic.
OBIECTIVE
După ce a citit acest curs, participantul ar trebui să poată:
- Discuta despre diferitele tipuri de medicamente care pot provoca mărirea gingivală.
- Identificați caracteristicile clinice ale măririi gingivale.
- Explicați etiologia și factorii de risc ai măririi gingivale induse de medicament.
- Enumerați opțiunile disponibile pentru tratarea acestei afecțiuni.
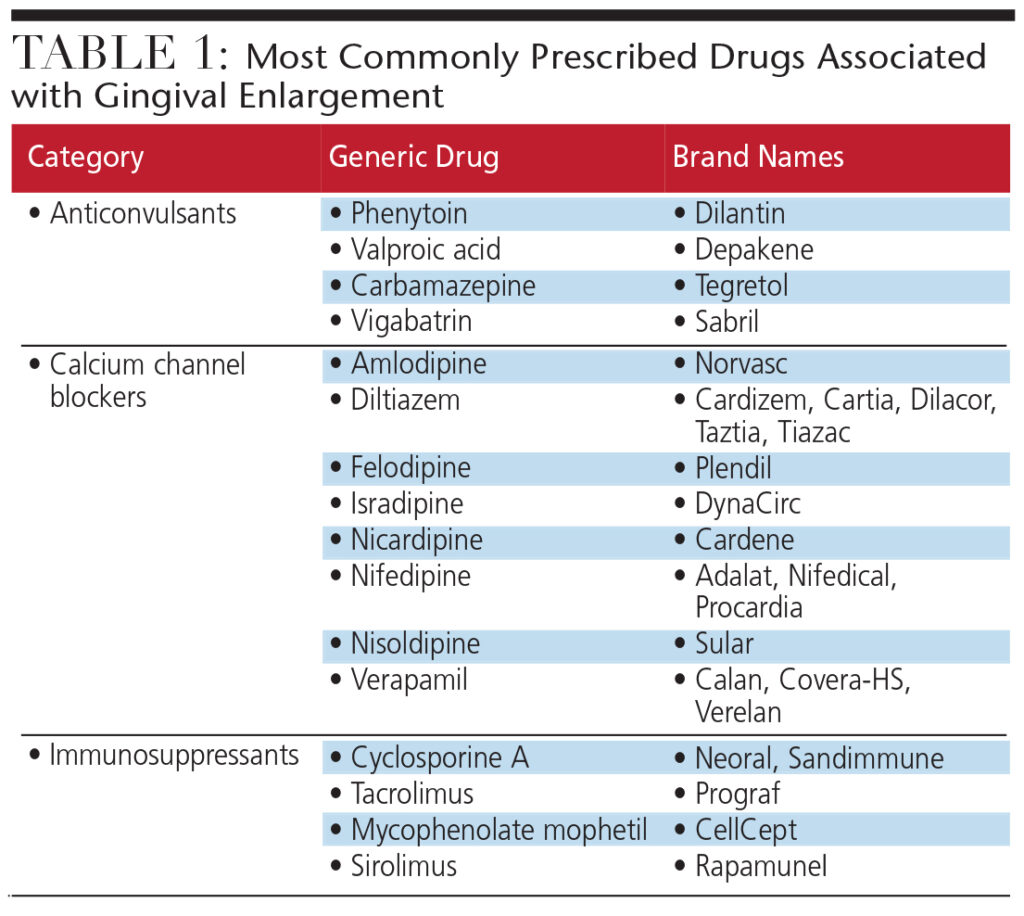
Bacteriile, virușii, neoplasmele și anumite medicamente pot afecta negativ sănătatea gingivală. Mărirea gingivală crește riscul de infecție, cariie și boală parodontală și afectează negativ estetica zâmbetului. Inițiată atât de factori sistemici, cât și de factori inflamatori, mărirea gingivală este adesea cauzată de medicamente obișnuite pe bază de rețetă. Aceste medicamente – anticonvulsivante, blocante ale canalelor de calciu (CCB) și imunosupresoare – promovează modificări ale funcției fibroblastelor, ceea ce duce la o creștere a matricei extracelulare a țesutului conjunctiv gingival (Tabelul 1). Pentru a restabili funcția normală a fibroblastului și a sănătății gingivale, este posibil să fie necesară înlocuirea medicamentului contravențional cu un alt medicament. Atunci când substituția nu este fezabilă, excizia chirurgicală a țesutului gingival poate oferi o ușurare temporară pacienților afectați de mărirea gingivală indusă de medicament.
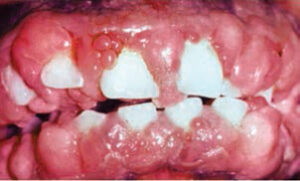
Descoperirea fenitoinei în 1938 de către Merritt și Putnam a furnizat o descoperire majoră în gestionarea pacienți cu epilepsie.1 La scurt timp după introducerea acesteia, totuși, au început să apară rapoarte care leagă fenitoina de creșterea gingivală.2 Sensibilitatea la acest medicament nu este universală, deoarece prevalența măririi benigne variază între subgrupurile populației. Mărirea gingivală indusă de anticonvulsivante este semnificativ mai mare în rândul copiilor și al pacienților instituționalizați. Pentru pacienții neinstituționalizați, prevalența creșterii exagerate gingivale cauzată de fenitoină este de aproximativ 50%, iar afecțiunea afectează cel mai adesea dinții anteriori maxilari (Figura 1). , atingând severitatea maximă aproximativ 12 luni până la 18 luni mai târziu.
Din 1938, au fost introduși mai mulți agenți anticonvulsivanti – inclusiv acid valproic, carbamazepină, fenobarbital și vigabatrin – în încercarea de a depăși efectele adverse ale fenitoinei . Au fost observate și cazuri de extindere gingivală la acești agenți, dar astfel de rapoarte sunt rare și slab documentate.
Datorită eficacității sale în controlul tulburărilor convulsive convulsive, precum și a costului redus și a disponibilității sale largi, fenitoina este în continuare medicamentul de elecție pentru tratarea epilepsiei – în special pentru crize de mal, lob temporal și convulsii psihomotorii. Mulți pacienți sunt reticenți să îl înlocuiască cu o nouă clasă de anticonvulsivante, făcând imperativ ca profesioniștii din domeniul sănătății orale să recunoască riscul crescut și să fie pregătiți să abordeze extinderea gingivală indusă de fenitoină în aceste populații de pacienți.
BLOCANTELE CANALULUI CALCIUM
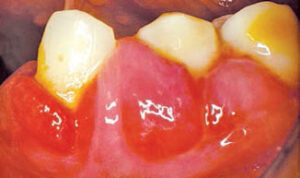
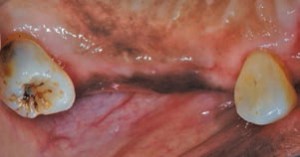
Această clasă de medicamente este utilizată pe scară largă pentru gestionarea hipertensiunii, anginei și a aritmiilor cardiace supraventriculare. Aceste medicamente își obțin principalele efecte terapeutice prin prevenirea influxului de ioni de calciu prin membranele celulare. Cu toate acestea, nu toate CCB afectează gingia în același mod. Nifedipina este CCB cel mai frecvent implicat în creșterea excesivă gingivală indusă de medicamente (Figura 2 până la Figura 4) .4 Lederman și colab. Au raportat pentru prima dată efectele sale negative orale în 1984, iar studiile ulterioare au arătat că prevalența efectelor adverse a variat de la 14% la 83% .5-7
Prevalența efectelor gingivale negative este semnificativ mai mică cu verapamil și amlodipină (4,2% și respectiv 3,3%).8,9 Numeroase rapoarte au asociat, de asemenea, extinderea gingivală cu noua generație de CCB, cum ar fi felodipina, nicardipina, manidipina și diltiazemul.
IMUNOSUPRESIVI
Imunosupresorii reduc incidența și severitatea respingerii alogrefelor în urma transplanturilor de organe majore (de exemplu, ficatul, pancreasul, inima sau plămânul), precum și pentru gestionarea afecțiunilor autoimune, cum ar fi artrita reumatoidă .
De la descoperirea sa de Borel și colab în 1977, ciclosporina A a devenit cel mai frecvent medicament prescris pentru prevenirea respingerii organelor.10 Poate exercita efecte secundare grave, din păcate, inclusiv nefrotoxicitatea, inducerea unei stări diabetice. , dureri de cap cronice și desfigurarea măririi gingivale (Figura 5). Prima publicare a creșterii excesive gingivale a fost raportată la pacienții cu transplant de rinichi la patru săptămâni până la șase săptămâni după doza inițială.11 Mărirea a fost mai pronunțată în ceea ce privește aspectul labial al gingiei și a fost asociată cu sângerări semnificative. Cu toate acestea, când dinții au fost extrasați chirurgical, mărirea a fost eliminată definitiv. Prevalența măririi gingivale asociate ciclosporinei A variază de la 8% la 81%, cu copii și adolescenți cu cel mai mare risc.12,13
Noile medicamente imunosupresoare, cum ar fi tacrolimus, micofenolatul mophetil și sirolimus, au furnizat opțiuni alternative pentru gestionarea pacienților cu transplant de organe fără riscul de creștere excesivă gingivală.14
CARACTERISTICI CLINICE
În timp ce manifestarea orală a fiecărui tip de mărire gingivală indusă de medicament este similară, nu este un factor de diagnostic. Păstrarea unui istoric medical detaliat al pacientului va ajuta profesioniștii în domeniul stomatologiei să realizeze un diagnostic precis. În stadiile lor inițiale, leziunile pot apărea ca mărire nodulară fermă a papilelor interdentare și pot apărea în toată cavitatea bucală. Excesul de creștere gingival afectează mai frecvent regiunea anterioară, cu o pronunțare mai mare pe suprafețele faciale / bucale decât suprafețele palatino-linguale.15 Mărirea poate varia de la o creștere ușoară a papilelor gingivale interproximale până la mărirea severă a țesuturilor marginale și papilare. În cazurile severe, întreaga papilă și țesuturile înconjurătoare sunt mărite, dând țesuturilor gingivale un aspect lobulat (Figura 6).
Mărirea se poate extinde coronal și poate interfera cu masticarea și vorbirea; în plus, în cazurile care implică dinții anteriori poate duce la probleme estetice. Țesutul crescut creează buzunare care pot adăposti microbi patogeni dincolo de acoperirea unei periuțe de dinți sau a aței dentare.
Deși aceste medicamente nu afectează în mod direct osul alveolar subiacent, mărirea gingivală poate deveni suprapusă la pacienții cu parodontită preexistentă, sau pacienții o pot dobândi concomitent. Mărirea gingivală se poate prezenta cu diferite forme, variind de la gingia neinflamată, fermă și fibroasă la țesutul gingival dominat de edem, eritem și sângerări.
DIAGNOSTIC DIFERENȚIAL
Excesul gingival indus de medicamente nu are o marker clinic distinctiv pentru a ajuta profesioniștii din domeniul sănătății orale să ajungă la un diagnostic precis. Aceste leziuni imită mai multe afecțiuni patologice care se manifestă în mod similar. Extinderea poate fi localizată sau generalizată. O supraaglomerare gingivală localizată poate fi cauzată de un abces parodontal, fibrom sau un granulom piogen (supraaglomerarea țesuturilor cauzată de iritații, traume sau fluctuații hormonale, cum ar fi experiența în timpul sarcinii). Natura locală a acestor leziuni – împreună cu semnele și simptomele clinice și istoricul medical și dentar al pacientului – ajută la diferențierea acestora de mărirea gingivală cauzată de utilizarea medicamentelor.
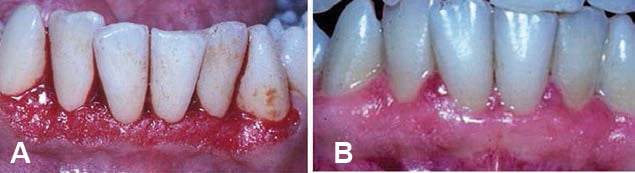
Mărire gingivală generalizată reprezintă o provocare diagnostic dificilă la unii pacienți. Cel mai frecvent factor implicat în majoritatea extinderii gingivale este biofilmul oral, care ar trebui tratat ca o creștere gingivală indusă de placă cu scalare și planificare a rădăcinilor, împreună cu o bună îngrijire de sine. Dacă leziunile persistă la trei săptămâni până la patru săptămâni după tratament, pacientul ar trebui trimis la un furnizor medical pentru a exclude boala sistemică ca factor cauzal. Diabetul nediagnosticat sau slab controlat este un vinovat major, provocând mărirea gingivală inflamatorie generalizată și distrugerea parodontală semnificativă.
Alte boli sistemice care pot provoca mărirea gingivală includ leucemia acută, granulomatoza Wegener și scorbutul. O creștere rapidă gingivală, însoțită de sângerări, poate indica prezența leucemiei mioblocale acute, a leucemiei mieloide cronice, a leucemiei limfocitare acute sau a leucemiei limfocitice cronice. Dintre pacienții diagnosticați cu leucemie mieloblastică acută, 5% prezintă mărirea gingivală ca primă complicație.16,17 Leucemia este o boală malignă, iar rezolvarea ei cu succes depinde de diagnosticul și tratamentul precoce. Profesioniștii din domeniul sănătății bucale ar trebui să trimită pacienții către un profesionist medical atunci când se constată o progresie rapidă a creșterii excesive.16,17
În granulomatoza Wegener, gingia apare umflată și roșu aprins, cu o suprafață granulară descrisă ca „gingii căpșuni. ” Diagnosticul diferențial este suspectat prin această manifestare clinică caracteristică, dar trebuie confirmat prin biopsie. Scorbutul, rezultatul deficitului de vitamina C, este destul de rar, dar pacienții afectați de această afecțiune pot prezenta umflături și sângerări gingivale severe, însoțite de dinți mobili. Clinicienii se pot baza pe o doză mare de vitamina C și pe terapie parodontală nechirurgicală pentru a rezolva extinderea gingivală în acest grup de pacienți.
În plus, creșterea excesivă generalizată se poate datora unei afecțiuni genetice rare numită fibromatoză gingivală ereditară, care este caracterizată printr-o mărire progresivă a gingiei. Aceste cazuri necesită de obicei intervenție chirurgicală pentru a îndepărta excesul de țesut gingival fibrotic, dar recurența leziunii este imprevizibilă. Natura fibrotică a acestor leziuni, împreună cu istoricul medical și familial al pacientului, le poate diferenția de medicament -progresie gingivală indusă.
ETIOLOGIE ȘI FACTORI DE RISC
Patogeneza inducerii medicamentului mărirea gingivală nu este pe deplin înțeleasă. S-ar putea datora unei reduceri a degradării colagenului de către colagenază sau a rezultatului supraproducției de substanță extracelulară din sol.18,19 Alte căi posibile sunt prezența unui subgrup de fibroblaste gingivale susceptibile genetic la aceste medicamente. efectul sinergic al citokinelor proinflamatorii (IL-1b și IL-6) în îmbunătățirea sintezei colagenului de către fibroblastele gingivale umane ca un alt posibil factor implicat în această extindere.21
Biofilmul este un factor de risc comun pentru toate formele de boală parodontală inflamatorie și prezența acesteia exacerbează mărirea gingivală indusă de medicamente. Alți factori de risc pot include sexul, deoarece bărbații sunt de trei ori mai predispuși să dezvolte o creștere excesivă gingivală decât femeile.22 Vârsta este invers corelată cu extinderea gingivală indusă de fenitoină și ciclosporină A, deoarece copiii și adolescenții au o prevalență mai mare a acestor leziuni decât adulții. .23 În ceea ce privește dozarea, există rapoarte contradictorii despre o asociere între severitatea extinderii și aportul zilnic al oricăreia dintre aceste clase de medicamente. Majoritatea rapoartelor nu au reușit să detecteze o relație semnificativă între dozajul medicamentului și severitatea măririi gingivale.18
TRATAMENT
Cel mai eficient tratament pentru extinderea gingivală indusă de medicament este retragerea droguri jignitoare. Furnizorii medicali pot înlocui CCB cu beta-blocante, diuretice sau inhibitori ai enzimei de conversie a angiotensinei, de exemplu – niciunul dintre aceștia nu afectează țesuturile orale. Fenitoina poate fi înlocuită cu carbamazepină, etosuximidă sau valproat de sodiu.24 Ciclosporina A poate fi substituită cu tacrolimus. În ciuda acestor opțiuni, medicii și pacienții sunt adesea reticenți să treacă la un regim diferit, mai ales atunci când boala este bine controlată sau au fost deja explorate alte opțiuni. Dacă schimbarea medicamentelor nu este o opțiune, unele leziuni pot fi gestionate nechirurgical. Leziunile ușoare ale măririi gingivale induse de CCB răspund favorabil la scalarea și planificarea rădăcinilor și la bucățile antimicrobiene.
O igienă orală bună este esențială în prevenirea inflamației ulterioare și menținerea rezultatelor pozitive obținute cu îngrijire profesională, inclusiv terapia periodontală nechirurgicală periodică.În ceea ce privește extinderea indusă de fenitoină, răspunsul gingival la descuamare și planificarea rădăcinii nu este la fel de favorabil datorită conținutului ridicat de colagen din leziuni, care previne contracția semnificativă a țesuturilor. gingivectomia poate elimina pseudo-buzunarele, restabilind arhitectura țesutului, aspectul și funcția. Această procedură se efectuează cu lame, cuțite chirurgicale, unități electrochirurgicale sau lasere (Figura 7). Repetarea creșterii gingivale induse de medicament a fost raportată în cazurile tratate fie cu metode chirurgicale, fie cu cele nechirurgicale – mai ales dacă încetarea medicamentului contravențional a fost doar temporară sau nu a fost o opțiune în primul rând. Recurența poate apărea încă din trei până la șase luni după intervenție și afectează până la 40% dintre pacienți.25 Recurența este mai frecventă în rândul celor cu igienă orală slabă sau care nu au acces la îngrijirea profesională (Figura 8). >
Mărirea gingivală indusă de medicament este o afecțiune frecventă care poate fi cauzată de o varietate de medicamente. Aceste leziuni nu au markeri clinici diferențiați de leziunile asociate plăcii și pot fi dificil de diagnosticat. Un istoric medical detaliat va ajuta ghidul clinicienilor cu privire la opțiunile de etiologie, diagnostic și tratament pentru pacienții care prezintă mărire gingivală indusă de medicament.
- Merritt HH, Putnam TJ. Articol de referință 17 septembrie 1938: Difenil hidantoinat de sodiu în tratamentul tulburărilor convulsive. JAMA. 1984; 251: 1062-1067.
- Kimball OP. Tratamentul epilepsiei cu difenilhidantoinat de sodiu. JAMA. 1939; 112: 1244–1245.
- Casetta I, Granieri E, Desidera M și colab. Exces de creștere gingivală indusă de fenitoină: un studiu transversal comunitar în Ferrara, Italia. Neuroepidemiologie. 1997; 16: 296-303.
- Butler RT, Kalkwarf KL, Kaldahl WB. Hiperplazie gingivală indusă de medicamente: fenitoină, ciclosporină și nifedipină. J Am Dent Conf. Univ. 1987; 114: 56–60.
- Lederman D, Lumerman H, Reuben S, Freedman PD. Hiperplazia gingivală asociată terapiei cu nifedipină. Raportul unui caz. Oral Surg Oral Med Oral Pathol. 1984; 57: 620-622.
- Barak S, Engelberg IS, Hiss J. Hiperplazia gingivală cauzată de nifedipină. Constatări histopatologice. J Parodontol. 1987; 58: 639-642.
- Fattore L, Stablein M, Bredfeldt G, Semla T, Moran M, Doherty-Greenberg JM. Hiperplazia gingivală: un efect secundar al nifedipinei și al diltiazemului. Spec Dentist. 1991; 11: 107–109.
- Miller CS, Damm DD. Incidența hiperplaziei gingivale induse de verapamil la o populație dentară. J Parodontol. 1992; 63: 453–456.
- Jorgensen MG. Prevalența hiperplaziei gingivale legate de amlodipină. J Parodontol. 1997; 68: 676-678.
- Borel JF, Feurer C, Magnée C, Stähelin H. Efectele noii peptide anti-limfocitice ciclosporina A la animale. Imunologie. 1977; 32: 1017-1025.
- Rateitschak-Plüss EM, Hefti A, Lörtscher R, Thiel G. Observație inițială că ciclosporina-A induce mărirea gingivală la om. J Clin Periodontol. 1983; 10: 237-246.
- Friskopp J, Klintmalm G. Lărgire gingivală. O comparație între primitorii de alogrefe renale tratați cu ciclosporină și azatioprină. Swed Dent J. 1986; 10: 85-96.
- Pernu HE, Pernu LM, Huttunen KR, Nieminen PA, Knuuttila ML. Excesul de creștere gingivală în rândul beneficiarilor de transplant renal legat de medicația imunosupresivă și de posibilii factori locali de fond. J Parodontol. 1992; 63: 548-553.
- Keown PA. Noi strategii imunosupresoare. Curr Opin Nephrol Hypertens. 1998; 7: 659-663.
- Marshall RI, Bartold PM. O analiză clinică a creșterii gingivale induse de medicamente. Aust Dent J. 1999; 44: 219-232.
- Demirer S, Ozdemir H, Sencan M, Marakoglu I. Hiperplazia gingivală ca manifestare orală de diagnostic precoce în leucemia monocitară acută: un raport de caz. Eur J Dent. 2007; 1: 111-114.
- Wu J, Fantasia JE, Kaplan R. Manifestări orale ale leucemiei mielomonocitare acute: un raport de caz și revizuirea clasificării leucemiilor. J Parodontol. 2002; 73: 664-668.
- Barclay S, Thomason JM, Idle JR, Seymour RA. Incidența și severitatea creșterii excesive gingivale induse de nifedipină. J Clin Periodontol. 1992; 19: 311-314.
- Lucas RM, Howell LP, Wall BA. Hiperplazia gingivală indusă de nifedipină. Un studiu histochimic și ultrastructural. J Parodontol. 1985; 56: 211-215.
- Pernu HE, Knuuttila MLE, Huttenen KRH, Tiilikainen ASK. Excesul de creștere gingivală indus de medicamente și antigenele majore de histocompatibilitate de clasa I1. Transplantul. 1994; 57: 1811-1813.
- Johnson RB, Zebrowski EJ, Dai X. Îmbunătățirea sinergică a sintezei proteinelor colagene de către fibroblastele gingivale umane expuse la nifedipină și interleukin-1-beta in vitro. J Oral Pathol Med. 2000; 29: 8-12.
- Ellis JS, Seymour RA, Steele JG, Robertson P, Butler TJ, Thomason JM. Prevalența creșterii excesive gingivale indusă de blocanții canalelor de calciu: un studiu comunitar. J Parodontol. 1999; 70: 63–67.
- Daley TD, Wysocki GP, Ziua C.Corelații clinice și farmacologice în hiperplazia gingivală indusă de ciclosporină. Oral Surg Oral Med Oral Pathol. 1986; 62: 417-421.
- Seymour RA, Smith DG, Turnbull DN. Efectul fenitoinei și valproatului de sodiu asupra sănătății parodontale a pacienților adulți epileptici. J Clin Periodontol. 1985; 12: 413-419.
- Ilgenli T, Atilla G, Baylas H. Eficacitatea terapiei parodontale la pacienții cu creștere excesivă gingivală indusă de medicamente. Rezultate pe termen lung. J Parodontol. 1999; 70: 967–972.