US Pharm. 2018; 43 (7): 22-26.
RÉSUMÉ: Les statines sont une classe de médicaments largement utilisés pour la prévention primaire et secondaire des événements cardiovasculaires. Avec six statines disponibles de manière générique, la sélection d’un agent approprié peut être déterminée sur la base de facteurs spécifiques au médicament, y compris des considérations de dosage, des interactions médicamenteuses et des événements indésirables. Des plans de soins individualisés peuvent être élaborés sur la base des données d’études cliniques importantes, des différences dans les directives et des recommandations de prise en charge actuelles pour deux événements indésirables majeurs associés à l’utilisation de statines.
La pierre angulaire du traitement de la dyslipidémie implique l’utilisation de Inhibiteurs de la 3-hydroxy-3-méthylglutaryl-coenzyme A réductase, plus communément appelés statines. Avec une variété d’options génériques sur le marché et des preuves solides étayant leur utilisation, les statines font partie des médicaments les plus prescrits dans le monde.1 Cependant, l’utilisation fréquente de ces agents a conduit à un examen continu de leur sécurité et à un débat permanent sur leur rôle dans la thérapie. Cet article, qui se concentre sur les statines génériques, mettra en évidence le débat sur le rôle des statines dans la thérapie, discutera de leur utilisation appropriée et explorera les preuves entourant deux événements indésirables majeurs.
Sur les sept statines différentes sur le marché, six sont disponibles de manière générique (TABLEAU 1) .2-7 Trois formulations de marque disponibles sont la pitavastatine (Livalo), la simvastatine suspension buvable (FloLipid) et la lovastatine à libération prolongée (Altoprev) .8-10 Le rôle des agents de marque dans le traitement est limité étant donné la disponibilité généralisée des options génériques.
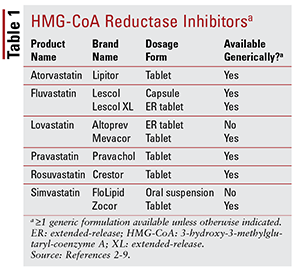
L’atorvastatine et la simvastatine sont également disponibles de manière générique dans plusieurs produits combinés. Il s’agit notamment de l’association d’atorvastatine et d’amlodipine, un inhibiteur calcique (CCB) indiqué pour l’hypertension, et de l’association de simvastatine et d’ézétimibe, un inhibiteur de l’absorption intestinale du cholestérol également indiqué pour l’hypercholestérolémie.11,12 Produits de statine et de niacine coformulés (niacine / lovastatine et niacine / simvastatine) ont été retirées du marché en 2016 en raison d’un manque de preuves indiquant que l’ajout de niacine chez les patients traités par statine réduit davantage les résultats cardiovasculaires (CV) au-delà de ce qui est observé avec les statines seules.13
RECOMMANDATIONS DE TRAITEMENT
Les statines se sont avérées efficaces à plusieurs reprises pour réduire les taux de LDL-cholestérol (LDL-C) et de triglycérides tout en augmentant les taux de HDL-cholestérol (HDL-C ).14 De plus, il a été démontré qu’elles améliorent les résultats axés sur le patient, tels que les événements CV majeurs (CVE), à la fois dans la prévention primaire et secondaire.15-19
Plusieurs directives de traitement fortement débattues discutent du rôle des statines dans le traitement de l’hy perlipidémie. Celles-ci incluent la ligne directrice 2013 de l’American College of Cardiology / American Heart Association (ACC / AHA) et la ligne directrice 2017 de l’American Academy of Clinical Endocrinology (AACE ).14,20 Les deux lignes directrices suggèrent qu’après la mise en œuvre des modifications du mode de vie, y compris l’arrêt du tabac, le respect un régime d’exercice, et suivant un régime alimentaire sain pour le cœur, les statines sont un traitement de première intention à la fois pour la prévention primaire et secondaire des maladies cardiovasculaires (MCV) .14,20 Les lignes directrices diffèrent cependant quant à la façon de déterminer quelles statines sont appropriées pour lesquelles les patients.
La directive 2013 de l’ACC / AHA a introduit quatre groupes de traitement à cibler pour le traitement par statine:
1. Patients ayant des antécédents de maladie cardiovasculaire athéroscléreuse (ASCVD), y compris ceux ayant déjà eu un événement (c.-à-d. Syndromes coronariens aigus, antécédents d’infarctus du myocarde, angor stable ou instable, revascularisation coronarienne ou autre artérielle, accident vasculaire cérébral, accident ischémique transitoire ou maladie artérielle périphérique présumée) origine athéroscléreuse).
2. Patients sans antécédent d’événement ASCVD qui ont un taux de LDL-C de 190 mg / dL ou plus. L’âge n’est pas un motif d’exclusion de ce critère.
3. Patients âgés de 40 à 75 ans atteints de diabète mais sans antécédent d’événement ASCVD et ayant un taux de LDL-C compris entre 70 et 189 mg / dL.
4. Patients âgés de 40 à 75 ans sans diabète, sans antécédent d’événement ASCVD et avec un taux de LDL-C compris entre 70 et 189 mg / dL.20
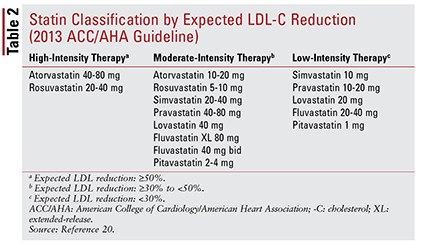
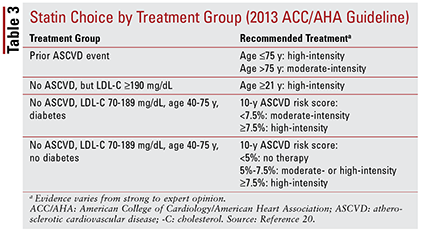
La directive ACC / AHA a également introduit l’idée de regrouper les statines par intensité (c.-à-d. leur capacité attendue de réduction du LDL-C) (TABLEAU 2) .20 Sur la base du groupe de traitement (tel que défini ci-dessus), la ligne directrice recommande des intensités de statines spécifiques pour des situations cliniques particulières (TABLEAU 3) .20 Plusieurs groupes de traitement exiger le calcul d’un score de risque ASCVD à l’aide d’un estimateur de risque ASCVD. Cet outil en ligne prend en compte l’âge, le sexe, la race, la pression artérielle systolique du patient, le cholestérol total, le HDL-C et les antécédents médicaux significatifs pour le traitement de l’hypertension, le diabète ou le tabagisme.21 Une fois que toutes les entrées ont été saisies, le 10 du patient – le risque annuel de subir un événement ASCVD est calculé.
Ces recommandations ne s’appliquent pas automatiquement à certains sous-groupes de patients. Par exemple, l’utilisation de statines chez les personnes âgées doit être abordée avec prudence. Bien que l’utilisation de statines pour la prévention secondaire chez les patients âgés confère des avantages significatifs, son utilisation pour la prévention primaire n’est pas claire.22-24 De plus, les patients souffrant d’insuffisance cardiaque ne se sont pas avérés bénéficier des mêmes avantages du traitement par statines que ceux qui ne sont pas Sur la base de ces résultats, les recommandations de traitement incluent la limitation de l’initiation des statines de haute intensité aux patients âgés de moins de 75 ans et peut-être d’éviter les statines chez les patients souffrant d’insuffisance cardiaque.20 Dans l’ensemble, la décision d’utiliser des statines dans ces groupes n’est pas claire et doit impliquer une conversation continue entre le fournisseur et le patient sur les risques et les avantages potentiels du traitement.20
Contrairement à la recommandation 2013 de l’ACC / AHA d’initier le traitement selon la classification des groupes de traitement, la directive 2017 de l’AACE recommande que les patients individuels soient Selon cette directive, le risque pour le patient est déterminé par une variété nd facteurs de risque non traditionnels. Les individus sont ensuite classés dans l’un des cinq groupes à risque, chacun avec un objectif correspondant LDL-C et non-HDL-C (TABLEAU 4). Sur la base des niveaux actuels et des objectifs individualisés, les statines seules ou en association avec d’autres agents doivent être initiées en fonction de la capacité attendue de réduction du LDL-C ou non-HDL-C.14

Le traitement combiné impliquant l’ajout d’un deuxième agent au traitement par statines en cours reste un sujet quelque peu controversé. Alors que les essais et directives antérieurs ont minimisé l’ajout d’autres agents au traitement de fond par les statines, des études récentes et des déclarations de consensus – y compris celle de l’ACC / AHA – soutiennent l’utilisation de l’ézétimibe, de l’évolocumab ou de l’alirocumab, les deux derniers étant la proprotéine convertase subtilisine / les inhibiteurs de la kexine de type 9, comme traitement d’appoint pour la prévention secondaire.20,26-31 Cela dit, les statines restent un traitement de première intention universel en prévention primaire et secondaire; le rôle définitif d’autres agents spécifiques reste incertain.
SÉLECTION DES STATINES
Le choix du traitement par statines commence par l’approche thérapeutique préférée du clinicien, qu’il s’agisse de la méthode ACC / AHA de traitement par statine groupes ou la méthode AACE des objectifs LDL-C ou non-HDL-C. À partir de là, les propriétés de chaque statine doivent être prises en compte pour déterminer la meilleure option pour chaque patient. Toutes les statines ne sont pas égales et il existe plusieurs différences clés qui peuvent influencer la sélection des patients, y compris les considérations posologiques, les interactions médicamenteuses et les événements indésirables (EI).
Dosage
Bien que la plupart des statines puissent être pris indépendamment des repas, la lovastatine à libération immédiate (IR) doit être prise avec le repas du soir en raison de l’augmentation de la biodisponibilité.4 Cependant, l’inverse est vrai pour la lovastatine à libération prolongée, qui ne doit pas être prise avec de la nourriture en raison d’une biodisponibilité réduite. En outre, bien que toutes les statines puissent être administrées une fois par jour, la fluvastatine IR et la lovastatine peuvent nécessiter une administration deux fois par jour.3,4 Enfin, alors que l’atorvastatine, la pravastatine et la rosuvastatine peuvent être administrées à tout moment de la journée, la fluvastatine, la lovastatine et La simvastatine doit être prise le soir.3,4,7 La simvastatine, en particulier, s’est avérée avoir une efficacité significativement différente lorsqu’elle est prise le soir par rapport au matin32.
Interactions médicamenteuses
Chaque statine a des préoccupations concernant les interactions médicament-médicament et médicament-aliment en raison des voies spécifiques par lesquelles chacune est métabolisée (TABLEAU 5). Il existe trop d’interactions médicamenteuses pour en discuter en détail; par conséquent, seuls quelques-uns sont décrits ci-dessous.
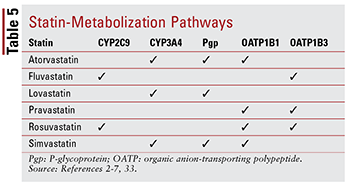
Fibrates: Bien que la combinaison d’un fibrate et d’une statine ne modifie pas de manière significative les résultats cliniques, les patients peuvent toujours se voir prescrire du gemfibrozil, du fénofibrate ou de l’acide fénofibrique en association avec une statine pour cibler une hypertriglycéridémie sévèrement non contrôlée.14,20,26,33 Parce que ces deux classes sont associés à une toxicité musculaire, la polythérapie augmente considérablement ce risque par rapport à l’un ou l’autre des traitements seuls.33 Cette toxicité additive est plus fréquemment observée avec le gemfibrozil qu’avec d’autres fibrates.33 Par conséquent, l’utilisation du gemfibrozil est contre-indiquée avec la simvastatine et doit être évitée avec d’autres statines.7,20 Si une statine et un fibrate sont utilisés ensemble, le fénofibrate ou l’acide fénofibrique est préférable.20,33 Cependant, si le gemfibrozil doit être utilisé, fluvastatine – ou, avec une surveillance étroite, l’atorvastatine ou la rosuvastatine (maximum 10 mg par jour ) – est l’agent de choix.33
Amiodarone: cet agent antiarythmique indiqué pour la fibrillation ventriculaire est un inhibiteur connu de la glycoprotéine P (Pgp) et du système enzymatique CYP450, en particulier le CYP3A4 et, dans une moindre mesure, le CYP2C9.33,34 Par conséquent, il existe des doses maximales recommandées pour la lovastatine (maximum 40 mg par jour) et la simvastatine (maximum 20 mg par jour) lorsqu’elles sont utilisées avec l’amiodarone.4,7,33 Bien que l’atorvastatine soit métabolisée par le CYP3A4, aucun ajustement posologique n’est nécessaire (comme pour les autres statines) car les données ne suggèrent pas d’effets indésirables graves lors de l’utilisation concomitante d’atorvastatine et d’amiodarone.2,33
BCC: Il a été démontré que les CCB dihydropyridine (amlodipine) et non dihydropyridine (diltiazem, vérapamil) ont des interactions médicamenteuses significatives avec les statines . De même que l’amiodarone, l’amlodipine, le diltiazem et le vérapamil inhibent le CYP3A4.33,35-37 L’amlodipine a également un effet inhibiteur sur la Pgp.33,35 Sur la base des EI rapportés dans la littérature, une posologie quotidienne maximale de 20 mg de lovastatine est recommandée lorsque utilisé avec l’amlodipine, le diltiazem ou le vérapamil.4,33 Il est également recommandé que la simvastatine ne dépasse pas 20 mg lorsqu’elle est utilisée avec l’amlodipine, mais une dose inférieure de 10 mg doit être administrée lorsqu’elle est utilisée avec le diltiazem et le vérapamil.7,33 Aucune posologie spécifique des recommandations existent avec l’atorvastatine, bien qu’il faille faire preuve de prudence lorsqu’elle est administrée avec l’un ou l’autre des BCC non dihydropyridiniques.2,33
Effets indésirables du médicament
Les statines sont généralement bien tolérées; cependant, les taux d’abandon restent élevés38. L’arrêt du traitement par statine et l’échec de la reprise du traitement par statine après la survenue d’effets indésirables médicamenteux sont associés à une augmentation des taux de CVE.39 Les préoccupations des patients concernant la sécurité des statines à la lumière de deux EI majeurs liés aux statines— myotoxicité et diabète d’apparition récente – peuvent conduire à l’arrêt des statines.
Myotoxicité: les statines ont longtemps été associées à une toxicité musculaire, y compris la myalgie (douleur musculaire sans augmentation de la créatine kinase), la myopathie (terme général pour le muscle maladie) et la myosite (inflammation musculaire), dont les deux derniers impliquent une élévation significative de la CK.40,41 Toutes les statines partagent un avertissement concernant l’effet secondaire rare mais grave de la rhabdomyolyse.2-7 Cependant, la myotoxicité attribuée aux statines est souvent en raison de l’effet nocebo; c’est-à-dire qu’une personne croit qu’un médicament causera un préjudice et que, par la suite, le médicament causera le préjudice anticipé.42,43 Par conséquent, pour garantir le meilleur résultat, les pharmaciens doivent bien connaître cet effet secondaire fréquemment signalé et sa prise en charge appropriée.
Il est incorrect de supposer que tous les rapports de symptômes musculaires sont dus à l’effet nocebo; Une vérification appropriée des antécédents médicaux du patient (PMH), la description de la douleur et l’association avec un traitement par statine est impérative.44 Premièrement, un examen de la PMH pour les élévations de la CK et d’autres causes potentielles de douleur ou de faiblesse musculaire permet au clinicien de traiter une alternative. physiopathologie sous-jacente ou corriger les facteurs susceptibles de modifier le métabolisme des statines. Les causes courantes incluent la vieillesse, les interactions médicamenteuses, une fonction rénale ou hépatique altérée, une activité physique accrue et une carence en vitamine D.20,41
Ensuite, le clinicien doit comparer la présentation du patient avec les symptômes fréquemment observés induits par les statines . La toxicité musculaire induite par les statines se manifeste généralement par une douleur, une sensibilité, des crampes et une faiblesse, généralement dans les muscles des jambes.20,41 Ces symptômes sont généralement pires après l’exercice et ne disparaissent pas sans l’arrêt de l’agent incriminé.41
La dernière étape consiste à déterminer s’il existe une relation de cause à effet entre les symptômes et l’utilisation de statines. Lorsqu’une statine est suspectée d’être la cause de symptômes légers à modérés, un arrêt temporaire est recommandé. Si les symptômes ne disparaissent pas après environ 2 semaines, la statine n’en est probablement pas la cause et doit être réinstaurée à la dose initiale. Cependant, si les symptômes disparaissent, un nouvel essai de la même statine à la même dose ou à une dose inférieure doit être entrepris. Si des symptômes similaires sont alors ressentis, la statine doit être présumée en être la cause et arrêtée. Lors de la résolution des symptômes, une faible dose d’une statine alternative doit être initiée et titrée à la dose maximale tolérée.20,41 L’acceptation et la compréhension par le patient de ce processus sont importantes car l’effet nocebo peut autrement conduire à d’autres réactions perçues.
Plusieurs autres stratégies existent pour gérer et prévenir ces symptômes. Premièrement, en raison d’une probabilité plus élevée de symptômes, le clinicien peut choisir d’éviter les statines les plus lipophiles (lovastatine et simvastatine) au profit de statines plus hydrophiles (fluvastatine, pravastatine et rosuvastatine) .44 La simvastatine 80 mg ne doit jamais être initiée comme nouvelle traitement chez tout patient en raison d’une fréquence inhabituellement élevée de symptômes musculaires associés aux statines.7,45 Les thérapies alternatives, telles que la coenzyme Q10, n’ont pas démontré de bénéfice constant mais peuvent être envisagées chez les patients présentant des symptômes induits psychologiquement.41,44,46 Enfin, une posologie à intervalle prolongé, qui consiste à administrer des statines plusieurs fois par semaine plutôt qu’une fois par jour, peut être envisagée. Cette approche améliore l’observance et les profils lipidiques chez les patients ayant déjà subi une intolérance aux statines.47-49
Nouveau diabète: un EI important associé à l’utilisation de statines est le diabète d’apparition récente. Il a été démontré que les statines augmentent le risque de développement du diabète, bien que plusieurs mises en garde importantes existent.50 Premièrement, bien que cela puisse être considéré comme un effet de classe, le risque réel de chaque statine spécifique est encore inconnu.51,52 Dans la plus grande méta -analyse à ce jour, la pravastatine présentait le risque le plus faible, la simvastatine et l’atorvastatine présentaient un risque modéré, et la rosuvastatine présentait le risque le plus élevé de provoquer un diabète d’apparition récente.53 Aucun de ces résultats n’était cependant statistiquement significatif53. le risque augmente à mesure que la dose de statine augmente de manière irrégulière.54
Le diabète induit par les statines est le plus répandu chez les personnes déjà à haut risque de développer un diabète.50,54 Cela comprend les patients plus âgés et ceux atteints de prédiabète ou métabolique. 50,55 Une constatation cohérente a été que, pour chaque nouveau cas de diabète incident causé par des statines, plusieurs CVE peuvent être évitées chez les patients à risque élevé.50 Par conséquent, les pharmaciens devraient conseiller un x les utilisateurs de statines à risque modéré ou élevé de complications CV que le risque de développer un diabète est plus que compensé par les avantages de la réduction du risque CV. Cependant, le rapport bénéfice / risque n’est pas clair chez les patients présentant un très faible risque de CVE.50
CONCLUSION
Bien que le traitement par statines ne soit pas sans risques, ses bénéfices en termes de réduction des résultats CV ont en a fait la pierre angulaire de la prévention de la CVE. Les lignes directrices disponibles diffèrent considérablement, mais la seule constante est que les statines doivent être un traitement de première intention pour la prévention primaire et secondaire chez presque tous les patients. La disponibilité générique généralisée des statines a rendu ces agents de plus en plus accessibles. En comprenant que toutes les statines ne sont pas identiques, le pharmacien peut aider à garantir le meilleur résultat possible pour chaque patient.
1. IMS Institute for Healthcare Informatics. Utilisation et dépenses en médicaments aux États-Unis: examen de 2015 et perspectives jusqu’en 2020. https://morningconsult.com/wp-content/uploads/2016/04/IMS-Institute-US-Drug-Spending-2015.pdf. Consulté le 18 mars 2018.
2. Notice d’emballage de Lipitor (atorvastatine). New York, NY: Pfizer, Inc; Juin 2017.
3. Notice d’emballage Lescol / Lescol XL (fluvastatine). East Hanover, NJ: Novartis Pharmaceuticals Corp; Août 2017.
4. Notice d’emballage de Mevacor (lovastatine). Whitehouse Station, NJ: Merck & Co, Inc; Février 2014.
5. Notice d’emballage de Pravachol (pravastatine). Princeton, NJ: Compagnie Bristol-Myers Squibb; Juillet 2016.
6. Notice d’emballage de Crestor (rosuvastatine). Wilmington, DE: AstraZeneca Pharmaceuticals LP; Août 2017.
7. Notice d’emballage de Zocor (simvastatine). Whitehouse Station, NJ: Merck & Co, Inc; Février 2015.
8. Notice d’emballage d’Altoprev (lovastatine). Zug, Suisse: Covis Pharma; Avril 2017.
9. Notice d’emballage de FloLipid (simvastatine). Brooksville, FL: Salerno Pharmaceuticals LP; Juillet 2017.
10. Notice d’emballage de Livalo (pitavastatine). Montgomery, AL: Kowa Pharmaceuticals America, Inc; Novembre 2016.
11. Notice d’emballage de Caduet (amlodipine / atorvastatine). New York, NY: Pfizer Inc; Octobre 2017.
12. Notice d’emballage de Vytorin (ézétimibe / simvastatine). Whitehouse Station, NJ: Merck & Co, Inc; Février 2018.
13. AbbVie Inc .; retrait de l’approbation des nouvelles demandes de médicaments pour Advicor et Simcor. www.federationregister.gov/documents/2016/04/18/2016-08894/abbvie-inc-withdrawal-of-approval-of-new-drug-applications-for-advicor-and-simcor. Consulté le 18 mars 2018.
14. Jellinger PS, Handelsman Y, Rosenblit PD, et al. Association américaine des endocrinologues cliniques et directives de l’American College of Endocrinology pour la gestion de la dyslipidémie et la prévention des maladies cardiovasculaires. Endocr Pract. 2017; 23 (suppl 2): 1-87.
15. LaRosa JC, Grundy SM, Waters DD, et al. Abaissement intensif des lipides avec l’atorvastatine chez les patients atteints de maladie coronarienne stable. N Engl J Med. 2005; 352: 1425-1435.
16. Ridker PM, Danielson E, Fonseca FA et al. Rosuvastatine pour prévenir les événements vasculaires chez les hommes et les femmes présentant une protéine C-réactive élevée. N Engl J Med. 2008; 359: 2195-2207.
17. Mihaylova B, Emberson J, Blackwell L et coll. Les effets de la réduction du cholestérol LDL avec un traitement par statine chez les personnes à faible risque de maladie vasculaire: méta-analyse des données individuelles de 27 essais randomisés. Lancette. 2012; 380: 581-590.
18. Baigent C, Landray MJ, Reith C et coll. Les effets de la réduction du cholestérol LDL avec la simvastatine plus l’ézétimibe chez les patients atteints d’insuffisance rénale chronique (étude de la protection cardiaque et rénale): un essai randomisé contrôlé par placebo Lancette. 2011; 377: 2181-2192.
19. Cannon CP, Braunwald E, McCabe CH, et al.Abaissement lipidique intensif versus modéré avec des statines après des syndromes coronariens aigus N Engl J Med. 2004; 350: 1495-1504.
20. Stone NJ, Robinson JG, Lichtenstein AH et coll. 2013 ACC / AHA guideline on the treatment of blood cholesterol to reduction atherosclerotic cardiovascular risk in adults: a report of the American College of Cardiology / American Heart Association Task Force on Practice Guidelines. Circulation. 2014; 129 (25 suppl 2): S1-S45.
21. Collège américain de cardiologie. ASCVD Risk Estimator Plus. http://tools.acc.org/ASCVD-Risk-Estimator. Consulté le 18 mars 2018.
22. Wenger NK, Lewis SJ, Herrington DM et al. Résultats de l’utilisation d’atorvastatine à dose élevée ou faible chez les patients de 65 ans ou plus atteints d’une maladie coronarienne stable. Ann Intern Med. 2007; 147: 1-9.
23. Shepherd J, Blauw GJ, Murphy MB et coll. Pravastatine chez les personnes âgées à risque de maladie vasculaire (PROSPER): un essai contrôlé randomisé. Lancette. 2002; 360: 1623-1630.
24. Teng M, Lin L, Zhao YJ et al. Statines pour la prévention primaire des maladies cardiovasculaires chez les patients âgés: revue systématique et méta-analyse. Vieillissement des drogues. 2015; 32: 649-661.
25. Kjekshus J, Apetrei E, Barrios V et al. Rosuvastatine chez les patients âgés atteints d’insuffisance cardiaque systolique. N Engl J Med. 2007; 357: 2248-2261.
26. Ginsberg HN, Elam MB, Lovato LC et al. Effets de la thérapie lipidique combinée dans le diabète sucré de type 2. N Engl J Med. 2010; 362: 1563-1574.
27. Kastelein JJ, Akdim F, Stroes ES et coll. Simvastatine avec ou sans ézétimibe dans l’hypercholestérolémie familiale. N Engl J Med. 2008; 358: 1431-1443.
28. Cannon CP, Blazing MA, Giugliano RP, et al. Ézétimibe ajouté au traitement par statine après des syndromes coronariens aigus. N Engl J Med. 2015; 372: 2387-2397.
29. Sabatine MS, Giugliano RP, Keech AC, et al. Evolocumab et résultats cliniques chez les patients atteints de maladies cardiovasculaires. N Engl J Med. 2017; 376: 1713-1722.
30. Lloyd-Jones DM, Morris PB, Ballantyne CM et coll. Mise à jour ciblée de 2017 de la voie de décision de consensus d’experts de l’ACC 2016 sur le rôle des thérapies non statiques pour la réduction du cholestérol LDL dans la gestion du risque de maladie cardiovasculaire athéroscléreuse: un rapport de l’American College of Cardiology Task Force on Expert Consensus Decision Pathways. J Am Coll Cardiol. 2017; 70: 1785-1822.
31. ODYSSEY Résultats: les résultats suggèrent que l’utilisation de l’inhibiteur PCSK9 réduit les événements CV, LDL-C chez les patients atteints de SCA. Collège américain de cardiologie. www.acc.org/latest-in-cardiology/articles/2018/03/05/15/53/sat-9am-odyssey-outcomes-cv-outcomes-with-alirocumab-after-acs-acc-2018. Consulté le 20 juin 2018.
32. Wallace A, Chinn D, Rubin G. Prenant la simvastatine le matin par rapport au soir: essai contrôlé randomisé. BMJ. 2003; 327: 788.
33. Wiggins BS, Saseen JJ, Page RL et coll. Recommandations pour la gestion des interactions médicamenteuses cliniquement significatives avec les statines et certains agents utilisés chez les patients atteints de maladie cardiovasculaire: une déclaration scientifique de l’American Heart Association. Circulation. 2016; 134: e468-e495.
34. Notice d’emballage de Pacerone (amiodarone). Maple Grove, MN: Upsher-Smith Laboratories LLC; Juillet 2017.
35. Notice d’emballage Norvasc (amlodipine). New York, NY: Pfizer Inc; Octobre 2017.
36. Notice d’emballage de Cardizem (diltiazem). Bridgewater, NJ: Valeant Pharmaceuticals; Novembre 2016.
37. Notice d’emballage Calan (vérapamil). New York, NY: Pfizer Inc; Septembre 2017.
38. Riaz H, Khan AR, Khan MS et al. Méta-analyse d’essais contrôlés randomisés contrôlés par placebo sur la prévalence de l’intolérance aux statines. Suis J Cardiol. 2017; 120: 774-781.
39. Zhang H, Plutzky J, Shubina M, Turchin A. Poursuite des ordonnances de statines après des effets indésirables et des résultats pour les patients: une étude de cohorte. Ann Intern Med. 2017; 167: 221-227.
40. Tomaszewski M, Stepien KM, Tomaszewska J, Czuczwar SJ. Myopathies induites par les statines. Pharmacol Rep.2011; 63: 859-866.
41. Stroes ES, Thompson PD, Corsini A et al. Symptômes musculaires associés aux statines: impact sur le traitement par statine – Déclaration du groupe de consensus de la European Atherosclerosis Society sur l’évaluation, l’étiologie et la prise en charge. Eur Heart J. 2015; 36: 1012-1022.
42. Gupta A, Thompson D, Whitehouse A et al. Evénements indésirables associés à un traitement par statine en aveugle, mais pas en aveugle, dans l’étude anglo-scandinave sur les résultats cardiaques – Bras hypolipidémiant (ASCOT-LLA): un essai randomisé en double aveugle contrôlé par placebo et son extension non randomisée et non aveugle phase. Lancette. 2017; 389: 2473-2481.
43. Pedro-Botet J, Rubiés-Prat J. Symptômes musculaires associés aux statines: attention à l’effet nocebo. Lancette. 2017; 389: 2445-2446.
44. Laufs U, Filipiak KJ, Gouni-Berthold I, et al. Aspects pratiques de la prise en charge des symptômes musculaires associés aux statines (SAMS). Atheroscler Suppl. 2017; 26: 45-55.
45. Communication de la FDA sur la sécurité des médicaments: nouvelles restrictions, contre-indications et limitations de dose de Zocor (simvastatine) pour réduire le risque de blessures musculaires. www.fda.gov/Drugs/DrugSafety/ucm256581.htm. Consulté le 18 mars 2018.
46.Banach M, Serban C, Sahebkar A et coll. Effets de la coenzyme Q10 sur la myopathie induite par les statines: une méta-analyse d’essais contrôlés randomisés. Mayo Clin Proc. 2015; 90: 24-34.
47. Goldberg AS, DeGorter MK, Ban MR, et al. Efficacité et concentrations plasmatiques du médicament avec une posologie non quotidienne de rosuvastatine. Can J Cardiol. 2013; 29: 915-919.
48. Matalka MS, Ravnan MC, Deedwania PC. Une autre dose quotidienne d’atorvastatine est-elle efficace dans le traitement des patients atteints d’hyperlipidémie? L’étude sur un jour alterné par rapport à la posologie quotidienne de l’atorvastatine (ADDAS). Am Heart J. 2002; 144: 674-677.
49. Copher HR, Stewart RD. Dosage quotidien versus dosage un jour sur deux de la simvastatine chez les patients atteints d’hypercholestérolémie. Pharmacothérapie. 2002; 22: 1110-1116.
50. Rochlani Y, Kattoor AJ, Pothineni NV, et al. Équilibrer la prévention primaire et la prévention du diabète sucré induit par les statines. Suis J Cardiol. 2017; 120: 1122-1128.
51. Corrao G, Ibrahim B, Nicotra F et coll. Les statines et le risque de diabète: preuves d’une vaste étude de cohorte basée sur la population. Traitements diabétiques. 2014; 37: 2225-2232.
52. Lim S, Oh PC, Sakuma I, Koh KK. Comment équilibrer les avantages cardiorénométaboliques et les risques des statines. Athérosclérose. 2014; 235: 644-648.
53. Navarese EP, Buffon A, Andreotti F, et al. Méta-analyse de l’impact de différents types et doses de statines sur le diabète sucré d’apparition récente. Suis J Cardiol. 2013; 111: 1123-1130.
54. Crandall JP, Mather K, Rajpathak SN et al. Utilisation de statines et risque de développer un diabète: résultats du programme de prévention du diabète. BMJ Open Diabetes Res Care. 2017; 5: e000438.
55. Ganda OP. Diabète induit par les statines: incidence, mécanismes et implications. F1000Res. 2016; 5.