Quand vous voyez le tableau périodique, qu’est-ce qui vous vient à l’esprit? Les morceaux sur une planche de scrabble? Peut-être pensez-vous à votre cours de chimie au lycée. Peut-être pensez-vous à la table colorée collée sur le mur d’une salle de conférence à l’université. Vous vous souvenez peut-être que votre professeur préféré a mis le feu à quelque chose devant la classe. Je suis professeur adjoint de chimie à l’Université de Richmond et quand j’entends l’expression «le tableau périodique», je pense à la vie.
Je pense à la façon dont les molécules et les produits chimiques qui nous entourent et dictent notre quotidien les activités sont constituées des éléments sur cette table – elles soutiennent notre vie, elles apportent de la beauté au monde et elles sont vitales en médecine.
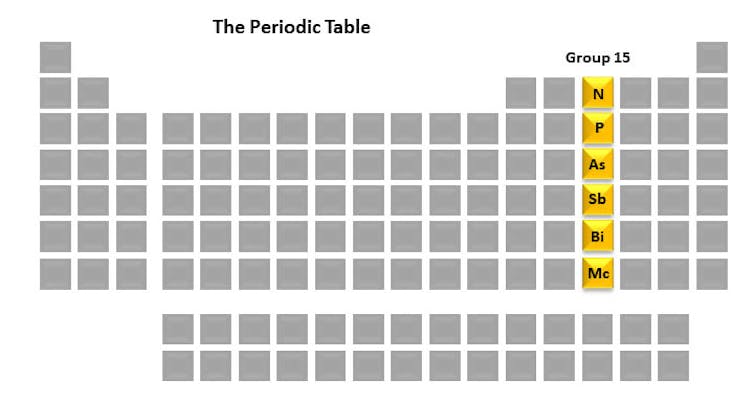
Chaque colonne du tableau périodique est appelée un groupe. Chaque membre du groupe a une disposition similaire d’électrons qui peut entraîner des propriétés chimiques similaires. Le groupe 15 éléments – azote, phosphore, arsenic, antimoine, bismuth et moscovium – m’intéressent en raison de leur rôle central dans la vie, ainsi que dans mon laboratoire de recherche. Un élément que nous étudions est le phosphore à cause de son rôle intégral dans le sort des cellules.
Mais avant d’entrer dans ces détails, examinons brièvement chacun des éléments du groupe 15. Ils constituent un ensemble unique dans leur histoire, leurs utilisations et leurs propriétés.
Groupe 15 – Donner la vie et causer la mort
L’azote (N) sous sa forme atmosphérique (N₂) constitue approximativement 78% de l’air que nous respirons. Lorsque les bactéries vivant dans les racines des plantes le convertissent en une forme utilisable par un processus appelé fixation de l’azote, cette forme élémentaire d’azote est incorporée dans de nombreux composés nécessaires à la vie – protéines et ADN, par exemple. Au bas de la colonne se trouve le Moscovium (Mc), ce qui est intéressant car il n’existe pas vraiment dans la nature. C’est un élément radioactif qui ne peut être généré que dans un laboratoire et qui survit moins d’une seconde.
L’arsenic (As) peut vous être familier en raison de son association avec des empoisonnements. En 1494, Pico della Mirandola, philosophe humaniste italien de la Renaissance, fut empoisonné par l’arsenic, bien que les détails entourant sa mort prématurée soient encore débattus. Pendant longtemps, on a cru que Napoléon Bonaparte était mort d’une exposition à l’arsenic en 1821, mais après des comparaisons approfondies d’échantillons de cheveux préservés à différentes étapes de sa vie, les chercheurs ont conclu que l’augmentation des niveaux d’arsenic était très probablement due aux techniques de conservation de l’époque. Plus récemment, l’Organisation mondiale de la santé a estimé que l’eau potable contaminée par l’arsenic au Bangladesh a entraîné plus de 9 000 décès en 2001. On ne comprend pas complètement comment l’arsenic empoisonne et tue, mais il ne fait aucun doute que l’élément provoque la destruction d’organes vitaux chez l’homme corps.

Lorsque l’élément antimoine (Sb) est combiné avec trois atomes d’oxygène pour former du trioxyde d’antimoine, il est largement utilisé comme retardateur de flamme pour les meubles, les tapis , rideaux, caoutchouc, plastiques et adhésifs. Les quantités de cette molécule dans ces produits ménagers ont tendance à être très petites et ces niveaux d’antimoine sont considérés comme sûrs.
Le bismuth (Bi) est un métal trouvé dans la même ligne du tableau périodique qu’un certain nombre de métaux toxiques; cependant, les composés contenant du bismuth sont inoffensifs. Les composés de bismuth peuvent être trouvés dans les cosmétiques en raison de leur miroitement argenté distinctif et souhaitable. Même si vous n’avez pas utilisé de produits de soins personnels contenant du bismuth, vous l’avez probablement rencontré dans le célèbre antiacide Peptobismol®, qui est utilisé pour traiter les maux d’estomac, ou le 4 juillet lorsque vous regardez des feux d’artifice. C’est un composé de bismuth qui provoque le crépitement des feux d’artifice de l’œuf de dragon.
Le dernier élément, mais non le moindre, du groupe 15 est le phosphore (P). Il a été découvert en 1669 par l’alchimiste Hennig Brandt et nommé d’après le mot grec «phosphoros», signifiant porteur de lumière. En effet, lorsque la forme élémentaire interagit avec l’oxygène atmosphérique, elle produit une lumière brillante. Les chimistes ont découvert comment exploiter le pouvoir de cette réaction pour le développement d’allumettes. La pointe rouge sur une allumette contient encore une forme de phosphore aujourd’hui.
Phosphates – régulant le devenir des cellules cancéreuses
En plus des étincelles générées par l’élément , le phosphore se trouve dans un composé appelé phosphate: le phosphore lié à quatre atomes d’oxygène.Dans les cellules, lorsqu’une molécule de phosphate est attachée à une protéine, elle peut allumer ou activer la protéine afin qu’elle puisse remplir sa fonction dans la cellule – comme une stimulation de croissance.
Lorsque le phosphate n’est plus attaché à la protéine, les cellules cessent de croître. Vous pouvez y penser presque comme les allumettes décrites ci-dessus – lorsque le phosphate est là, l’allumette peut s’enflammer et les affaires peuvent continuer. Lorsque le phosphate est éliminé, l’allumette n’est qu’un bâton et aucune lumière n’est fournie; il ne peut pas y avoir autant de travail dans l’obscurité.
Dans les cellules cancéreuses, le statut de phosphate est hors de contrôle. Imaginez beaucoup d’allumettes éclairées et une pièce très lumineuse qui peut entraîner une vague d’activité. Cette activité peut avoir de graves conséquences sur les cellules. Par exemple, une croissance et une migration non réglementées peuvent conduire au cancer.
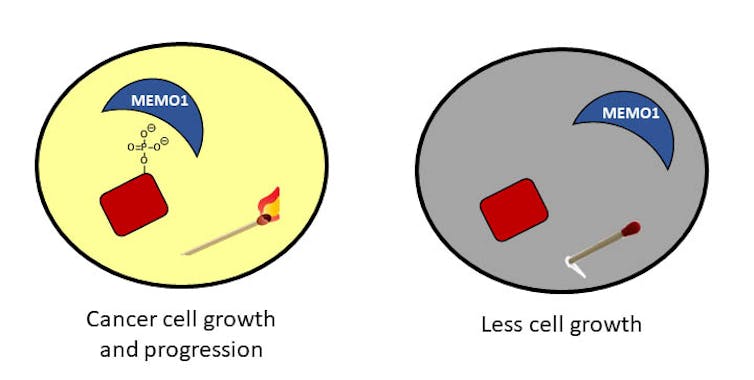
Dans mon laboratoire de l’Université de Richmond, nous nous intéressons à la compréhension de ces phosphates et d’une protéine en particulier qui interagit avec eux. Cette protéine, appelée MEMO1, se trouve en grande quantité chez les patientes atteintes d’un cancer du sein et aide les phosphates à toujours rester attachés aux protéines. Nous essayons de comprendre comment MEMO1 interagit avec ces phosphates et développons des stratégies pour perturber ces interactions.
Nous espérons que notre travail révèle un moyen d’aider à éliminer les phosphates pour arrêter la croissance incontrôlée des cellules – en d’autres termes, pour faire sauter les correspondances.
Alors la prochaine fois que vous entendrez les mots «tableau périodique», pensez à la vie. Pensez aux molécules que vous rencontrez à chaque instant de chaque jour, pensez au médicament qui vous maintient en bonne santé et pensez à ceux d’entre nous qui s’efforcent de comprendre comment vous maintenir ainsi .