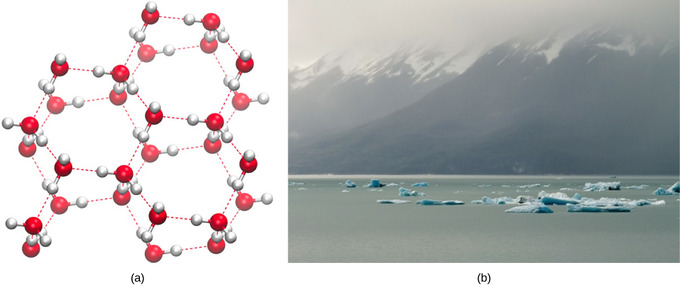
Estados da Água: Gás, Líquido e Sólido
A formação de ligações de hidrogênio é uma qualidade importante da água líquida que é crucial para a vida como a conhecemos. Como as moléculas de água fazem ligações de hidrogênio umas com as outras, a água assume algumas características químicas únicas em comparação com outros líquidos e, como os seres vivos têm um alto teor de água, entender essas características químicas é a chave para entender a vida. Na água líquida, as ligações de hidrogênio são formadas e quebradas constantemente à medida que as moléculas de água deslizam umas pelas outras. A quebra dessas ligações é causada pelo movimento (energia cinética) das moléculas de água devido ao calor contido no sistema. Quando o calor é aumentado enquanto a água é fervida, a energia cinética mais alta das moléculas de água faz com que as ligações de hidrogênio se rompam completamente e permitem que as moléculas de água escapem para o ar como gás (vapor ou vapor d’água). Por outro lado, quando a temperatura da água é reduzida e a água congela, as moléculas de água formam uma estrutura cristalina mantida por ligações de hidrogênio (não há energia suficiente para quebrar as ligações de hidrogênio). Isso torna o gelo menos denso do que a água líquida, um fenômeno não visto na solidificação de outros líquidos.
Fases da matéria: veja o que acontece com as ligações intermoleculares durante as mudanças de fase neste interativo.
A densidade mais baixa da água em sua forma sólida se deve à maneira como as ligações de hidrogênio são orientadas conforme ela congela: as moléculas de água são empurradas para mais longe em comparação com a água líquida. Com a maioria dos outros líquidos, a solidificação quando a temperatura cai inclui a redução da energia cinética entre as moléculas, permitindo que elas se compactem ainda mais do que na forma líquida e dando ao sólido uma densidade maior do que o líquido.
O baixo A densidade do gelo, uma anomalia, faz com que ele flutue na superfície da água líquida, como um iceberg ou os cubos de gelo em um copo d’água. Em lagos e lagoas, o gelo se forma na superfície da água criando uma barreira isolante que protege os animais e a vida vegetal do lago do congelamento. Sem essa camada de gelo isolante, as plantas e os animais que vivem na lagoa congelariam no bloco sólido de gelo e não poderiam sobreviver. O efeito prejudicial do congelamento em organismos vivos é causado pela expansão do gelo em relação à água líquida. Os cristais de gelo que se formam com o congelamento rompem as delicadas membranas essenciais para o funcionamento das células vivas, danificando-as irreversivelmente. As células só podem sobreviver ao congelamento se a água nelas contida for substituída temporariamente por outro líquido como o glicerol.