Jak interpretovat IR Spectra za 1 minutu nebo méně: 2 nejdůležitější věci, které je třeba hledat
Poslední příspěvek, krátce jsme představili koncept vibrací vazby a viděli jsme, že si můžeme kovalentní vazby představit tak trochu jako koule a pružiny: pružiny vibrují a každá z nich „zpívá“ charakteristickou frekvencí , což závisí na síle vazby a na hmotnostech atomů. Tyto vibrace mají frekvence, které jsou ve střední infračervené (IR) oblasti elektromagnetického spektra.
Můžeme to pozorovat a měřit „zpěv“ vazeb aplikací IR záření na vzorek a měřením frekvencí, při kterých je záření absorbováno. Výsledkem je technika známá jako infračervená spektroskopie, což je užitečný a rychlý nástroj pro identifikaci vazeb přítomných v dané molekule.
Viděli jsme, že IR spektrum vody bylo docela jednoduché – ale přesun k relativně složitá molekula, jako je glukóza (níže), jsme byli najednou konfrontováni s lesem vrcholů!
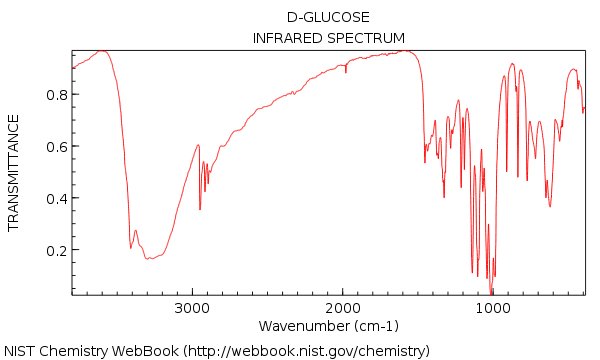
Váš první dojem z pohledu v tom IR může být: ach! jak to mám dávat smysl ??
K čemuž chci říct: nepanikařte!
Obsah
- Opravme některé běžné mylné představy o IR
- Počínaje slovem „Hunt And Peck“ není správná cesta
- IR spektroskopie: Celkový obraz
- Dvě hlavní věci, které je třeba v IR spektru hledat: „jazyky“ a „meče“.
- Alkoholy a karboxylové kyseliny: více Detail
- Specifické příklady IR spektra karbonylových funkčních skupin
- Méně zásadní, ale přesto užitečné: Dvě další velmi diagnostické oblasti.
- Glukóza, revisited: The 1 Minute Analysis
Pojďme opravit některé běžné mylné představy o IR
V tomto příspěvku chci ukázat, že typická analýza IR spektra je mnohem jednodušší, než si myslíte . Ve skutečnosti, jakmile se naučíte, co hledat, lze to často udělat za minutu nebo méně. Proč?
- IR se obecně nepoužívá k určení celé struktury neznámé molekuly. Například není naživu člověk, který by se mohl podívat na IR spektrum výše a odvodit strukturu glu cose z toho. IR je nástroj s velmi specifickým využitím.
- Nepotřebujeme analyzovat každý vrchol! (jak uvidíme později, k tomu slouží NMR: -)). Místo toho je IR skvělé pro identifikaci určitých specifických funkčních skupin, jako jsou alkoholy a karbonyly. Tímto způsobem je komplementární s jinými technikami (jako je NMR), které neposkytují tyto informace tak rychle.
S ohledem na tuto skutečnost můžeme zjednodušit analýzu IR spektra vyříznutím všechno kromě nejnižšího ovoce.
Vidíte ten les vrcholů od 500 do 1400 cm-1? V zásadě je budeme všechny ignorovat!
80% nejužitečnějších informací pro naše účely lze získat sledováním dvou konkrétních oblastí spektra: 3200-3400 cm-1 a 1650-1800 cm-1. Uvidíme také, že existují alespoň další dvě oblasti IR spektra, na které se vyplatí podívat, a tak uzavřeme analýzu „spektra prvního řádu“ neznámého.
Sečteno a podtrženo: Účelem tohoto příspěvku je ukázat vám, jak upřednostnit svůj čas při analýze infračerveného spektra.
2. Počínaje „Hunt And Peck“ není správná cesta
Co dělá typický nový student konfrontovaný s IR spektrem neznáma (a pocit rostoucí paniky)?
Často sáhnou po prvním nástroji, který dostanou, což je tabulka běžných rozsahů pro IR vrcholy, které jim dal jejich instruktor.
Dalším krokem v jejich analýze je projít spektrem z jedné strany na druhou a pokusit se spojit každý jednotlivý vrchol s jedním z čísel v tabulce . Vím to, protože to je přesně to, co jsem udělal, když jsem se poprvé naučil IR. Říkám tomu „lov a klování“.
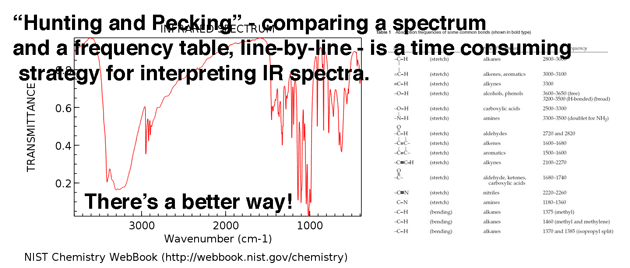
Jediní lidé, kteří jako první krok „loví a klování“, jsou lidé kteří nemají žádný plán (tj. „nováčci“).
Takže čtením několika následujících odstavců si můžete ušetřit spoustu času a zmatku.
Celkový obraz
V infračervené spektroskopii měříme, kde molekuly absorbují fotony infračerveného záření. Vrcholy představují oblasti spektra, kde dochází ke specifickým vibracím vazeb. Stejně jako pružiny různých hmotností vibrují při charakteristických frekvencích v závislosti na hmotnosti a napětí, tak i vazby.
Zde je přehled infračerveného okna od 4 000 cm -1 do 500 cm -1 se zvýrazněnými různými oblastmi zájmu.
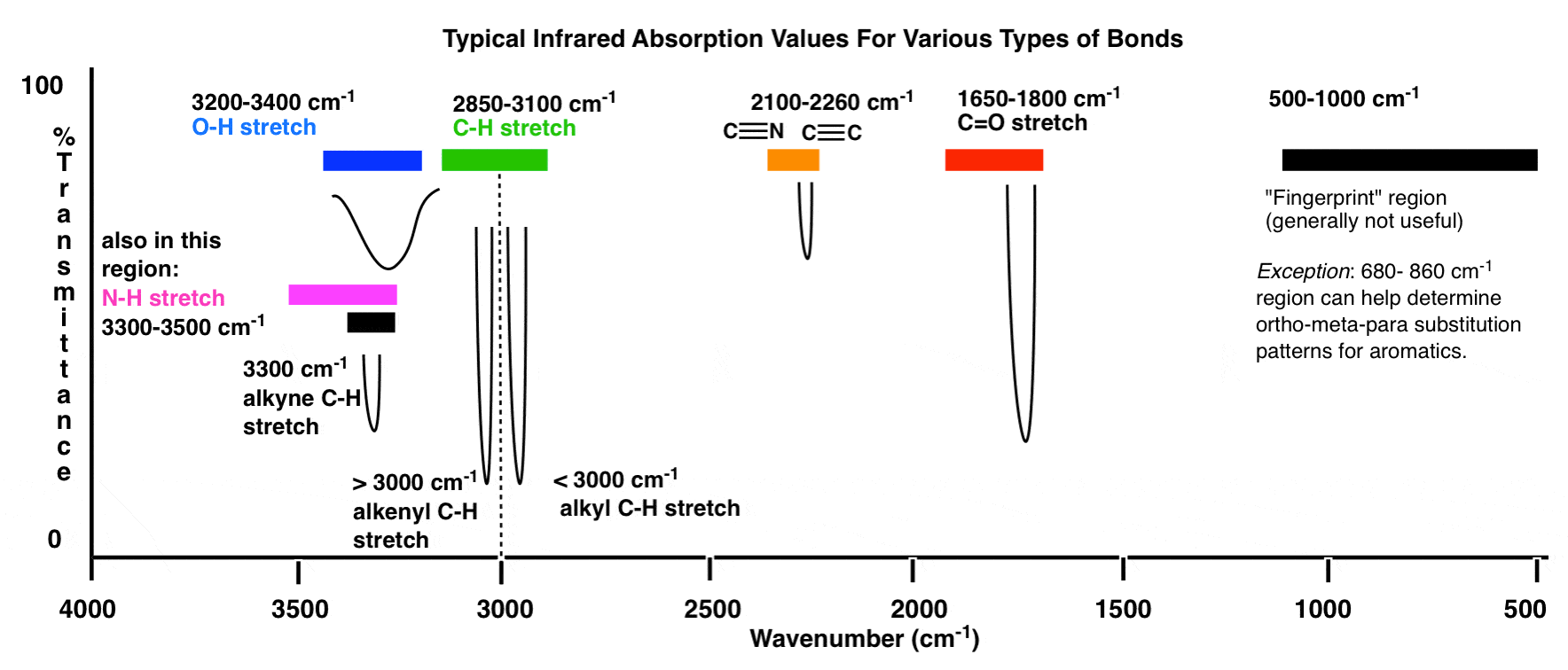
Ještě více komprimovaný přehled vypadá takto: (zdroj)
V těchto rozsazích jsou dvě oblasti s vysokou prioritou, na které se zaměříme, a dvě oblasti s nižší prioritou, diskutujte dále níže.
4. Dvě hlavní věci, které je třeba hledat v IR spektru: „Jazyky“ a „Meče“.
Při konfrontaci s novým IR spektrem upřednostněte svůj čas položením dvou důležitých otázek:
- Existuje v oblasti široký, zaoblený vrchol kolem 3 400 – 3 200 cm – 1? Tam se objevují hydroxylové skupiny (OH).
- Existuje v oblasti ostrý, silný vrchol kolem 1850 – 1630 cm-1? To je místo, kde se objevují karbonylové skupiny (C = O).
Nejprve se podívejme na několik příkladů vrcholů hydroxylových skupin v oblasti 3 400 cm-1 až 3 400 cm-1, které Jon popisuje živě jako „jazyky“. Vrcholy níže patří alkoholům. Vodíková vazba mezi hydroxylovými skupinami vede k určitým změnám v síle vazby OH, což má za následek řadu vibračních energií. Výsledkem této variace jsou široké vrcholy.
Hydroxylové skupiny, které jsou součástí karboxylových kyselin, mají ještě širší vzhled, který si trochu popíšeme.
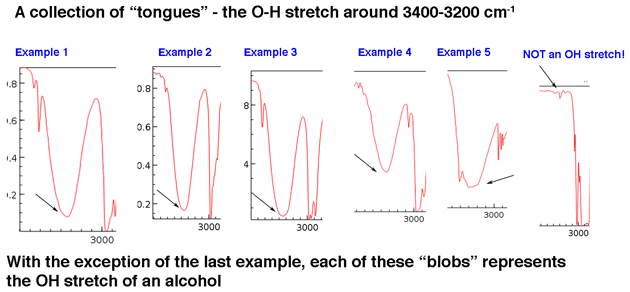
Hlavním bodem je, že hydroxylová skupina není obecně něco, co musíte hledat při základním šumu.
Ačkoli jsou hydroxylové skupiny nejběžnějším typem širokého píku v této oblasti, vrcholy NH se mohou objevit i v této oblasti (více o nich v poznámce pod čarou níže). Mají tendenci mít ostřejší vzhled a mohou se objevit jako jeden nebo dva vrcholy v závislosti na počtu NH vazeb.
Dále, le Podívejme se na některé příklady vrcholů C = O, v oblasti kolem 1630-1800 cm-1. Tyto vrcholy jsou téměř vždy nejsilnějšími vrcholy v celém spektru a jsou relativně úzké, což jim dodává poněkud „mečový“ vzhled .
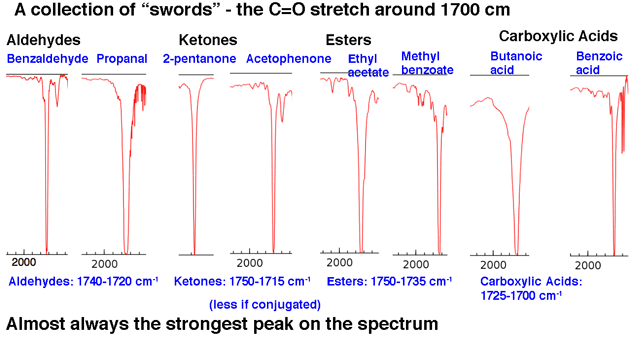
To shrnuje naši analýzu 80/20: hledejte jazyky a meče.
Pokud z tohoto příspěvku se nedozvíte nic jiného, naučte se rozpoznávat tyto dva typy vrcholů!
Dva další regiony infračerveného spektra mohou rychle přinést užitečné informace, pokud se procvičíte, abyste je hledali.
3. Hranice při 3000 cm-1 je užitečnou „hranicí“ mezi alkenem C – H (nad 3000 cm-1) a alkanem C – H (pod 3000 cm-1). To vám rychle pomůže zjistit, zda jsou přítomny dvojné vazby.
4. Vrchol v oblasti kolem 2200 cm-1 – 2050 cm-1 je jemným indikátorem přítomnosti trojné vazby. Nic jiného se v této oblasti neobjeví.
Připomenutí běžného rozumu
Nejprve několik jasných rad:
- pokud dostanete molekulární vzorec, který určí, jaké funkční skupiny byste měli hledat. smysl hledat skupiny OH, pokud ve svém molekulárním vzorci nemáte kyslík, nebo také přítomnost aminu, pokud ve vzorci chybí dusík.
- Méně zjevně vypočítejte stupně nenasycení, pokud vám bude dán molekulární vzorec, protože poskytne důležité vodítka. Nehledejte C = O ve struktuře jako C4H10O, která nemá žádné stupně nenasycení.
5. Alkoholy a karboxylové kyseliny: Více podrobností
Alkoholy
Le Podíváme se na konkrétní příklad, abychom mohli vidět všechno v perspektivě. Níže uvedené spektrum obsahuje 1-hexanol.
Všimněte si píku hydroxylové skupiny kolem 3 300 cm-1, typického pro alkohol (Tento ostrý pík kolem 3 600 cm-1 je běžným společníkem hydroxylových píku: představuje nevodíkově vázaný OH).
Jak byste očekávali od 1-hexanolu, neexistuje žádný výmluvný karbonylový pík kolem 1700 cm-1. Začátečníci by mohli být v pokušení označit silný dýkovitý vrchol asi 1450 cm-1 jako možný úsek C = O. Není. (je to pravděpodobně ohyb C-H). Variace se vyskytují pouze ve velmi úzkém rozsahu a je velmi nepravděpodobné, že byste viděli úsek C = O mnohem pod 1650 cm-1. Čím více spekter uvidíte, tím lépe budete s těmito úsudky.
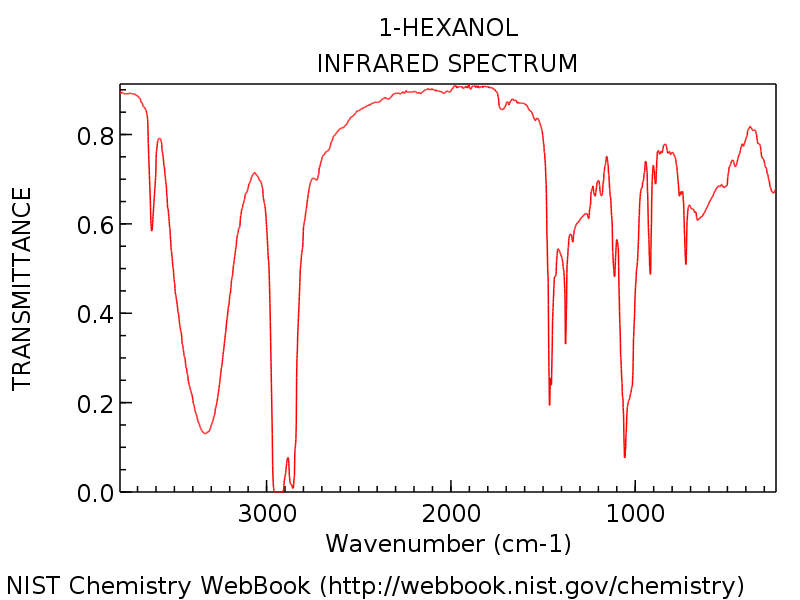
Chcete-li se seznámit s různými variantami, zde je několik dalších příkladů celých IR spekter různých alkoholů.
- Fenol
- Cyklohexanol
- 1-butanol
Karboxylové kyseliny
Hydroxylové skupiny v karboxylových kyselinách jsou podstatně širší než v alkoholech. Jon tomu říká „chlupatý vous“, což je perfektní popis. Jejich vzhled je také velmi variabilní. Absorpce OH v karboxylových kyselinách může být tak široká, že sahá pod 3000 cm-1, což do značné míry „přebírá“ levou ruku část spektra.
Zde je příklad: kyselina butanová.
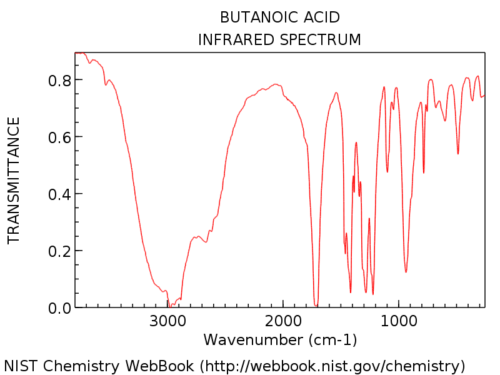
Zde je několik dalších příkladů plná spektra, abyste viděli variaci.
- Kyselina benzoová,
- kyselina pentanová,
- kyselina octová
ozdíl ve vzhledu mezi OH alkoholu a karboxylové kyseliny je obvykle diagnostický. Ve vzácných případech, kdy si nejste jisti, zda je široký pík způsoben OH alkoholu nebo karboxylové kyseliny, je doporučeno zkontrolovat oblast kolem 1700 cm na úsek C = O. Pokud chybí, pravděpodobně se díváte na alkohol.
Specifické příklady IR spektra karbonylových funkčních skupin
Druhou důležitou oblastí píku je oblast roztažení karbonylu C = O přibližně 1630-1830 cm. Karbonylové úseky jsou ostré a silné.
Jakmile uvidíte několik z nich, je nemožné si je nechat ujít. V této oblasti se neobjeví nic jiného.
Abychom to uvedli na pravou míru, zde je IR spektrum hexanalu. Tento vrchol něco po 1700 cm-1 je úsek C = O. Pokud je přítomen, úsek C = O je téměř vždy nejsilnějším vrcholem v IR spektru a nelze jej minout.
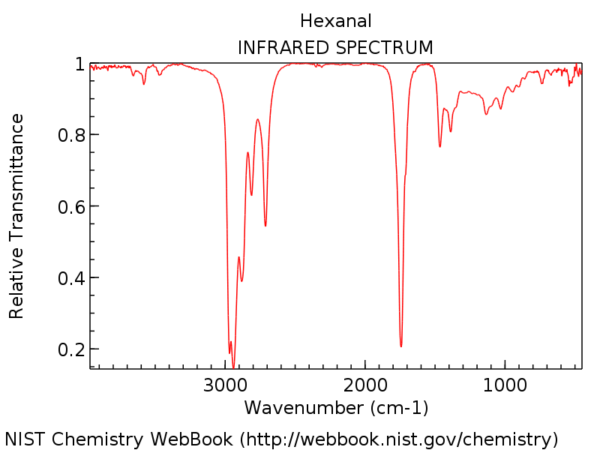
Poloha úseku C = O se mírně liší podle karbonylové funkční skupiny. Některé rozsahy (v cm-1) jsou uvedeny níže:
Konjugace poněkud ovlivní polohu úseku C = O a posune jej na nižší vlnové číslo.
Důstojné pravidlo je to, že nikdy neuvidíte úsek C = O pod 1630. Pokud například uvidíte silný vrchol na 1500, není to C = O. Je to něco jiného.
Méně zásadní, ale přesto užitečné: Dvě další velmi diagnostické oblasti.
- Hranice roztažení CH při 3000 cm-1
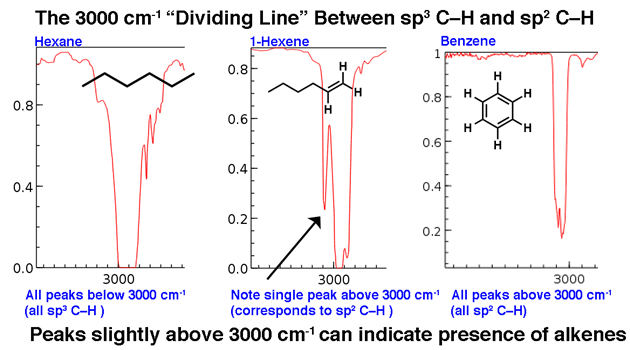
3000 cm-1 slouží jako užitečná dělicí čára. Nad touto linií jsou pozorovány vyšší frekvence C-H úseků, které připisujeme sp2 hybridizovaným C-H vazbám. Dva níže uvedené příklady: 1-hexen (všimněte si vrcholu, který je o něco vyšší) a benzen.
U molekuly, která má pouze sp3-hybrizované CH vazby, se čáry objeví pod 3000 cm-1 jako v hexanu níže.
2. Výrazná oblast trojných vazeb kolem 2200 cm-1
Molekuly s trojnými vazbami se ve velkém schématu věcí objevují relativně zřídka, ale pokud ano, mají v IR výraznou stopu.
Oblast mezi 2 000 cm-1 a 2 400 cm-1 je v IR spektrech trochu „městem duchů“; v této oblasti se toho objevuje jen velmi málo. Pokud v této oblasti uvidíte vrcholy, pravděpodobným kandidátem je uhlík s trojnou vazbou, jako je alkyn nebo nitril.
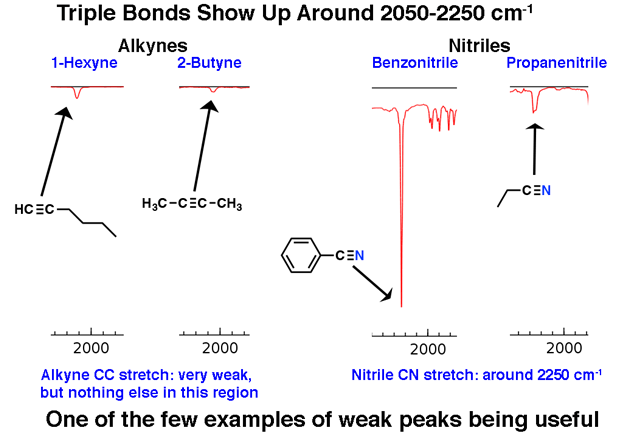
Všimněte si, jak slabé jsou alkynové vrcholy. To je jedna výjimka z pravidlo, že je třeba ignorovat slabé vrcholy. Přesto je nutná opatrnost: pokud dostanete molekulární vzorec, potvrďte, že je alkyn možný, a to výpočtem stupňů nenasycení a zajištěním, že je alespoň 2 nebo více.
Terminálové alkyny (například 1-hexyn) mají také silný úsek CH kolem 3 400 cm-1, který je silněji diagnostický.
Glukóza, znovu: analýza 1 minuty
OK. Ove 4 oblasti, které jsou užitečné pro rychlou analýzu infračerveného spektra.
Nyní se vraťme zpět a podívejme se na IR glukózy. Co vidíme?
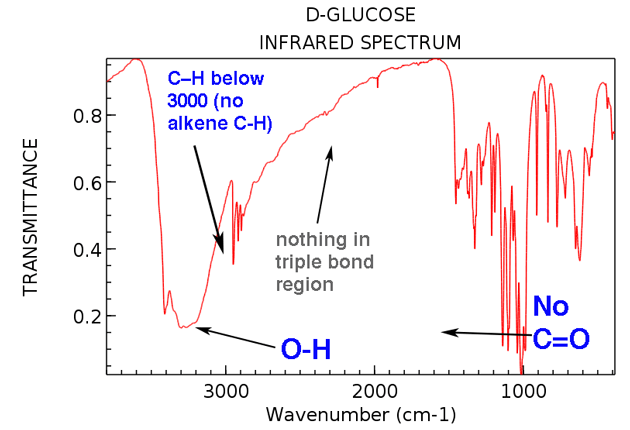
Je třeba si uvědomit dvě velké věci:
Také, pokud potřebujeme trochu času navíc:
- Žádný alken CH (žádné vrcholy nad 3000 cm-1)
- Nic v oblasti trojné vazby (vzácné, ale stále snadno se naučíte kontrolovat)
Nyní: Pokud jste dostali toto spektrum jako „neznámé“ spolu s jeho molekulárním vzorcem C6H12O6, jaké závěry byste mohli vyvodit ohledně jeho struktury?
- Molekula má alespoň jednu OH skupinu (a možná i více)
- Molekula nemá žádné C = O skupiny
- Molekula * pravděpodobně * nemá žádné alkeny. Pokud jsou přítomny nějaké alkeny, nenesou žádné CH vazby, protože bychom viděli jejich CH protáhnout se nad 3000 cm-1.
A molekula s jedním stupněm nedostatku vodíku (C6H12O6), ale bez C = O a pravděpodobně bez C = C?
Dobrý odhad by byl, že molekula obsahuje kruh. (Víme, že tomu tak je, samozřejmě, ale je hezké vidět IR potvrzující wha To už víme).
To nám může říci 1minutová analýza IR glukózy. Ne celá struktura, pamatujte, ale určitě některé důležité věci.
To je pro dnešek dost. V dalším příspěvku provedeme další 1minutové analýzy a uvedeme konkrétnější příklady toho, jak využít informace v IR spektru k vyvození závěrů o molekulární struktuře.
Více k oblasti 3200: Aminy „Amides a Terminal Alkyne CH
Zatímco jsme v oblasti 3200…. Aminy a amidy
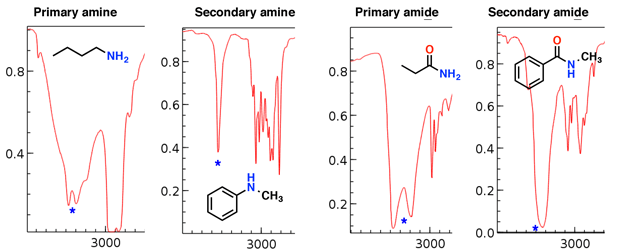
Aminy a amidy mají také N-H úseky, které se v této oblasti objevují.
Všimněte si, jak primární amin a primární amid mají dva „zuby“, zatímco sekundární amin a sekundární amid mají jediný vrchol.
Aminové úseky bývají ostřejší než amid úseky; také amidy lze odlišit silným úsekem C = O (viz níže).
Primární aminy (klikněte pro spektra)
- Anilin
- Benzylamin
- Cyklohexylamin
Sekundární aminy:
- N-methylbenzylamin
- N, N-dibenzylamin
- N-methylanilin
primární amidy
- propionamid
- benzamid
- butanamid
Sekundární amidy
- N-methylbenzamid
Terminální alkyn CH
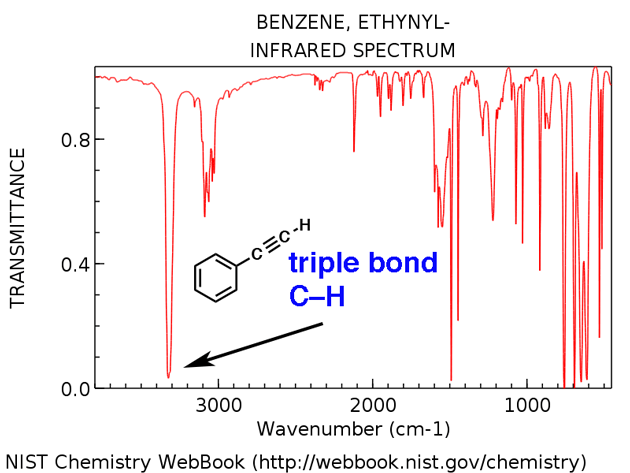
Terminální alkyny mají charakteristický úsek CH kolem 3300 cm-1. Tady je to pro ethynylbenzen, níže.
- Ethynylbenzene