Hoe IR-spectra in 1 minuut of minder te interpreteren: de 2 belangrijkste dingen om naar te zoeken
Laatste bericht, we introduceerden kort het concept van bindingstrillingen, en we zagen dat we covalente bindingen kunnen beschouwen als een beetje zoals ballen en veren: de veren trillen en ze ‘zingen’ allemaal met een karakteristieke frequentie , wat afhangt van de sterkte van de binding en van de massa van de atomen. Deze trillingen hebben frequenties die zich in het midden-infrarood (IR) gebied van het elektromagnetische spectrum bevinden.
We kunnen dit waarnemen en meten “zingen” van bindingen door IR-straling op een monster toe te passen en de frequenties te meten waarop de straling wordt geabsorbeerd. Het resultaat is een techniek die bekend staat als infraroodspectroscopie, een handig en snel hulpmiddel voor het identificeren van de bindingen die aanwezig zijn in een bepaald molecuul.
We zagen dat het IR-spectrum van water vrij eenvoudig was – maar we gingen verder met een relatief complexe molecule zoals glucose (hieronder) werden we plotseling geconfronteerd met een woud van pieken!
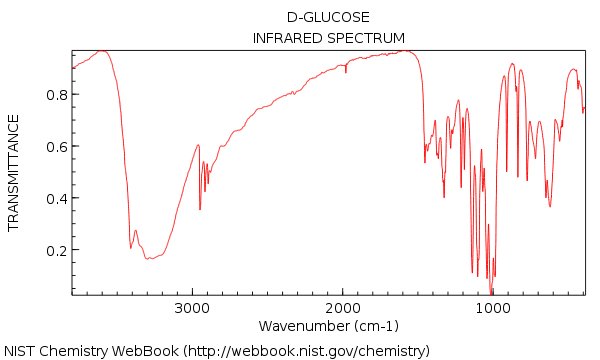
Je eerste indruk van kijken bij die IR zou kunnen zijn: agh! hoe moet ik dat begrijpen ??
Waarop ik wil zeggen: geen paniek!
Inhoudsopgave
- Laten we enkele veelvoorkomende misvattingen over IR corrigeren
- Beginnen met “Hunt and Peck” is niet de manier om te gaan
- IR-spectroscopie: het grote geheel
- De twee belangrijkste dingen om naar te zoeken in een IR-spectrum: “tongen” en “zwaarden”.
- Alcoholen en carbonzuren: meer Detail
- Specifieke voorbeelden van IR-spectra van functionele carbonylgroepen
- Minder cruciaal, maar nog steeds nuttig: nog twee zeer diagnostische gebieden.
- Glucose, opnieuw bekeken: de 1 Minuutanalyse
Laten we enkele veelvoorkomende misvattingen over IR corrigeren
In dit bericht wil ik aantonen dat een typische analyse van een IR-spectrum veel eenvoudiger is dan je misschien denkt . In feite, als je eenmaal leert waarnaar je moet zoeken, kan het vaak binnen een minuut of minder worden gedaan. Waarom?
- IR wordt over het algemeen niet gebruikt om de hele structuur van een onbekend molecuul te bepalen. Er is bijvoorbeeld geen persoon in leven die naar het IR-spectrum hierboven zou kunnen kijken en de structuur van glu zou kunnen afleiden er uit te onderscheiden. IR is een tool met een heel specifiek gebruik.
- We hoeven niet elke piek te analyseren! (zoals we later zullen zien, is dat waar NMR voor is: -)). In plaats daarvan is IR geweldig voor het identificeren van bepaalde specifieke functionele groepen, zoals alcoholen en carbonylen. Op deze manier is het complementair aan andere technieken (zoals NMR) die deze informatie niet zo snel opleveren.
Met dit in gedachten kunnen we de analyse van een IR-spectrum vereenvoudigen door alles behalve de laagste vrucht.
Zie je dat woud van toppen van 500-1400 cm-1? We gaan ze in principe allemaal negeren!
80% van de meest bruikbare informatie voor onze doeleinden kan worden verkregen door naar twee specifieke gebieden van het spectrum te kijken: 3200-3400 cm-1 en 1650-1800 cm-1. We zullen ook zien dat er ten minste twee extra regio’s van een IR-spectrum zijn die de moeite waard zijn om naar te kijken, en dus concluderen we een “eerste-orde” analyse van het IR-spectrum van een onbekende.
Kort gezegd: de Het doel van dit bericht is om u te laten zien hoe u prioriteit kunt geven aan uw tijd in een analyse van een IR-spectrum.
2. Beginnen met “Hunt and Peck” is niet de juiste keuze
Wat doet een typische nieuwe student wanneer hij wordt geconfronteerd met een IR-spectrum van een onbekende (en een gevoel van toenemende paniek)?
Ze grijpen vaak naar het eerste hulpmiddel dat ze krijgen, een tabel met veelvoorkomende bereiken voor IR-pieken die hun instructeur hun heeft gegeven.
De volgende stap in hun analyse is om van de ene kant naar de andere kant door het spectrum te gaan en elke afzonderlijke piek te matchen met een van de getallen in de tabel . Ik weet dit omdat dit precies is wat ik deed toen ik IR voor het eerst leerde. Ik noem het “jagen en pikken”.
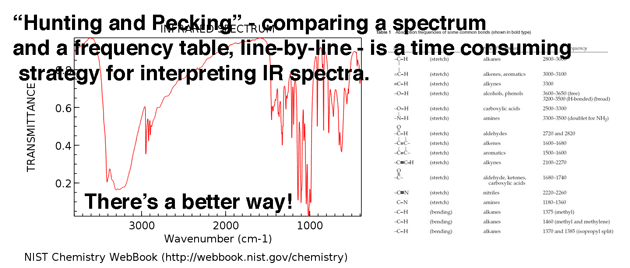
De enige mensen die “jagen en pikken” als eerste stap zijn mensen die geen plan hebben (dwz “nieuwelingen”).
Dus door de volgende paragrafen te lezen, kunt u uzelf veel tijd en verwarring besparen.
The Big Picture
In IR-spectroscopie meten we waar moleculen fotonen van IR-straling absorberen. De pieken vertegenwoordigen gebieden van het spectrum waar specifieke bindingsvibraties optreden … Net als veren met verschillende gewichten trillen op karakteristieke frequenties, afhankelijk van massa en spanning, zo ook bindingen.
Hier is een overzicht van het IR-venster van 4000 cm -1 tot 500 cm -1 met verschillende interessegebieden gemarkeerd.
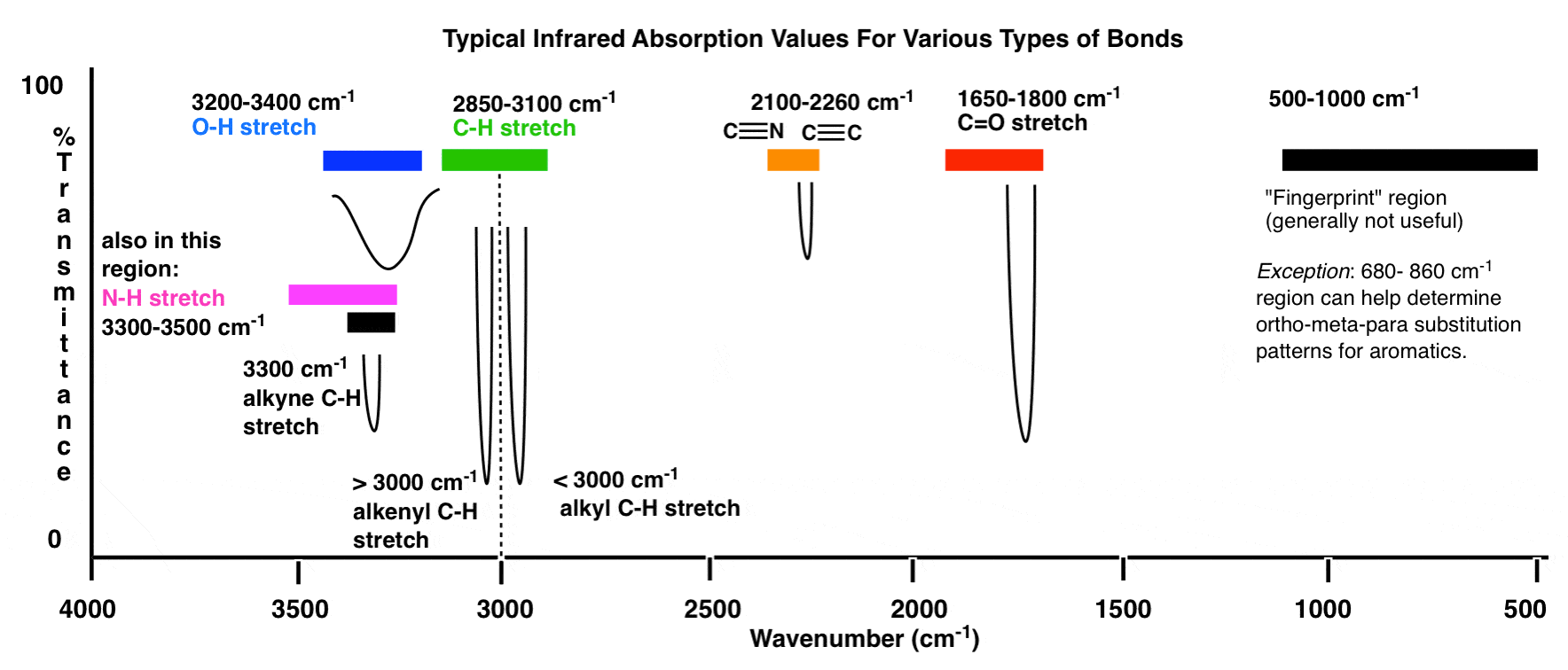
Een nog compacter overzicht ziet er als volgt uit: (bron)
Binnen deze bereiken zijn er twee gebieden met hoge prioriteit om op te focussen, en twee gebieden met minder prioriteit bespreek hieronder verder.
4. De twee belangrijkste dingen om naar te zoeken in een IR-spectrum: “Tongen” en “Zwaarden”.
Wanneer u wordt geconfronteerd met een nieuw IR-spectrum, geef dan prioriteit aan uw tijd door twee belangrijke vragen te stellen:
- Is er een brede, ronde piek in de regio rond 3400-3200 cm- 1? Dat is waar hydroxylgroepen (OH) voorkomen.
- Is er een scherpe, sterke piek in het gebied rond 1850-1630 cm-1? Dat is waar carbonylgroepen (C = O) verschijnen.
Laten we eerst eens kijken naar enkele voorbeelden van hydroxylgroeppieken in het 3400 cm-1- tot 3200 cm-1-gebied, dat Jon beschrijft levendig als “tongen”. De pieken hieronder behoren allemaal tot alcoholen. Waterstofbinding tussen hydroxylgroepen leidt tot enkele variaties in OH-bindingssterkte, wat resulteert in een reeks trillingsenergieën. De variatie resulteert in de brede waargenomen pieken.
Hydroxylgroepen die deel uitmaken van carbonzuren hebben een nog breder uiterlijk, dat we straks zullen beschrijven.
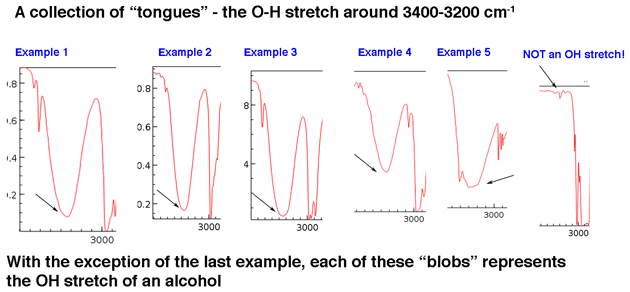
Het belangrijkste punt is dat een hydroxylgroep over het algemeen niet iets is waarnaar u op zoek hoeft te gaan in de basislijnruis.
Hoewel hydroxylgroepen het meest voorkomende type brede piek zijn in deze regio, pieken NH kunnen ook in dit gebied voorkomen (meer hierover in de voetnoot hieronder). Ze zien er meestal scherper uit en kunnen verschijnen als een of twee pieken, afhankelijk van het aantal NH-bindingen.
Vervolgens le Kijk eens naar enkele voorbeelden van C = O-pieken, in het gebied rond 1630-1800 cm-1 .. Deze pieken zijn bijna altijd de sterkste pieken in het hele spectrum en zijn relatief smal, waardoor ze een ietwat “zwaardachtig” uiterlijk krijgen .
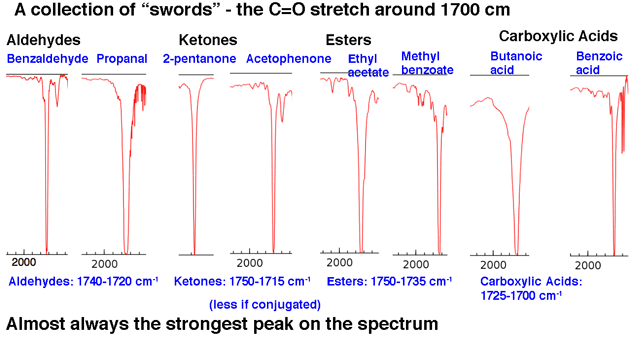
Dat is een samenvatting van onze 80/20-analyse: zoek naar tongen en zwaarden.
Als je leert niets anders van dit bericht, leer deze twee soorten pieken te herkennen!
Twee andere regio’s van het IR-spectrum kunnen snel nuttige informatie opleveren als je jezelf traint om ernaar te zoeken.
3. De lijn op 3000 cm-1 is een bruikbare “grens” tussen alkeen C – H (boven 3000 cm-1) en alkaan C – H (onder 3000 cm-1) Dit kan je helpen snel te bepalen of er dubbele bindingen aanwezig zijn.
4. Een piek in de regio rond 2200 cm-1 – 2050 cm-1 is een subtiele indicator voor de aanwezigheid van een drievoudige binding. Niets anders komt voor in deze regio.
Een gezond verstand-herinnering
Allereerst een voor de hand liggend advies:
- als u de molecuulformule krijgt, zal die bepalen naar welke functionele groepen u moet zoeken. zin om OH-groepen te zoeken als je geen zuurstofatomen in je molecuulformule hebt, of evenzo de aanwezigheid van een amine als de formule geen stikstof bevat.
- Bereken minder duidelijk de mate van onverzadiging als je de moleculaire formule, omdat het belangrijke aanwijzingen geeft. Zoek niet naar C = O in een structuur zoals C4H10O die geen enkele graad van onverzadiging heeft.
5. Alcoholen en carbonzuren: Meer details
Alcoholen
Le We kijken naar een specifiek voorbeeld, zodat we alles in perspectief kunnen zien. Het spectrum hieronder is van 1-hexanol.
Let op de hydroxylgroeppiek rond 3300 cm-1, typisch voor een alcohol (die scherpe piek rond 3600 cm-1 is een veel voorkomende aanvulling op hydroxylpieken: het vertegenwoordigt niet-waterstofgebonden OH).
Zoals je zou verwachten voor 1-hexanol, is er geen veelzeggende carbonylpiek rond de 1700 cm-1. Beginners zouden in de verleiding kunnen komen om die dolkachtige sterke piek op ongeveer 1450 cm-1 te bestempelen als een mogelijke C = O-rek. Het is niet. (het is waarschijnlijk een CH-bocht). Variaties komen alleen voor binnen een zeer smal bereik, en het is uiterst onwaarschijnlijk dat een C = O-rek veel lager is dan 1650 cm-1. Hoe meer spectra u ziet, hoe beter u deze beoordelingen kunt maken.
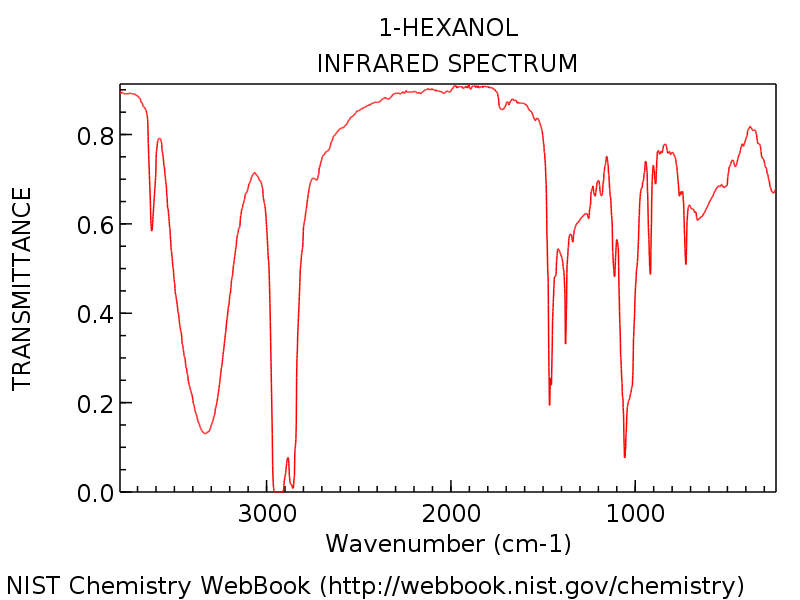
Om wat vertrouwd te raken met variatie, volgen hier enkele voorbeelden van volledige IR-spectra van verschillende alcoholen.
- Fenol
- Cyclohexanol
- 1-butanol
Carboxylzuren
Hydroxylgroepen in carbonzuren zijn aanzienlijk breder dan in alcoholen. Jon noemt het een “harige baard”, wat een perfecte omschrijving is. Hun uiterlijk is ook zeer variabel. De OH-opname in carbonzuren kan zo breed zijn dat deze zich uitstrekt tot onder 3000 cm-1, wat de linkerhand vrijwel overneemt. deel van het spectrum.
Hier is een voorbeeld: butaanzuur.
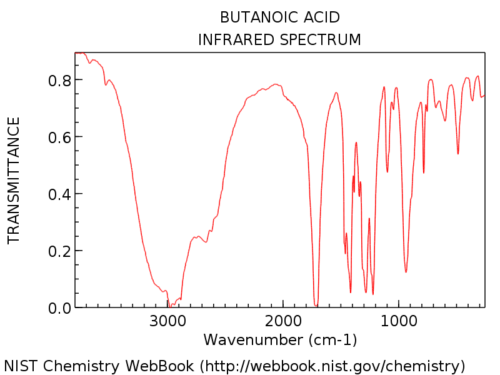
Hier zijn nog enkele voorbeelden van volledige spectra zodat u de variatie kunt zien.
- Benzoëzuur,
- pentaanzuur,
- azijnzuur
Het verschil in uiterlijk tussen de OH van een alcohol en die van een carbonzuur is meestal diagnostisch. In het zeldzame geval dat u niet zeker weet of de brede piek te wijten is aan de OH van een alcohol of een carbonzuur, is een suggestie om het gebied rond 1700 cm te controleren op het C = O-traject. Als het afwezig is, kijk je waarschijnlijk naar een alcohol.
Specifieke voorbeelden van IR-spectra van functionele carbonylgroepen
Het tweede belangrijke piekgebied is het carbonyl C = O-strekgebied op ongeveer 1630-1830 cm. Carbonyl-stukken zijn scherp en sterk.
Als je er eenmaal een paar ziet, kun je ze niet meer missen. Niets anders verschijnt in deze regio.
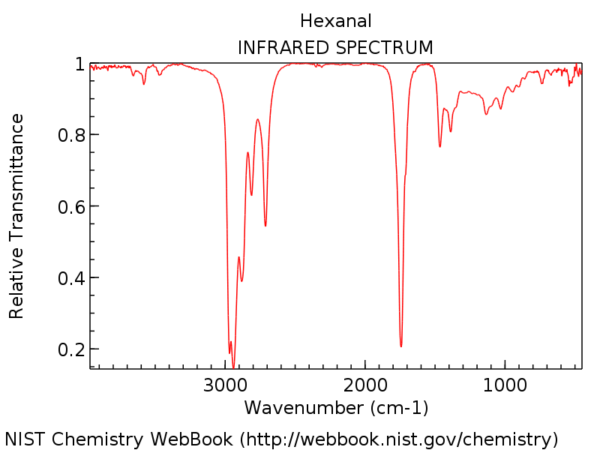
Om het in perspectief te plaatsen, hier is het IR-spectrum van hexanal. Die piek iets na 1700 cm-1 is de C = O-rek. Wanneer het aanwezig is, is de C = O-rek bijna altijd de sterkste piek in het IR-spectrum en onmogelijk te missen.
De positie van het C = O-stuk varieert enigszins per carbonylfunctionele groep. Enkele bereiken (in cm-1) worden hieronder weergegeven:
Vervoeging zal de positie van de C = O-rek enigszins beïnvloeden, waardoor het naar een lager golfgetal wordt verplaatst.
Een behoorlijke vuistregel is dat je nooit, ooit een C = O-rek onder 1630 zult zien. Als je bijvoorbeeld een sterke piek op 1500 ziet, is het niet C = O. Het is iets anders.
Minder cruciaal, maar nog steeds nuttig: nog twee zeer diagnostische gebieden.
- De CH-strekgrens op 3000 cm-1
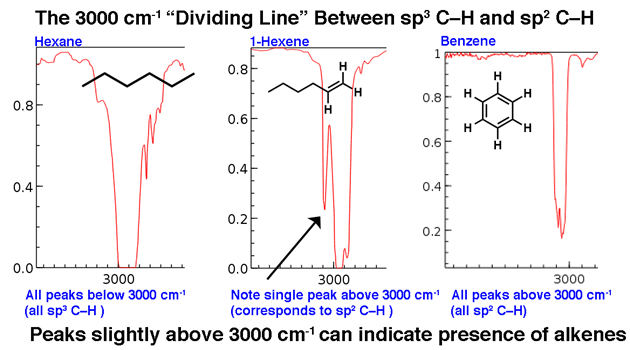
3000 cm-1 dient als een bruikbare scheidslijn. Boven deze lijn worden C-H-strekkingen met een hogere frequentie waargenomen die we toeschrijven aan sp2-gehybridiseerde C-H-bindingen. Twee voorbeelden hieronder: 1-hexeen (let op de piek die iets hoger staat) en benzeen.
Voor een molecuul met alleen sp3-gehybriseerde CH-bindingen verschijnen de lijnen onder 3000 cm-1 zoals in hexaan , hieronder.
2. Het onderscheidende drievoudige bindingsgebied rond 2200 cm-1
Moleculen met drievoudige bindingen komen relatief weinig voor in het grote geheel van dingen, maar als ze dat wel doen, hebben ze een onderscheidend spoor in de IR.
Het gebied tussen 2000 cm-1 en 2400 cm-1 is een beetje een “spookstad” in IR-spectra; er komt heel weinig voor in dit gebied. Als je pieken in dit gebied ziet, is een waarschijnlijke kandidaat dat een drievoudig gebonden koolstof, zoals een alkyn of nitril.
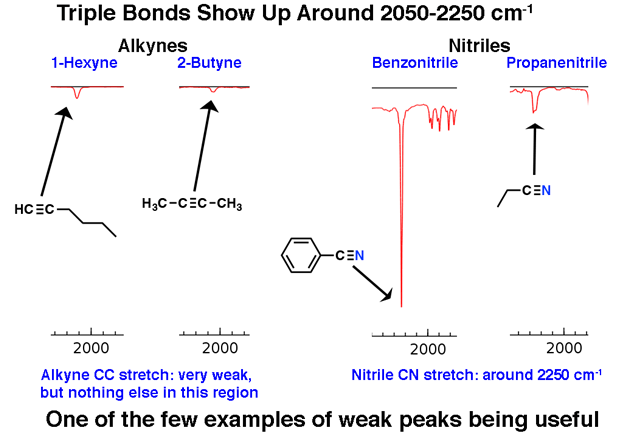
Merk op hoe zwak de alkynpieken zijn. Dit is een uitzondering op de regel dat men zwakke pieken moet negeren. Toch is voorzichtigheid geboden: als je de molecuulformule krijgt, bevestig dan dat een alkyn mogelijk is door de mate van onverzadiging te berekenen en ervoor te zorgen dat deze minstens 2 of meer is.
Terminal alkynen (zoals 1-hexyne) hebben ook een sterke CH-rek rond 3400 cm-1 die sterker diagnostisch is.
Glucose, opnieuw bezocht: de 1-minuutanalyse
OK, we zijn vertrokken 4 regio’s die handig zijn voor een snelle analyse van een IR-spectrum.
Laten we nu teruggaan en kijken naar de IR van glucose. Wat zien we?
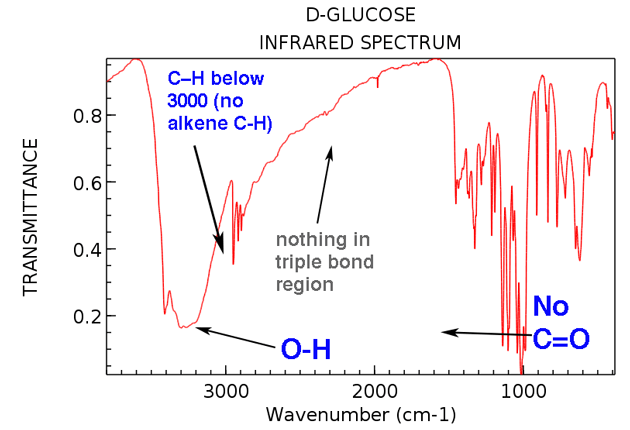
Hier zijn de twee belangrijke dingen om op te merken:
Ook als we nemen wat extra tijd die we kunnen zien:
- Geen alkeen CH (geen pieken boven 3000 cm-1)
- Niets in triple bonded-gebied (zeldzaam, maar toch wat gemakkelijk te leren is om te controleren)
Nu: als u dit spectrum als “onbekend” zou krijgen, samen met zijn moleculaire formule, C6H12O6, welke conclusies zou u dan kunnen trekken over de structuur ervan?
- Het molecuul heeft minstens één OH-groep (en mogelijk meer)
- Het molecuul heeft geen C = O-groepen
- Het molecuul * waarschijnlijk * heeft geen alkenen. Als er alkenen aanwezig zijn, dragen ze geen CH-bindingen, omdat we hun CH-lengte boven 3000 cm-1 zien.
A molecuul met één graad waterstofdeficiëntie (C6H12O6) maar geen C = O, en waarschijnlijk ook geen C = C?
Een goede gok zou zijn dat het molecuul een ring bevat. (we weten dat dit het geval is, natuurlijk, maar het is leuk om te zien dat de IR bevestigt wat t weten we al).
Dit is wat een 1-minuut analyse van de IR van glucose ons kan vertellen. Let wel, niet de hele structuur, maar zeker enkele belangrijke stukjes en beetjes.
Dat is genoeg voor vandaag. In de volgende post zullen we nog wat analyses van 1 minuut doen en meer concrete voorbeelden geven van hoe we de informatie in een IR-spectrum kunnen gebruiken om conclusies te trekken over moleculaire structuur.
Meer over de 3200-regio: Amines , Amides en Terminal Alkyne CH
Terwijl we in de 3200-regio zijn…. Aminen en amiden
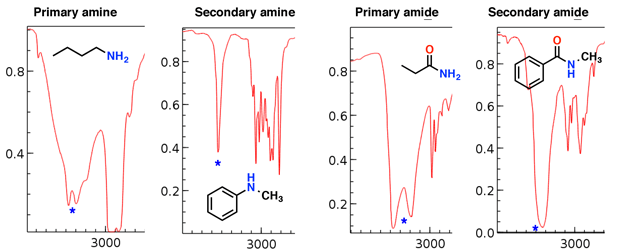
Aminen en amiden hebben ook NH-stukken die in deze regio voorkomen.
Merk op hoe het primaire amine en het primaire amide twee “hoektanden” hebben, terwijl het secundaire amine en het secundaire amide een enkele piek hebben.
De aminestukken zijn meestal scherper dan het amide strekt zich uit; ook de amiden kunnen worden onderscheiden door een sterke C = O-rek (zie hieronder).
Primaire aminen (klik voor spectra)
- Aniline
- Benzylamine
- Cyclohexylamine
Secundaire aminen:
- N-methylbenzylamine
- N, N-dibenzylamine
- N-methylaniline
Primaire amiden
- Propionamide
- Benzamide
- Butaanamide
Secundaire amiden
- N-methylbenzamide
Terminal alkyn CH
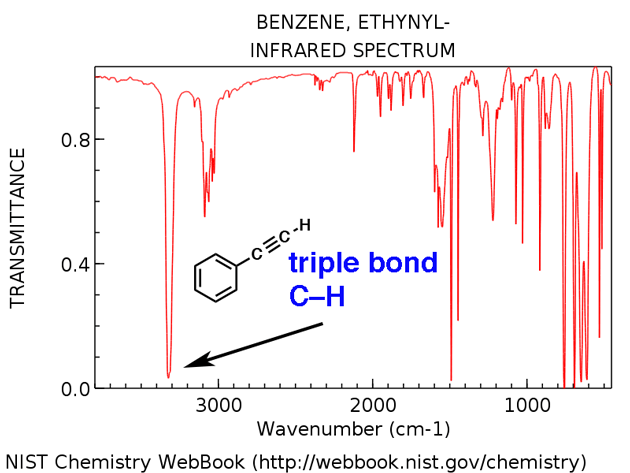
Terminal alkynen hebben een karakteristieke CH-rek rond 3300 cm-1. Hier is het voor ethynylbenzeen, hieronder.
- Ethynylbenzeen